Clear Sky Science · ru
Секретная система выделения VI у Acinetobacter: механизмы, биология и терапевтический потенциал
Скрытое оружие в госпитальных микробах
Многие знают, что некоторые госпитальные микробы умеют противостоять антибиотикам, но меньше кто представляет, что эти микроорганизмы ведут ожесточённые схватки друг с другом. В этом обзоре рассматривается микроскопическое «пружинящее копьё» у Acinetobacter — группы бактерий, в которую входит пресловутый внутрибольничный штамм Acinetobacter baumannii. Понимание того, как действует это встроенное оружие, когда оно включается и как помогает инфекции укореняться, может открыть новые пути для диагностики и обезвреживания опасных, устойчивых к лекарствам инфекций.
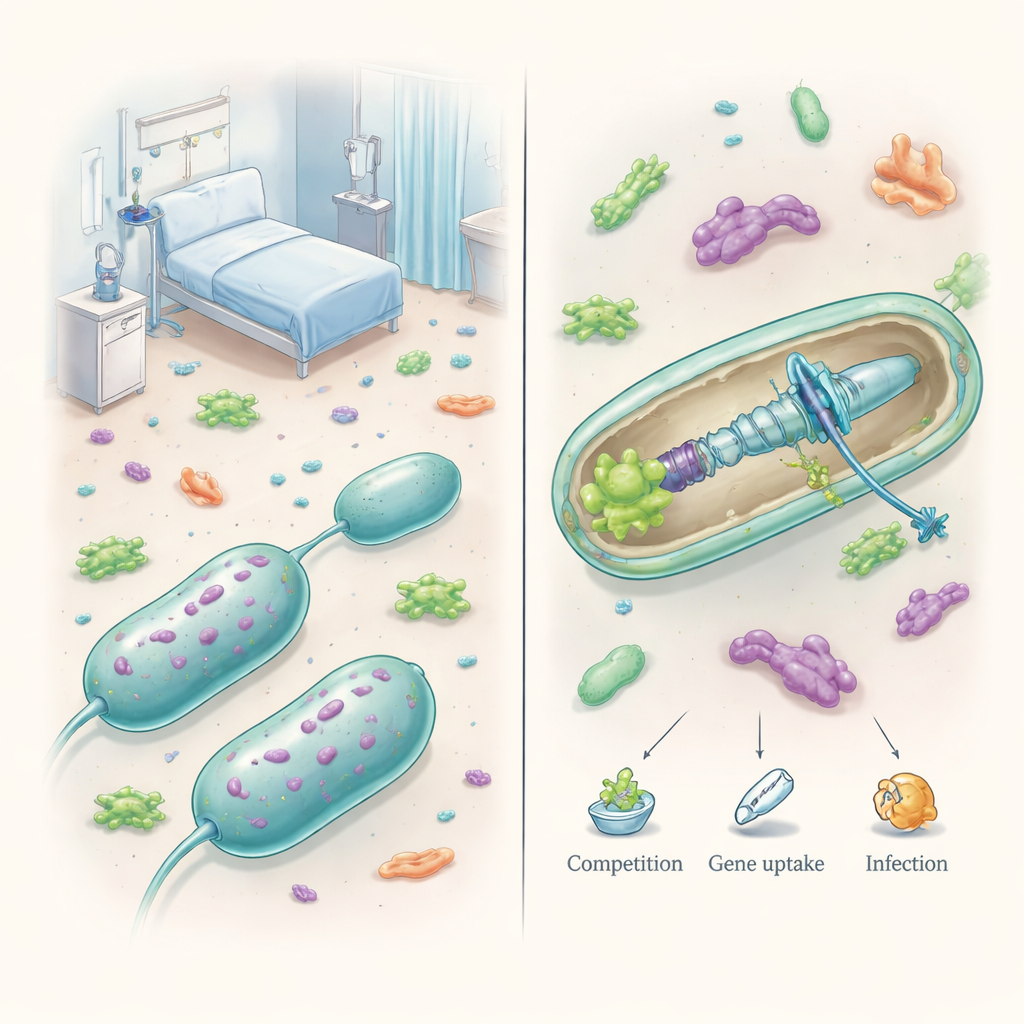
Машина для выживания, а не просто ядовитая стрела
Виды Acinetobacter обитают в почве, воде и на коже человека, но некоторые из них стали очень успешными госпитальными патогенами. Ключевой инструмент в их арсенале — система выделения типа VI, или T6SS, крошечный сокращающийся аппарат, встроенный в оболочку клетки. При срабатывании он выбрасывает шипообразный стержень, нагруженный токсическими белками, в соседние клетки, часто убивая конкурирующие бактерии на место. В отличие от некоторых других микроорганизмов, у которых есть несколько вариантов этой системы, патогенные Acinetobacter обычно имеют только одну T6SS, однако они перестроили эту единственную платформу для множества задач — от отражения соперников до формирования инфекции.
Перестроенное оборудование: необычная пусковая платформа
Большинство бактерий строят свою T6SS вокруг стандартного набора частей, но Acinetobacter перестроил несколько ключевых компонентов. Ему не хватает обычного внешне-мембранного анкера TssJ; вместо этого система опирается на трио специализированных помощников: TsmK образует основание во внутренней мембране, TslA стабилизирует длинный «туннельный» белок (TssM), проходящий через стенку клетки, а TagX локально разрезает стенку, освобождая место для оружия. Кроме того, конкретный белок-шип VgrG1 должен быть почти идеально сложен, чтобы система вообще сработала — замена одного аминокислотного остатка может её отключить. Вместе эти модификации демонстрируют, как эволюция способна заменить отсутствующие части новыми решениями, сохранив при этом основной принцип выстрела.
Умное управление: когда имеет смысл режим атаки
Сборка и выстрел этого наномеханизма дорого обходятся, поэтому Acinetobacter держит его под строгим контролем. Глобальный ДНК-связывающий белок (H‑NS) и специальные репрессоры, находящиеся на плазмидах с множественной лекарственной устойчивостью, могут зафиксировать систему в положении «выключено», особенно когда гены устойчивости передаются между клетками. При высокой плотности популяции химические «кворумные» сигналы могут включить её, готовя бактерии к тесной конкуренции. Ионы металлов тоже играют роль: при окислительном стрессе поступающий марганец активирует малую РНК, которая приводит к разрушению ключевых сообщений T6SS, снижая активность оружия в пользу выживания внутри хозяина. Даже капсула — сахаристое внешнее покрытие — служит одновременно щитом и тормозом: она блокирует входящие атаки, но также физически ослабляет собственную стрельбу Acinetobacter.
Разнообразный набор микроскопических ударов
Когда Acinetobacter всё же нажимает на курок, он может доставить широкий спектр токсинов. Одни ферменты разрушают жёсткую клеточную стенку соперников; другие медленно подтачивают клеточные мембраны, а третьи расщепляют ДНК внутри мишени. Каждый токсин сопровождается соответствующим «иммунным» белком, который защищает нападающего от дружественного огня. Один из ДНК-режущих токсинов, ныне называемый TafE, способен даже убивать грибы, что указывает на межцарственные столкновения в таких местах, как кишечник или лёгкие. Геномные исследования предполагают, что Acinetobacter кодируют ещё множество неизученных токсинов, часто собранных в большие Rhs-белки, выступающие как модульные носители. Вместо того чтобы полагаться на единичный удар, эти бактерии, по-видимому, используют многоуровневые атаки, повреждающие сразу несколько жизненно важных структур.
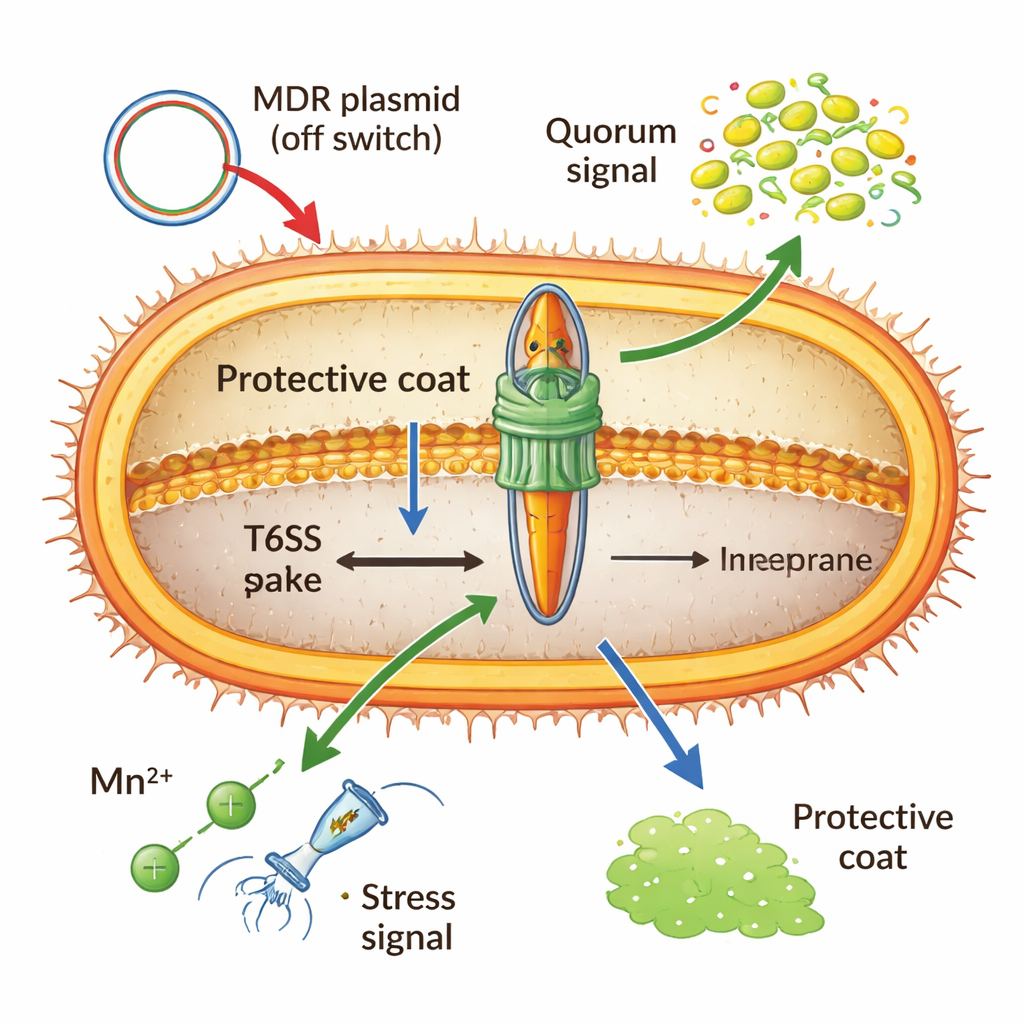
Формирование инфекций, генов и будущих методов лечения
Данные из изолятов пациентов и моделей на животных указывают, что активная T6SS часто сопровождается более тяжёлым течением болезни, усиленным воспалением и лучшим выживанием бактерий внутри хозяина. Убивая соседние микроорганизмы, система также высвобождает ДНК, которую естественно компетентные клетки Acinetobacter могут поглощать, ускоряя распространение признаков, таких как устойчивость к антибиотикам. Тем не менее постоянное поддержание оружия в активном состоянии дорого обходится, поэтому многие успешные внутрибольничные штаммы несут плазмиды или мутации, которые заглушают её после закрепления устойчивости. В целом авторы утверждают, что эту систему выделения следует рассматривать не как простой фактор вирулентности, а как гибкий «модуль приспособленности», который Acinetobacter настраивает вверх или вниз, чтобы балансировать агрессию, персистенцию и энергозатраты. Этот новый взгляд указывает на практические применения — от вакцин, нацеленных на консервативные части T6SS, до препаратов, селективно блокирующих механизм выстрела, что поможет врачам перехитрить опасного и адаптирующегося внутрибольничного противника.
Цитирование: Jie, J., Gu, S., Li, D. et al. The type VI secretion system of Acinetobacter: mechanisms, biology and therapeutic potential. Commun Biol 9, 327 (2026). https://doi.org/10.1038/s42003-026-09782-w
Ключевые слова: Acinetobacter, система выделения типа VI, устойчивость к антибиотикам, бактериальная конкуренция, госпитальные инфекции