Clear Sky Science · ru
Участие оси гипоталамус–рафе магнус–спинной центр дефекации в стресс-индуцированной дефекации у крыс
Почему стресс расстраивает живот
Большинство людей испытывали бурлящий живот, внезапную необходимость в туалете или даже диарею в стрессовых ситуациях — при экзаменах или публичных выступлениях. Хотя связь «ум—кишечник» хорошо известна, точные нервные пути, превращающие психологический стресс в стремление бежать в туалет, оставались удивительно неясными. Это исследование на крысах выявляет конкретную цепочку мозговых и спинальных цепей, которая связывает эмоциональный стресс с мощными сокращениями в нижней части кишечника, помогая объяснить, почему стресс так часто проявляется в туалете.
Маршрут от тревоги к кишечнику через мозг
Исследователи сосредоточились на области мозга, называемой гипоталамусом, ключевом центре контроля эмоций и вегетативных функций организма. Ранее показали, что стресс активирует гипоталамус и ствол мозга, и что эти области могут ускорять движения в толстой кишке. Однако точный путь передач сигналов от мозга к удалённой нижней части толстой кишки и прямой кишке, важным для дефекации, был неизвестен. С помощью трассирующих вирусов, перемещающихся вдоль нервных волокон, команда картировала нейроны, соединяющие гипоталамус со структурами ствола мозга, известными как рафе магнус, и далее вниз по спинному мозгу в направлении таза.
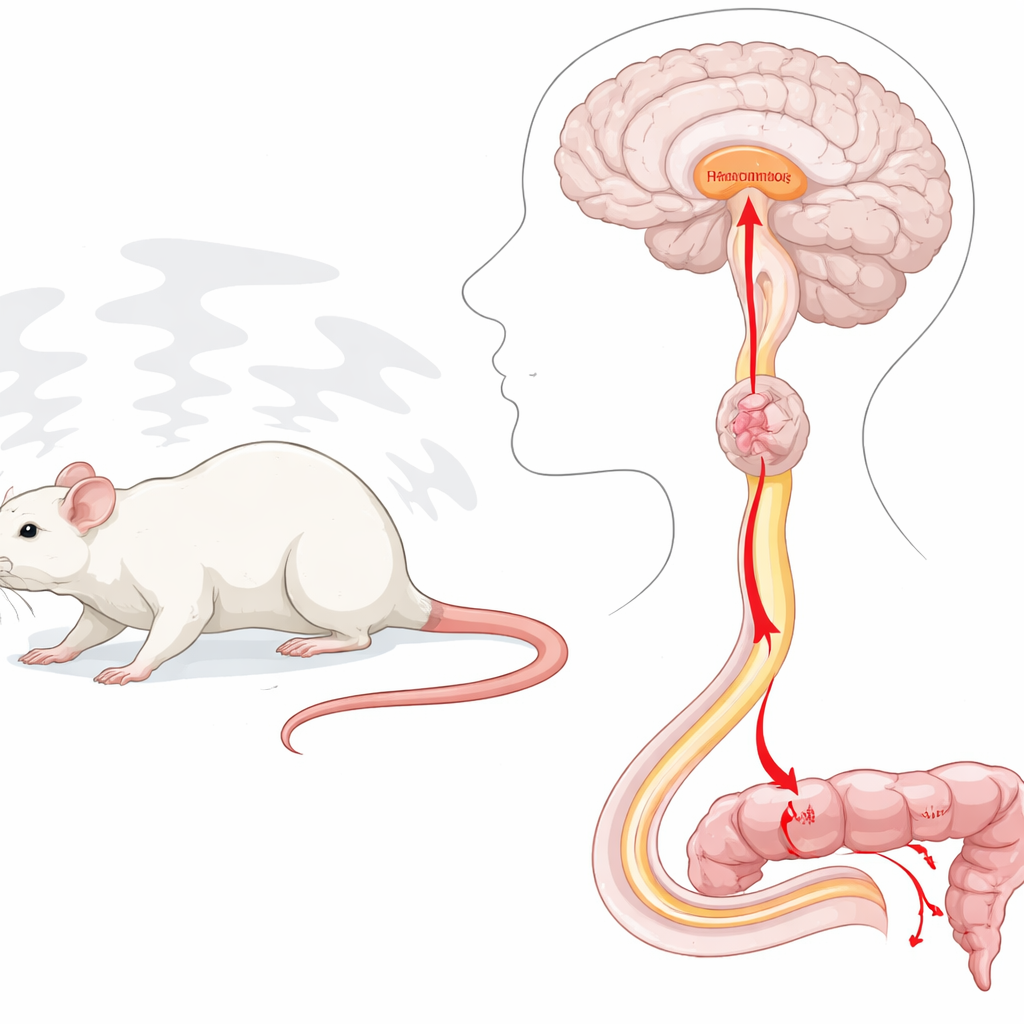
Стресс «включает» конкретную цепочку мозг–спинной мозг–кишечник
Чтобы смоделировать психологический стресс, крыс помещали на небольшую платформу, окружённую водой — классическая модель «избегания воды», которая надёжно вызывает тревогу и увеличение дефекации. Учёные обнаружили, что при этом стрессе активируются нейроны гипоталамуса, проектирующиеся в рафе магнус. Когда они химически возбуждали те же зоны гипоталамуса — особенно паравентрикулярную и дорсомедиальную области — у анестезированных крыс нижняя часть толстой кишки демонстрировала энергичные, пропульсивные сокращения, а у животных повышались артериальное давление и частота сердечных сокращений. Блокирование гормонов, связанных со стрессом, называемых кортикотропин-высвобождающими факторами, не прекращало эти кишечные сокращения, что указывало на участие другой системы сигналов.
От ствола мозга к спинному мозгу и тазовому нерву
Следующим вопросом было, как активация в мозге достигает мышц кишечника. Команда показала, что рафе магнус посылает длинные нисходящие волокна, которые выделяют медиатор серотонин в пояснично-крестцовом отделе спинного мозга, где находится центр дефекации. Когда исследователи наносили препараты непосредственно на спинной мозг, блокируя два ключевых типа серотониновых рецепторов, толщина кишки переставала реагировать на активацию гипоталамуса. Аналогично, перерезка тазового нерва — который передаёт парасимпатические сигналы от спинного мозга к прямой и дистальной части толстой кишки — устраняла усиленную моторику. Вместе эти эксперименты выявляют непрерывный путь: гипоталамус → рафе магнус → спинной центр дефекации → спинной выход через тазовый нерв к кишечнику.
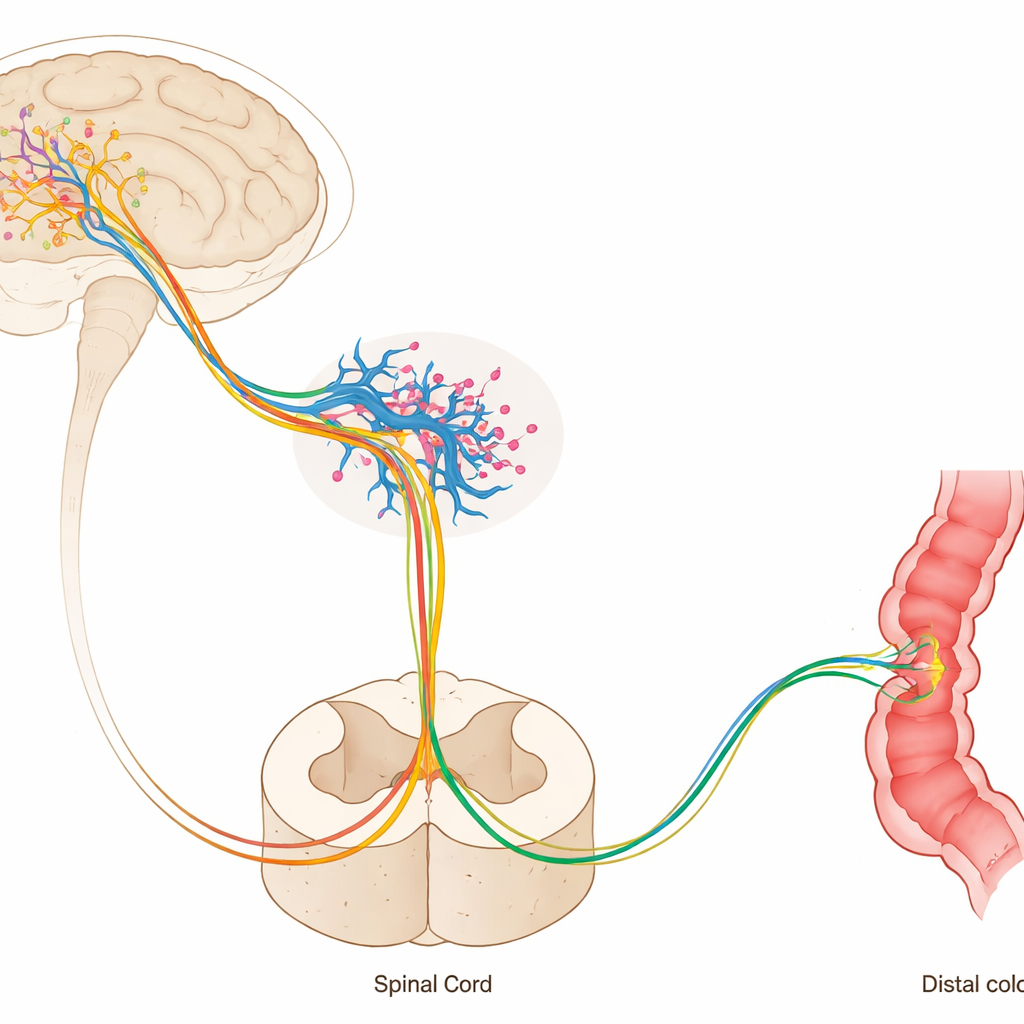
Окситоцин даёт серотонинергическим нейронам команду
Чтобы понять, что активирует нейроны рафе магнус в этой цепочке, исследователи изучили двух кандидатов: глутамат, распространённый быстрый нейротрансмиттер, и окситоцин, более известный как «гормон привязанности». Вводя направленные препараты в рафе магнус при искусственной стимуляции гипоталамуса, они обнаружили, что блокирование окситоциновых рецепторов резко снижало сокращения толстой кишки, тогда как блокада глутаматных рецепторов этого не делала. Микроскопическая визуализация подтвердила, что волокна, содержащие окситоцин из гипоталамуса, тесно контактируют с серотонин-продуцирующими нейронами рафе, которые проецируют вниз в спинной мозг. По сути, окситоцин, выделяемый в рафе, по-видимому, «включает» серотонинергические клетки, которые затем активируют спинной центр дефекации.
Выключение пути уменьшает стресс-индуцированные испражнения
Наконец, команда задала вопрос, действительно ли этот путь важен у бодрствующих животных в условиях стресса. С помощью современной «хемогенетической» методики они запрограммировали только те нейроны гипоталамуса, которые проецируются в рафе магнус, чтобы нести специальный, активируемый препаратом выключатель. При включении этого выключателя стимуляция гипоталамуса больше не усиливала моторику толстой кишки, артериальное давление или частоту сердечных сокращений у анестезированных крыс. Самое поразительное: у свободно движущихся крыс, подвергнутых стрессу избегания воды, заглушение этого пути значительно снизило число экскрементов, которые они выделяли, хотя сама стрессовая ситуация не изменилась. Это показывает, что ось гипоталамус–рафе–спинной мозг–тазовый нерв не просто существует, но и необходима для полного проявления стресс-индуцированной дефекации.
Что это значит для проблем с кишечником у людей
Проще говоря, исследование выявляет конкретную цепочку «тревога→кишечник»: чувствительные к стрессу клетки гипоталамуса активируют окситоцин-чувствительные серотонинергические нейроны ствола мозга, которые в свою очередь стимулируют спинальные и тазовые нервы, заставляя нижнюю часть толстой кишки сокращаться и опорожняться. Хотя работа проведена на крысах, аналогичная проводка, вероятно, существует и у людей и может помочь объяснить, почему одни люди при стрессе страдают диареей, а другие — запорами. Указание на конкретные мозговые и спинальные узлы открывает новые точки входа для понимания и, в перспективе, лечения стресс-чувствительных расстройств кишечника, таких как синдром раздражённого кишечника, при котором разговор между мозгом и кишечником даёт сбой.
Цитирование: Yuki, N., Sawamura, T., Mori, A. et al. Involvement of the hypothalamus–raphe magnus–spinal defecation center axis in stress-induced defecation in rats. Commun Biol 9, 411 (2026). https://doi.org/10.1038/s42003-026-09779-5
Ключевые слова: стресс и функция кишечника, связь мозга и кишечника, моторика толстой кишки, окситоцин и серотонин, синдром раздражённого кишечника