Clear Sky Science · ru
Моделирование, основанное на темпе роста, указывает на то, что фенотипическая адаптация приводит к лекарственной устойчивости при меланоме с мутацией BRAFV600E
Раковые клетки, которые учатся жить с препаратами
Таргетные препараты изменили подход к лечению многих пациентов с меланомой, серьезным видом рака кожи. Тем не менее эти препараты почти всегда перестают работать: опухоли, которые раньше уменьшались, снова начинают расти. В этом исследовании поставлен простой, но важный вопрос: могут ли клетки меланомы «научиться» переживать лечение, меняя свое поведение, вместо того чтобы полагаться лишь на генетические мутации — и может ли такое обучение объяснить, почему некоторые режимы введения препаратов работают лучше других?
От чувствительных клеток к выжившим
Исследователи сосредоточились на клетках меланомы с распространенной мутацией в гене BRAF, из-за которой они особенно чувствительны к классу препаратов, известных как ингибиторы BRAF. В лабораторных экспериментах из предыдущих работ эти клетки подвергались воздействию препарата энкорафениба в разных дозах и в разные промежутки времени. Тщательно измеряя скорость их роста или гибели в каждой из условий, авторы разделили клетки на две широкие категории: «лекарственно наивные» клетки, которые никогда ранее не встречались с препаратом, и «адаптированные» клетки, которые жили в присутствии препарата по крайней мере неделю. Лекарственно наивные клетки хорошо росли без лечения, но сильно замедлялись или гибнули под действием препарата. Адаптированные клетки, напротив, росли лучше в присутствии препарата, но теряли это преимущество после его снятия — что указывает на то, что их выживание связано с гибким, обратимым изменением состояния, а не с постоянным генетическим повреждением.
Карта скрытых поведенческих состояний клеток
Чтобы осмыслить эти изменения, команда построила математическую модель, в которой каждой раковой клетке присваивается «фенотипическое состояние» — абстрактная позиция на шкале от очень чувствительного к очень устойчивому к препарату. Вместо предположения о наличии только двух типов клеток они включили множество промежуточных состояний, отражая постепенные сдвиги в биомаркерах устойчивости. Для каждой комбинации состояния и дозы препарата они оценивали чистую скорость роста, которая могла быть положительной (делений больше, чем смертей) или отрицательной (смертей больше, чем делений). Все эти скорости были организованы в сетку, или «матрицу приспособленности», которая действует как ландшафт: в одних состояниях и при одних дозах клетки чувствуют себя хорошо, в других — гибнут. В модели клетки могут перемещаться по этому ландшафту шаг за шагом по мере включения или выключения лечения.
Клетки дрейфуют или поднимаются к преимуществу?
Ключевым неизвестным было то, как именно клетки перемещаются по этому ландшафту. Авторы протестировали четыре возможные стратегии. В одной клетки никогда не меняют состояния, значит любые устойчивые клетки должны присутствовать изначально. В другой клетки блуждают случайно между соседними состояниями, подобно пьяной прогулке, независимо от того, становится ли им лучше. В двух оставшихся стратегиях клетки склонны перемещаться в сторону состояний с более высокой скоростью роста — либо с шумом и некоторыми ошибками, либо сильно, всегда поднимаясь к лучшей выживаемости. При запуске компьютерных симуляций и сравнении их с реальными лабораторными данными, особенно экспериментами с непрерывным введением препарата и с чередованием (неделя приема — неделя перерыва), только стратегии, в которых клетки поднимаются к более высокой приспособленности, смогли воспроизвести наблюдаемое: прерывистая терапия высокой дозой лучше подавляла количество клеток, чем непрерывное лечение при том же общем времени и при большем суммарном количестве препарата.
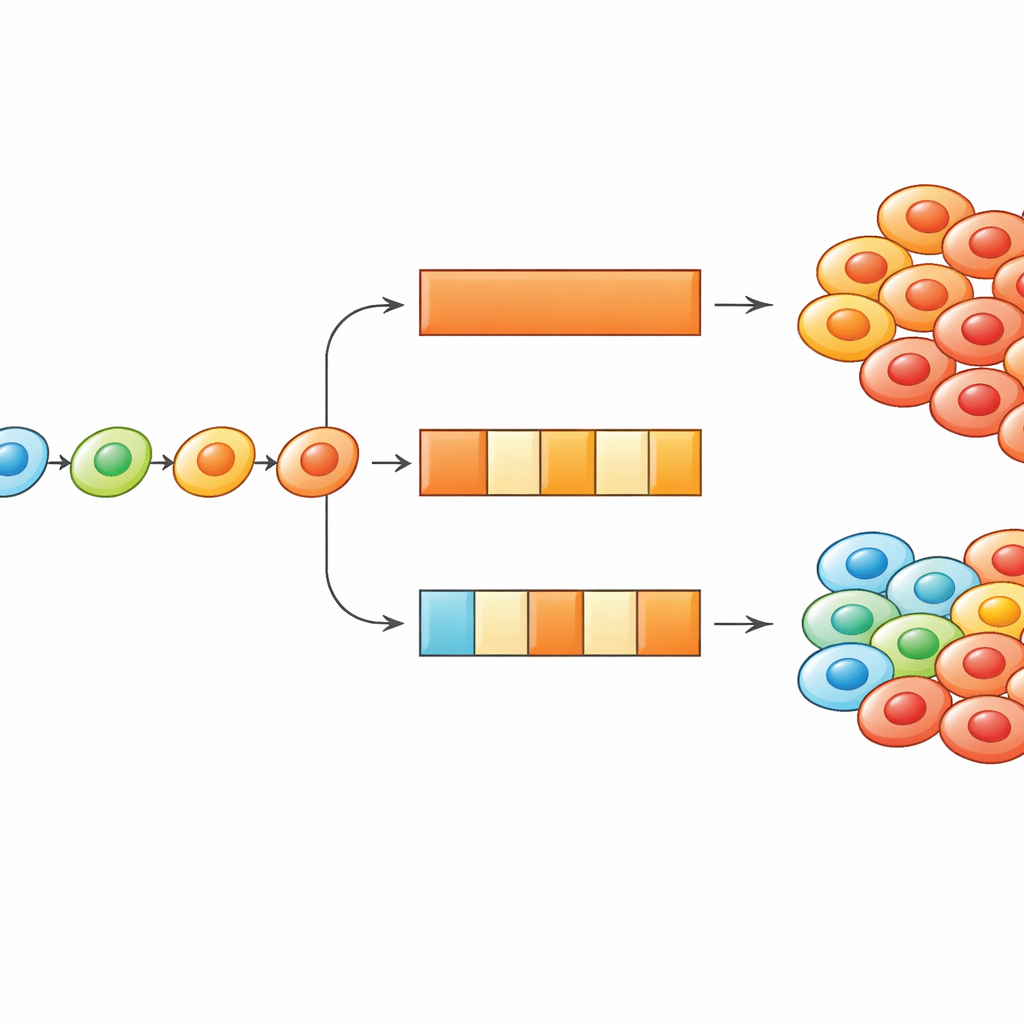
Использование режимов «вкл–выкл», чтобы обратить адаптацию против рака
Углубляясь, исследователи с помощью симуляций и упрощенных уравнений изучили, как часто клетки могут менять состояние и какова длительность периодов «препарат включен» и «препарат выключен». Они обнаружили, что при направленной адаптации режимы лечения можно настроить либо чтобы замедлять, либо чтобы использовать эту адаптацию. Уменьшение частоты обновления состояния клеток — концептуально, замедление биологических механизмов, обеспечивающих фенотипические изменения — делает прерывистые режимы более эффективными, потому что клетки не успевают быстро подняться в высокоустойчивые состояния. Наоборот, если клетки изначально находятся в сильно устойчивом состоянии, перерывы в приеме позволяют им скользнуть обратно к более чувствительным состояниям, так что повторное введение препарата вызывает всплеск гибели клеток. Исследование показывает, как тайминг дозирования и скорость клеточной адаптации вместе определяют, какой режим будет оптимальным.
Что это значит для будущей помощи при раке
Для непрофессионала главный посыл состоит в том, что раковые клетки не являются фиксированными врагами — они меняют форму. В этой системе меланомы клетки, по-видимому, активно смещаются в сторону поведенческих состояний, которые помогают им расти в данных условиях. Модель авторов показывает, что эта направленная адаптация сама по себе — без привлечения разных постоянных клонов — может объяснить, почему режимы «вкл–выкл» иногда превосходят постоянное дозирование, даже если при них используется меньше препарата в целом. Хотя эти результаты получены на клетках, выращенных в лаборатории, и требуют дополнительных исследований прежде чем их можно будет применить в клинике, подход предлагает практическую схему: измеряя, как быстро и в каком направлении клетки рака адаптируются, врачи в будущем смогут разрабатывать графики лечения, которые не только атакуют опухоль, но и направляют фенотипическое «обучение» клеток в тупики, а не в пути спасения.
Цитирование: Hamis, S., Browning, A.P., Jenner, A.L. et al. Growth rate-driven modelling suggests that phenotypic adaptation drives drug resistance in BRAFV600E-mutant melanoma. Commun Biol 9, 385 (2026). https://doi.org/10.1038/s42003-026-09760-2
Ключевые слова: меланома, лекарственная устойчивость, клеточная пластичность, прерывистая терапия, математическое моделирование