Clear Sky Science · ru
Структурная основа активации нитроксидредуктазы, зависящей от хинола, у Neisseria meningitidis через димеризацию
Как бактерии перехитривают нашу иммунную защиту
Когда вредоносные бактерии проникают в организм, наши иммунные клетки выделяют токсичные молекулы, такие как оксид азота, чтобы убить их. Некоторые патогены, однако, выработали молекулярные уловки, позволяющие нейтрализовать эту атаку и выжить. В этом исследовании подробно показано на атомном уровне, как ключевой бактериальный фермент переориентируется в пары и становится гораздо эффективнее в детоксикации оксида азота, и почему понимание этого изменения формы может открыть новые пути для разработки антибиотиков.
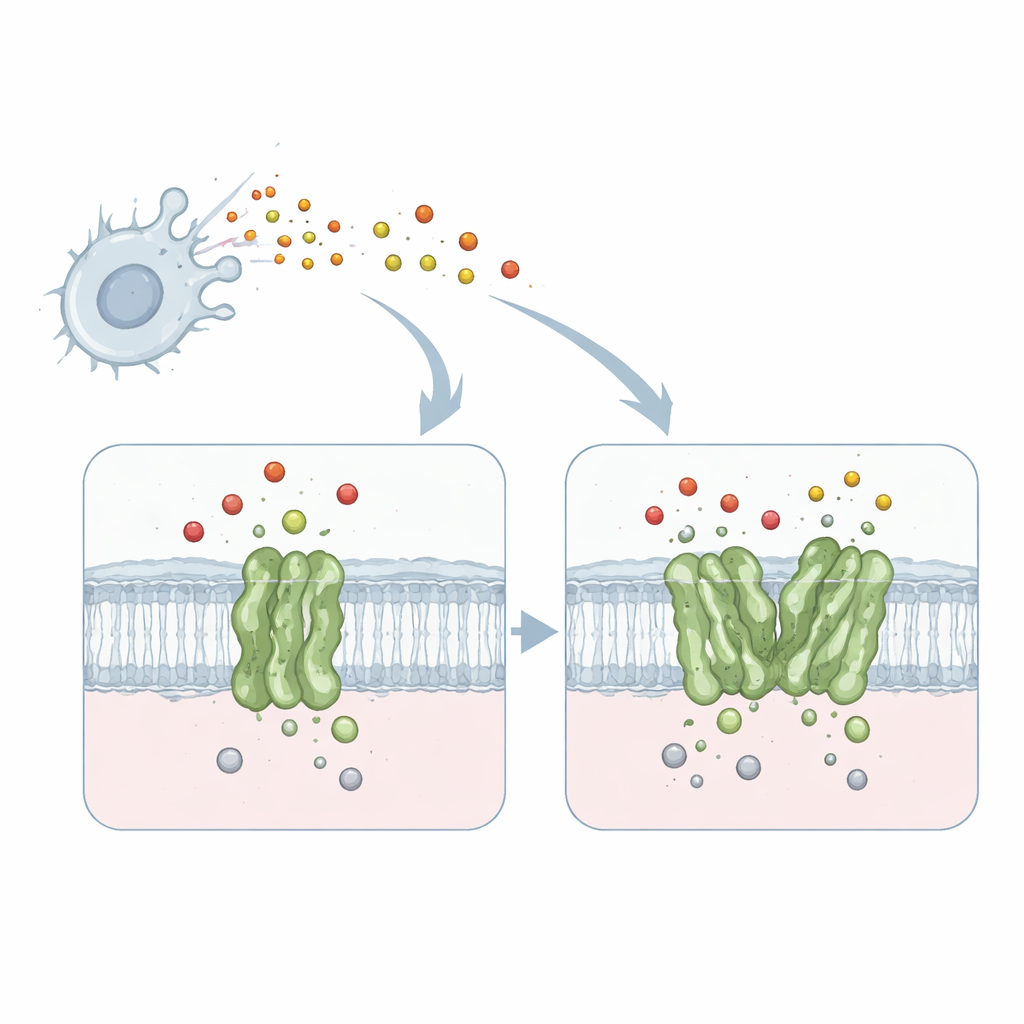
Крошечный механизм, обезвреживающий токсичный газ
Работа сосредоточена на мембранном белке, называемом хинол-зависимой нитроксидредуктазой (qNOR) из менингитной бактерии Neisseria meningitidis. qNOR локализуется в бактериальной клеточной мембране и превращает оксид азота — токсичный газ, производимый нашей иммунной системой — в менее вредные продукты. Эта детоксикация позволяет микроорганизму продолжать дыхание и рост даже в враждебной среде, например внутри человеческих макрофагов. Поскольку дыхание и удаление оксида азота жизненно важны для выживания патогена, qNOR представляет собой привлекательную мишень для новых антимикробных препаратов.
Когда один — хорошо, но два — лучше
Предыдущие биохимические исследования показали, что qNOR может существовать либо как одиночная молекула (мономер), либо как пара (димер), причём димер действует в два-четыре раза быстрее при нейтрализации оксида азота. До сих пор оставалось неясным, почему простое соединение двух копий одного и того же фермента так драматически улучшает его работу. Чтобы ответить на этот вопрос, исследователи использовали высокоразрешающую крио-электронную микроскопию одиночных частиц для получения детальных трехмерных структур как мономерного, так и димерного qNOR от одного и того же штамма бактерии. Они получили изображения почти атомного разрешения — 1,89 Å для димера и 2,25 Å для мономера — достаточно четкие, чтобы определить отдельные боковые цепи аминокислот, ионы металлов и множество молекул воды.
Гибкий спиральный сегмент превращается в стабилизирующую опору
Удивительно, но каталитическое ядро фермента — металлический центр, где происходит превращение оксида азота — оказалось почти идентичным в обеих формах. Ключевые различия проявлялись на некотором удалении, в трансмембранной спирали, названной TM10, и в том, как она контактирует с другой спиралью (TM2) при образовании пары qNOR. В мономере TM10 слабо закреплена и может существенно отклоняться и изгибаться, что выявило компьютерное моделирование данных крио-ЭМ. В димере TM10 от каждого партнёра фиксируется у своего соседа, образуя связку из четырёх спиралей и сильно ограничивая подвижность. Такая стабилизация тонко смещает критическую аминокислоту — глутамат Glu563 — приближая её к другому глутамату (Glu494) рядом с активным центром и формируя более направленный путь для приходящих протонов, необходимых для реакции.
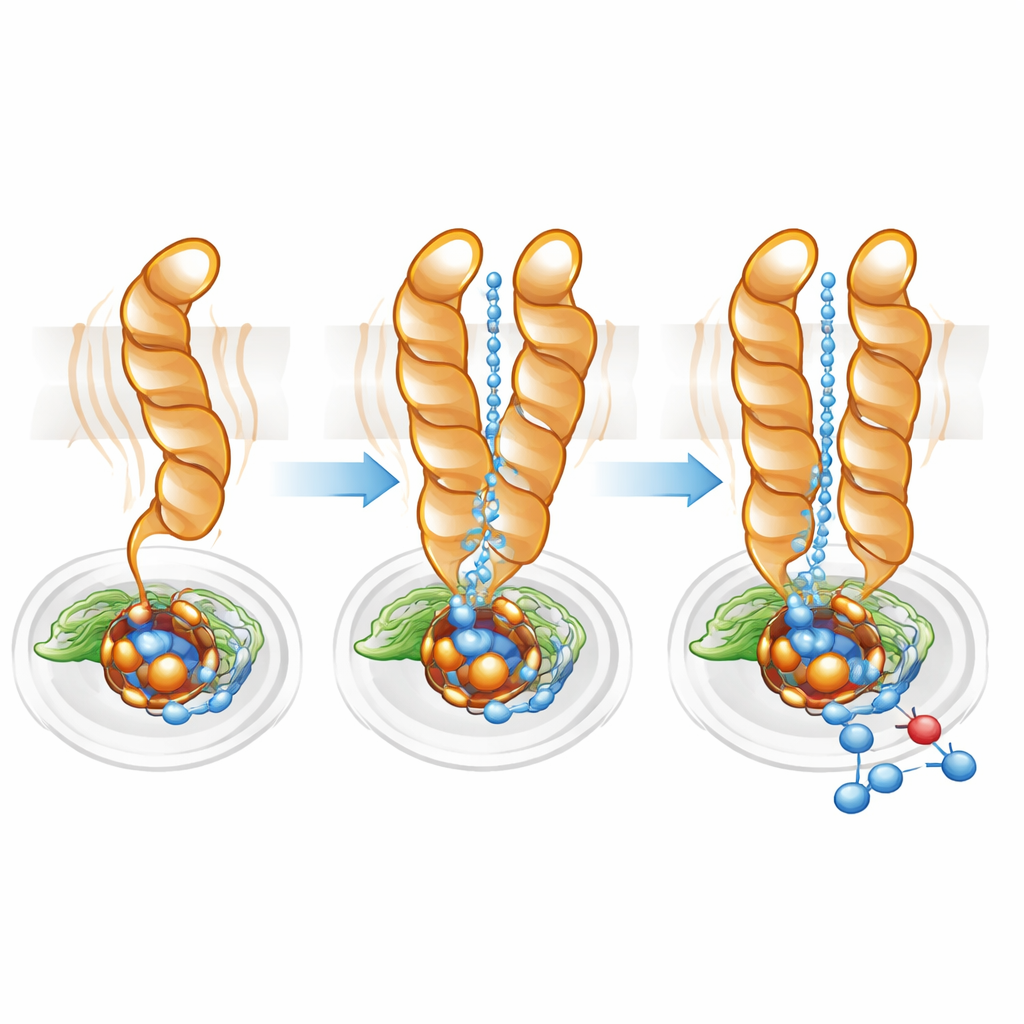
Тонкая настройка протонного шоссе
Протоны — положительно заряженные ионы водорода — должны эффективно доставляться из цитоплазмы к погребённому активному центру, чтобы восстановление оксида азота происходило. С помощью программного картирования путей команда обнаружила гидрофильную полость, соединяющую цитоплазму с активным центром как в мономере, так и в димере. Однако в мономере этот канал был шире и более рассеян, что согласуется с большей подвижностью TM10. В димере фиксированное положение TM10 и благоприятная ориентация Glu563 помогали определить более прямой и лучше организованный путь. Замена Glu563 на аминокислоты, неспособные образовать такие же взаимодействия, сократила активность фермента до менее чем 10% от нормальной и также дестабилизировала димер, тогда как мутации в родственных позициях уменьшали количество незамерзающего железа (non-heme iron) в активном центре. В совокупности эти результаты показывают, что образование димера и точное позиционирование Glu563 и Glu494 тесно связаны как со структурной целостностью, так и с каталитической эффективностью.
От структурных открытий к новым методам лечения
Полученные данные показывают прямую связь между парированием белков на поверхности мембраны и тонкой перестройкой глубоко в активном центре, которая контролирует эффективность удаления оксида азота ферментом qNOR. Проще говоря, когда две копии фермента сцепляются, они выпрямляют и упрочняют гибкий сегмент, который направляет протоны в реакционный центр, повышая выход фермента. Для разработки лекарств это подсказывает нестандартную стратегию: вместо прямой блокировки активного центра можно спроектировать молекулы, которые разъединяют димер или нарушают взаимодействие Glu563–Glu494, заставляя фермент переходить в медленный мономерный формат. Поскольку qNOR и родственные ферменты важны для выживания нескольких опасных, резистентных к лекарствам патогенов, такие структурно-ориентированные подходы могут внести вклад в создание следующего поколения целевых антимикробных средств.
Цитирование: Gopalasingam, C.C., Egami, H., Shigematsu, H. et al. Structural basis of Neisseria meningitidis quinol dependent nitric oxide reductase activation by dimerization. Commun Biol 9, 433 (2026). https://doi.org/10.1038/s42003-026-09754-0
Ключевые слова: детоксикация оксида азота, бактериальное дыхание, мембранные ферменты, криоэлектронная микроскопия, мишени для антимикробных препаратов