Clear Sky Science · ru
Пространственная мультиомика выявляет иммуно‑метаболические особенности воспалительной границы при раке печени после необратимой электропорации
Почему новое лечение рака печени требует пристального внимания
Необратимая электропорация (IRE) — относительно новый метод разрушения опухолей печени с помощью коротких высоковольтных электрических импульсов вместо тепла. Поскольку он может сохранять рядом расположенные кровеносные сосуды и желчные протоки, этот подход особенно полезен для опухолей в деликатных зонах. Тем не менее у трети пациентов опухоль возвращается прямо у границы обработанной области. В этом исследовании выясняют, что происходит в этой узкой пограничной зоне после IRE — и не подготавливают ли скрытые изменения в иммунных клетках и клеточном метаболизме почву для повторного роста рака.
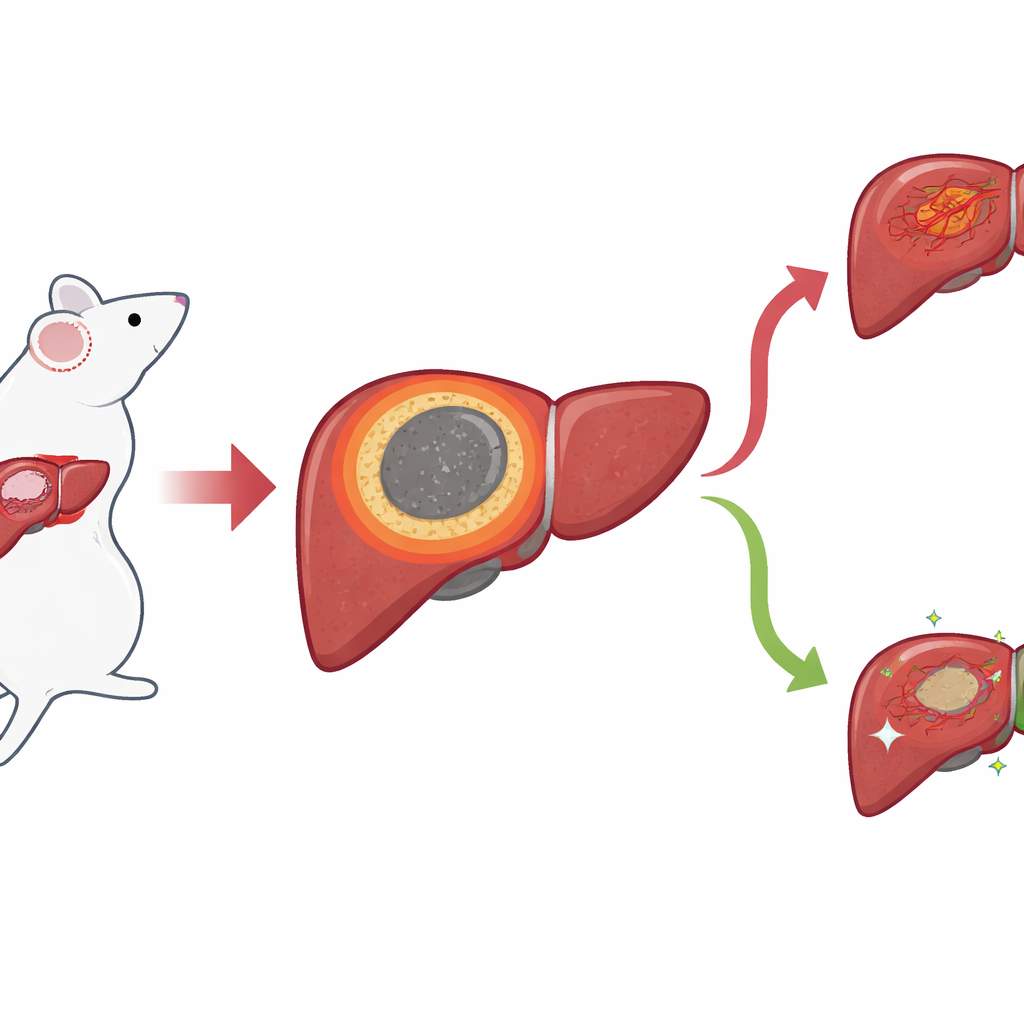
Узкая граница с большими последствиями
Используя модель рака печени у мышей, авторы сосредоточились на тонком кольце ткани, которое формируется между мёртвым, обработанным ядром и окружающей здоровой печенью после IRE. Они называют эту зону воспалительной границей, или IM. Обычная микроскопия показала, что эта область совпадает с местом, где обычно появляются местные рецидивы, но её контуры было трудно провести невооружённым глазом. Чтобы получить более чёткую картину, команда применила «пространственные» методы, позволяющие определить, какие гены и малые молекулы присутствуют, сохраняя при этом их локализацию в ткани. С помощью пространственного транскриптома они картировали активность генов по точкам и обнаружили отдельный кластер точек, точно совпадающий с IM, отделяющий некротический центр от нормальной печени и областей опухоли.
Иммунные клетки собираются — но многие тормозят атаку
Затем учёные использовали одноклеточный и одноядерный РНК‑секвенирование вместе с мощным методом профилирования CyTOF, чтобы каталогизировать отдельные типы клеток по всей печени. Они обнаружили, что IM доминируют макрофаги. В частности, в IM в течение нескольких дней после IRE массово проникал подтип, напоминающий «липид‑ассоциированные макрофаги» (LAM). Эти клетки несут поверхностные маркеры и сигнатуры генов, связанные с иммунным подавлением, включая высокие уровни PD‑L1, молекулы, известной тем, что она ослабляет ответы Т‑клеток. Анализ экспрессии генов указывал, что эти макрофаги хорошо поглощают чужеродный материал, реагируют на химические сигналы‑аттрактанты и посылают молекулярные сигналы, способные сдерживать те самые Т‑клетки, необходимые для уничтожения раковых клеток. Визуализация подтвердила, что макрофагов с PD‑L1 в IM значительно больше, чем в прилежащей нормальной ткани.
Очаг изменённой липидной химии
Далее команда сопоставила эту иммунную карту с пространственной метаболомикой — методом масс‑спектрометрической визуализации, отображающим распределение сотен малых молекул. Они показали, что IM имеет метаболический отпечаток, отличающийся от мёртвого центра и окружающей печени. В этой узкой полосе многие липидные пути были значительно усилены, включая синтез ненасыщенных жирных кислот, производные арахидоновой кислоты и сфинголипиды. Ключевые сигнальные липиды, такие как простагландины и лейкотриены, происходящие от арахидоновой кислоты, были обогащены в IM, в то время как другие ферментативные маршруты переработки той же молекулы были относительно приглушены. Другая группа липидов — сфинголипиды, включая церамиды и сфингомиелины — также накапливалась, что сопровождалось повышенной экспрессией ферментов, синтезирующих и перестраивающих эти молекулы.
Пошаговый сдвиг от повреждения к нише, богатой топливом
Разделив воспалительную границу на три тонких слоя от некротического центра наружу, исследователи увидели постепенный сдвиг в химии. Ближе всего к зоне некроза были наибольшие уровни сложных липидов и молекул, связанных с холестерином, тогда как дальше наружу повышались уровни малых энергетических молекул, таких как глюкоза и отдельные аминокислоты. Эта картина указывает на то, что на коротком расстоянии ткань переходит от богато насыщенной липидами, сигнально‑обогащённой среды к более ориентированной на обеспечение энергии и материалов для выживания и роста клеток. Авторы предполагают, что такое пошаговое перепрограммирование помогает поддерживать липидно‑чувствительных, иммуносупрессивных макрофагов, доминирующих в IM, и может тихо подготавливать почву для повторного закрепления опухолевых клеток.
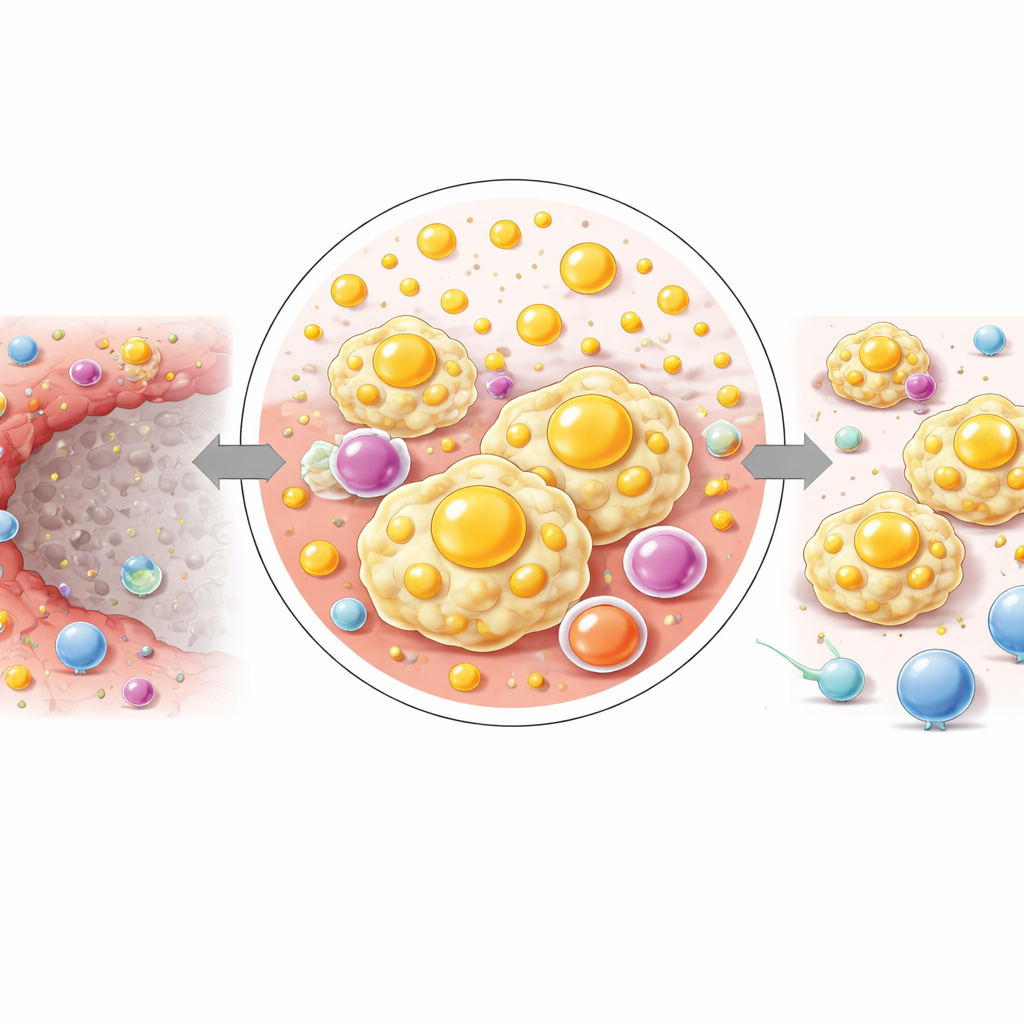
Что это значит для ухода за больными раком печени в будущем
Проще говоря, эта работа показывает, что IRE делает больше, чем просто убивает опухолевые клетки: он создаёт узкое кольцо ткани, где иммунные клетки и липидная химия вместе формируют защищённую, благоприятную для опухоли среду. Макрофаги в этой зоне многочисленны, богаты липидами и склонны выключать Т‑клетки, а не помогать им. Поскольку эти изменения тесно связаны с конкретными метаболическими путями, они указывают новые подходы к терапии. Комбинация IRE с препаратами, таргетирующими липидный метаболизм или блокирующими PD‑L1 в этой границе, теоретически может превратить склонную к рецидиву зону в место, где опухоль действительно окончательно уничтожается.
Цитирование: Liu, J., Guan, S., Sun, Z. et al. Spatial multiomics reveals irreversible electroporation-induced immuno-metabolic characteristics of the inflammatory margin in liver cancer. Commun Biol 9, 458 (2026). https://doi.org/10.1038/s42003-026-09742-4
Ключевые слова: рак печени, аблация опухоли, иммунная микросреда, макрофаги, метаболизм липидов