Clear Sky Science · ru
Поверхностная «декорация» бактерий создаёт надёжные живые терапевтические средства для улучшения лечения язвенного колита
Превращая дружелюбные микробы в крошечных телохранителей
Язвенный колит — болезненное заболевание кишечника, при котором собственные ткани кишечника постоянно воспаляются, что приводит к неотложной диарее, кровотечениям и существенному снижению качества жизни. Врачи и пациенты воодушевлены идеей «хороших бактерий» в виде капсул, которые могли бы успокаивать воспаление изнутри, но большинство этих микроорганизмов погибают в суровом пути через желудок и тонкую кишку, так и не достигнув толстой кишки, где они наиболее необходимы. В этом исследовании описан новый способ «одеть» пробиотические бактерии в защитную оболочку, чтобы они могли безопасно пройти через пищеварительный тракт, обосноваться в толстой кишке и помочь восстановить повреждённый кишечник.
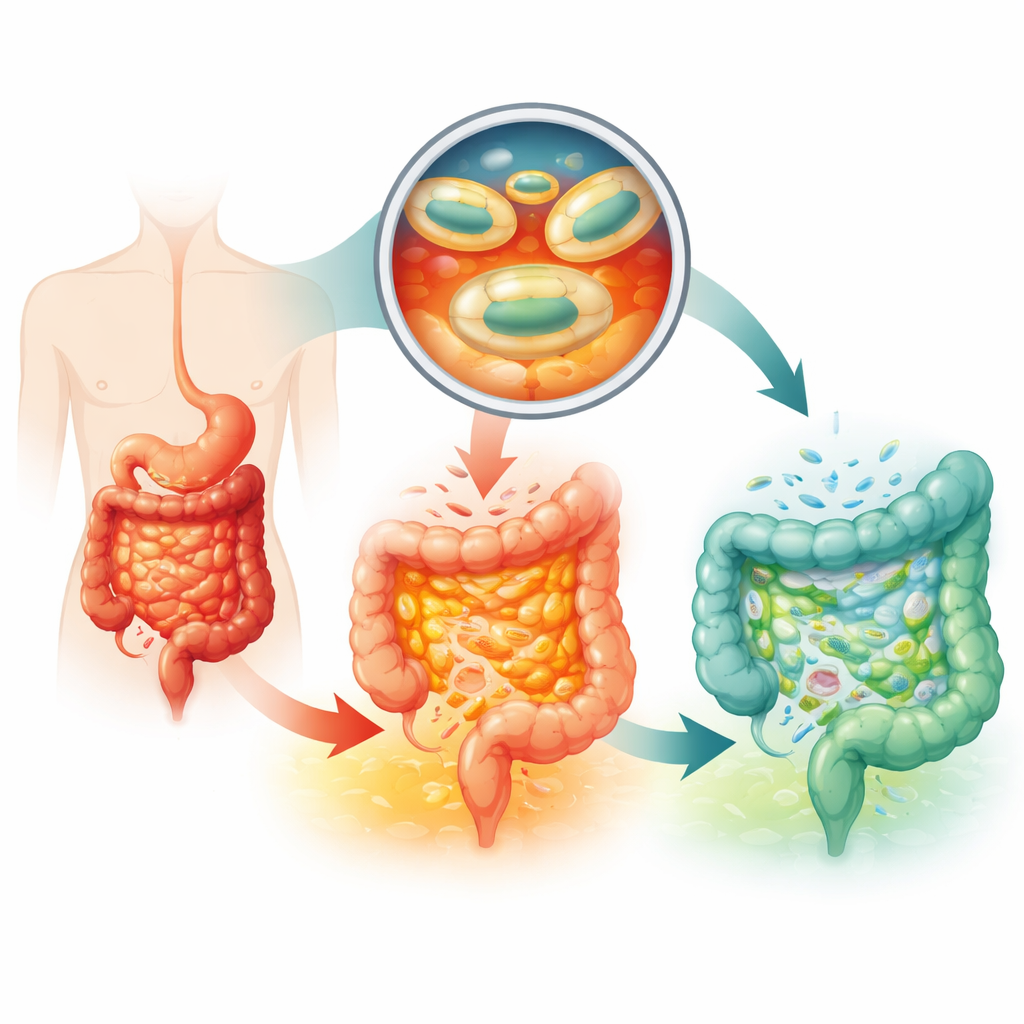
Почему нынешние пробиотические препараты часто не оправдывают ожиданий
Стандартные методы лечения язвенного колита опираются на противовоспалительные и иммуносупрессорные препараты, которые могут иметь серьёзные побочные эффекты и не работают для всех пациентов. Пробиотики предлагают более мягкий подход, помогая восстановить баланс микробного сообщества кишечника. Особая штамм Escherichia coli Nissle 1917 уже одобрен как лекарство для этого заболевания, но пациентам приходится принимать чрезвычайно большие дозы ежедневно, и даже в таком случае эффект невелик. Ключевая проблема — выживание и доставка: кислотность желудка, пищеварительные ферменты и быстрое продвижение по верхним отделам кишечника убивают или смывают большинство бактерий до того, как они смогут прикрепиться и размножиться в толстой кишке, где обычно обитает более 99% микробов кишечника.
Создание защитной оболочки вокруг полезных бактерий
Чтобы решить эту проблему, исследователи разработали тонкое «умное» покрытие вокруг каждой пробиотической клетки, использовав растительное вещество лигнин. Они химически модифицировали лигнин, чтобы повысить его растворимость и чувствительность к изменениям кислотности, получив материал, который остаётся стабильным в сильной кислоте, но распадается в более нейтральной среде толстой кишки. С помощью щадящего послойного метода сначала нанесли ионы кальция на поверхность пробиотика, а затем обернули его модифицированным лигнином, сформировав гладкую «броню» толщиной примерно одну десятитысячную миллиметра. Микроскопия и измерения размера частиц показали, что эта защита не убивает бактерии, а такой же метод сработал для нескольких очень разных видов бактерий, что указывает на возможность использования платформы для множества пробиотических терапий.
Целевое попадание в толстую кишку и помощь её заживлению
При испытаниях в моделируемых пищеварительных жидкостях незащищённые бактерии быстро разрушались под действием желудочной кислоты, тогда как «в броне» бактерии оставались живыми часами и эффективно высвобождали своё содержимое только при уровнях pH, характерных для толстой кишки. У мышей с химически вызванным язвенным колитом покрытые бактерии значительно накапливались в толстой кишке, тогда как непокрытые бактерии или простые смеси с материалом покрытия в основном не справлялись с этой задачей. Команда с помощью флуоресцентной визуализации, генетических тестов и математического моделирования показала, что защищённые бактерии не только доезжают до толстой кишки целыми, но и там размножаются, составляя примерно одну тысячную часть всех микробов кишечника. Лечёные мыши теряли меньше веса, сохраняли более длинную толстую кишку и имели гораздо более здоровую ткань кишечника при микроскопическом исследовании — с более плотными межклеточными контактами и восстановленным слоем слизи, которые вместе образуют важный барьер между организмом и содержимым кишечника.
Успокоение иммунной системы и восстановление микробиома
Кроме физического ремонта, «в броне» пробиотики изменяли иммунный и микробный ландшафт нездорового кишечника. В крови и толстой кишке больных мышей уровни провоспалительных молекул были высоки, а уровень ключевого противовоспалительного сигнала низок; новое лечение обращало эти тенденции, сдвигая иммунную систему в более спокойное состояние. Детализированные клеточные анализы показали изменения в составе иммунных клеток как в толстой кишке, так и в селезёнке. Одновременно секвенирование ДНК микробов кишечника выявило, что терапия увеличивала общую микробную разнообразность и усиливала присутствие нескольких групп бактерий, связанных со здоровьем кишечника, включая Akkermansia и Muribaculum. Профилирование метаболитов также продемонстрировало широкие изменения в малых молекулах, связанных с метаболизмом витаминов, жирных кислот и аминокислот, что указывает на то, что восстановленный микробиом создаёт химическую среду, более благоприятную для заживления.
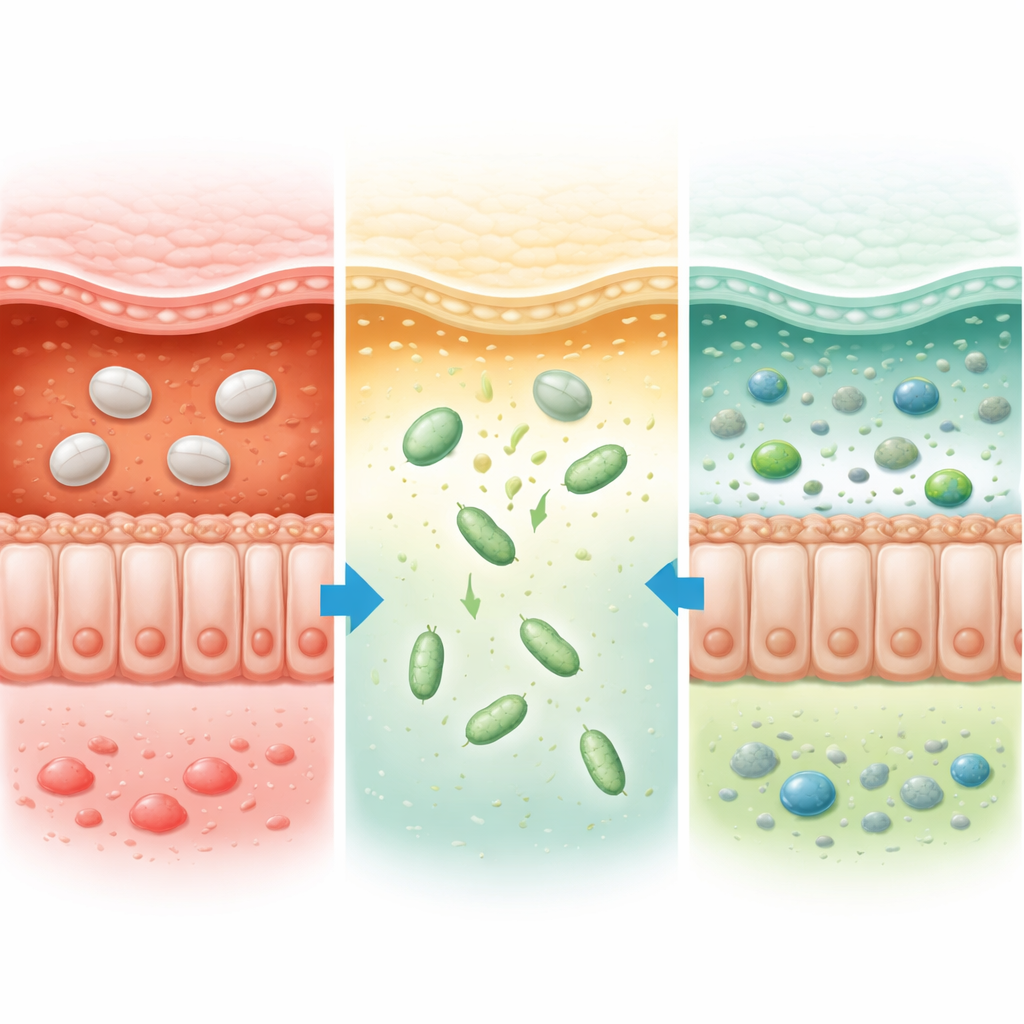
От мышиной модели к будущим живым лекарствам
В целом проделанная работа показывает, что придание пробиотикам рН‑чувствительной «бронёй» позволяет надёжно провести их через пищеварительный лабиринт и доставить в те районы толстой кишки, где язвенный колит причиняет наибольший ущерб. У мышей эта стратегия позволила гораздо меньшим дозам бактерий колонизировать толстую кишку, восстановить её барьер, снизить вредное воспаление и вернуть более здоровое микробное сообщество и метаболический профиль. Поскольку растительное покрытие в основном проходит через организм без значительных изменений и метод применим к многим типам бактерий, авторы полагают, что их подход представляет собой широко полезный план для разработки следующего поколения «живых» лекарственных средств для лечения язвенного колита и других заболеваний толстой кишки.
Цитирование: Liu, J., Fang, Z., Li, X. et al. Surface decoration of bacteria generates robust living therapeutics for improved ulcerative colitis therapy. Commun Biol 9, 428 (2026). https://doi.org/10.1038/s42003-026-09732-6
Ключевые слова: язвенный колит, пробиотики, микробиом кишечника, доставка лекарств, кишечный барьер