Clear Sky Science · ru
Активаторы NRF2 и ингибитор ядерного экспорта селинексор ограничивают коронавирусы, нацеливаясь на сеть, включающую ACE2, TMPRSS2 и XPO1, через механизм, независимый от NRF2
Препараты, которые помогают клеткам говорить «нет» коронавирусам
Большинство современных препаратов против коронавирусов нацелены на сам вирус. Но вирусы мастера изменчивости, и новые варианты быстро ослабляют эффективность таких лекарств. В этом исследовании изучается другой подход: сделать собственные клетки менее гостеприимными для как опасных коронавирусов, таких как SARS-CoV-2, так и для более мягких сезонных штаммов. Манипулируя тем, как клетки управляют несколькими ключевыми белками‑«привратниками», исследователи показали, что существующие малые молекулы могут резко снизить заражение в лабораторных моделях, и при этом действуют они не через тот антивирусный путь, которым они прославились.
Новый ракурс в защите от коронавирусов
Команда сосредоточилась на соединениях, известных как активаторы клеточной защитной программы, контролируемой белком NRF2. Эти соединения — 4‑октил итаконат (4OI), бардоксалон (BARD) и сульфорафан (SFN) — были протестированы рядом с селинексором (SEL), препаратом, блокирующим транспортный белок XPO1, который помогает выносить другие белки из ядра клетки. В моделях легочных и почечных клеток все четыре препарата снижали уровни SARS‑CoV‑2 без вреда для клеток. Они также оказались эффективными против нескольких вариантов, вызывающих обеспокоенность. Удивительно, но при генетическом удалении NRF2 вирусы реплицировались даже лучше, что доказывает природную защитную роль NRF2 — однако препараты по‑прежнему работали хорошо, показывая, что их антивирусная сила опирается на другой путь. 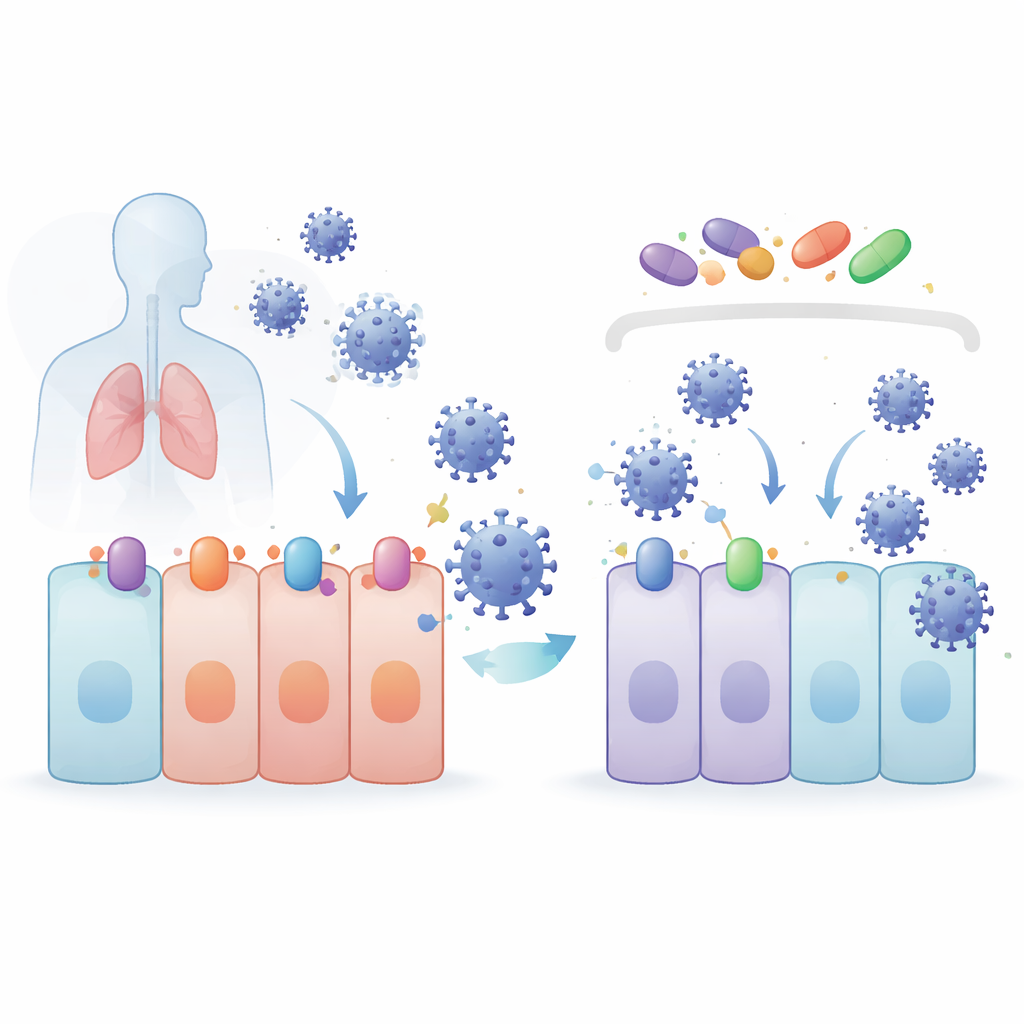
Закрытие вирусной входной двери
Коронавирусы начинают инфекцию, прикрепляясь к рецепторным белкам на поверхности клетки. Для SARS‑CoV‑2 и близких ему вирусов главная «дверь» — ACE2, с участием режущего фермента TMPRSS2. Экспортный белок XPO1 также, по‑видимому, содействует инфекции. Исследователи обнаружили, что 4OI, BARD, SFN и SEL все снижали количество ACE2, TMPRSS2 и XPO1 в человеческих легочных клетках. 4OI и SEL были особенно эффективны при применении до заражения, и они блокировали проникновение частиц, подобным вирусам, покрытых спайковыми белками коронавируса. Иными словами, эти препараты не просто замедляют вирус после попадания в клетку — они помогают убрать замки и ручки, которые вирусу нужны, чтобы открыть дверь с самого начала.
Как клетки разбирают ключевые подсобные белки вируса
Глубже изучая механизм, команда показала, что 4OI ускоряет разрушение белка ACE2. При нормальных условиях ACE2 сохраняется в течение многих часов; при добавлении 4OI он исчезал с поверхности клетки за долю этого времени. Это разрушение требовало двух клеточных «маркировщиков», NEDD4L и MDM2, которые прикрепляют молекулярные «уничтожьте меня» метки к белкам. Блокирование этих маркировщиков ослабляло способность 4OI устранять ACE2. Удивительно, что обычная система протеасомного расщепления не была главным путем. Вместо этого ACE2 направлялся в систему переработки и утилизации клетки — лизосому. Препараты также снижали активность экспрессии генов ACE2 и XPO1, отчасти через уменьшение активации STAT3 — белка, который обычно усиливает чтение гена ACE2. 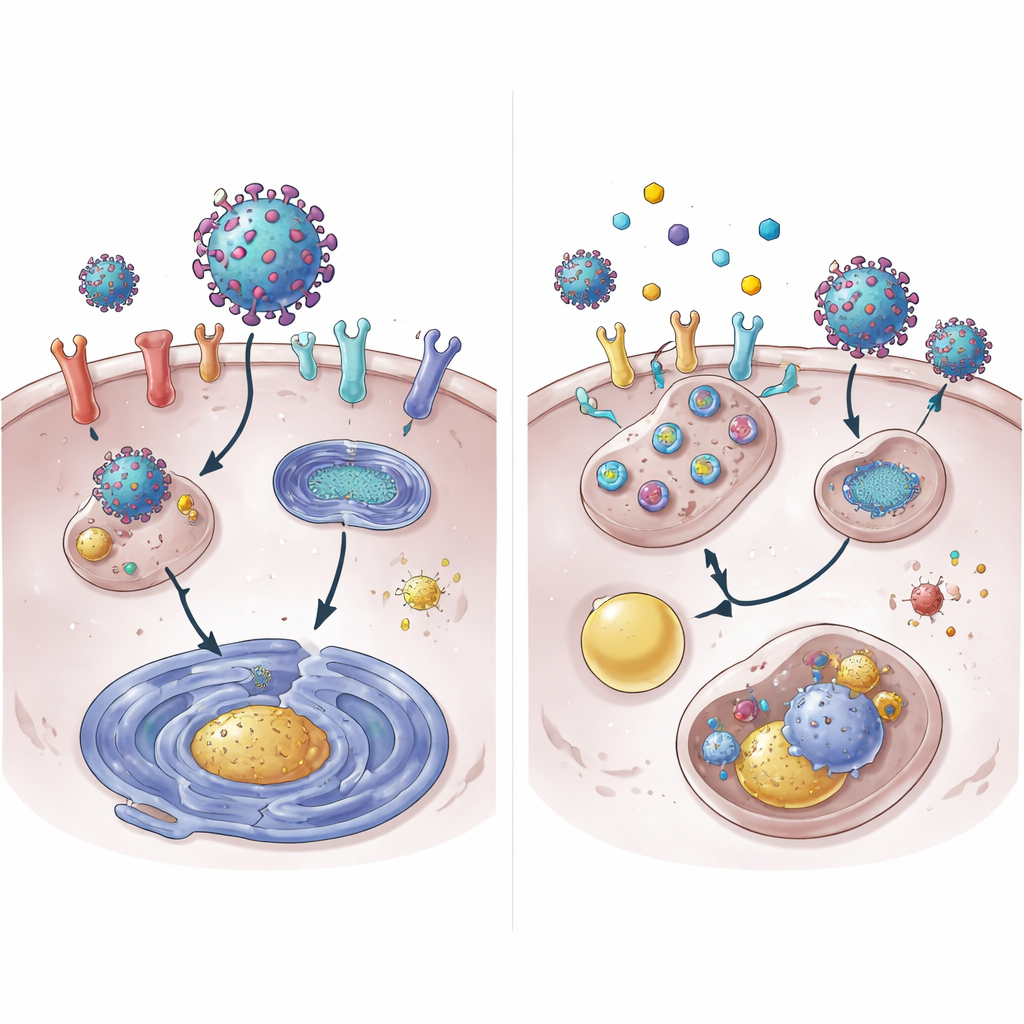
Сезонные коронавирусы и связь с XPO1
Далее учёные обратились к hCoV‑229E, сезонному коронавирусу, вызывающему обычные простуды, но потенциально опасному для людей с ослабленным иммунитетом. Используя генетически модифицированные вирусы, которые светятся при репликации, они показали, что все четыре соединения сильно подавляют 229E в легочных и сосудистых клетках, даже при отсутствии NRF2. В отличие от SARS‑CoV‑2, этот вирус использует другой рецептор, ANPEP, который препараты не меняли. Вместо этого их эффект тесно коррелировал со способностью снижать XPO1. Понижение уровня XPO1 само по себе резко уменьшало репликацию 229E, а эффект селинексора почти исчезал в клетках с низким XPO1. Это соотношение — SEL наиболее зависим от XPO1, BARD наименее — указывает на то, что у каждого соединения немного разный набор целей, при этом XPO1 является центральным узлом для многих их антивирусных действий.
Что это может значить для будущих терапий
Для неспециалистов главное послание в том, что бороться с коронавирусами можно не только, атакуя сам вирус, но и мягко перенастроив наши собственные клетки так, чтобы они были менее восприимчивы к инфекции. В культурированных человеческих клетках изученные соединения устраняли ключевые сайты прикрепления и вспомогательные пути, на которых зависят SARS‑CoV‑2 и вирус обычной простуды, и делали это во многом без участия того самого пути NRF2, из‑за которого их впервые заинтересовались. Хотя эти результаты пока доклинические и не переводятся напрямую в лекарства, они подчеркивают перспективный путь: препараты, которые одновременно снижают вход вируса, ослабляют вредное воспаление и защищают ткани, нацеливаясь на общую сеть белков хозяина, таких как ACE2, TMPRSS2 и XPO1.
Цитирование: Waqas, F.H., Silva da Costa, L., Zapatero-Belinchón, F.J. et al. NRF2 activators and the inhibitor of nuclear export, selinexor, restrict coronaviruses by targeting a network involving ACE2, TMPRSS2, and XPO1 through an NRF2-independent mechanism. Commun Biol 9, 384 (2026). https://doi.org/10.1038/s42003-026-09724-6
Ключевые слова: антивирусы, направленные на хозяина, вход коронавируса, ACE2 и TMPRSS2, активаторы NRF2, ингибирование XPO1