Clear Sky Science · ru
Двухэтапная актин‑опосредованная стратегия позволяет Campylobacter jejuni вызывать агрегацию митохондрий и регулировать гомеостаз железа для внутриклеточного выживания и персистенции
Почему эта крошечная борьба внутри клеток важна
Пищевое отравление из‑за недоваренной курицы часто связывают с бактерией Campylobacter jejuni. Большинство людей выздоравливают, но этот микроорганизм удивительно хорошо приспосабливается к самым разным условиям, что облегчает его распространение от фермы до стола. В исследовании рассматривают, что происходит, когда бактерия прячется внутри свободноживущей амёбы — обычного микроба пресной воды — и обнаруживают неожиданно изощрённый приём выживания, который сводится к перестройке внутреннего каркаса клетки, сгруппированию энергетических «электростанций» — митохондрий, и контролю за железом и реактивными формами кислорода. Понимание этой скрытой фазы жизненного цикла может указать на новые способы сокращения загрязнений ещё до того, как бактерия попадёт к людям.
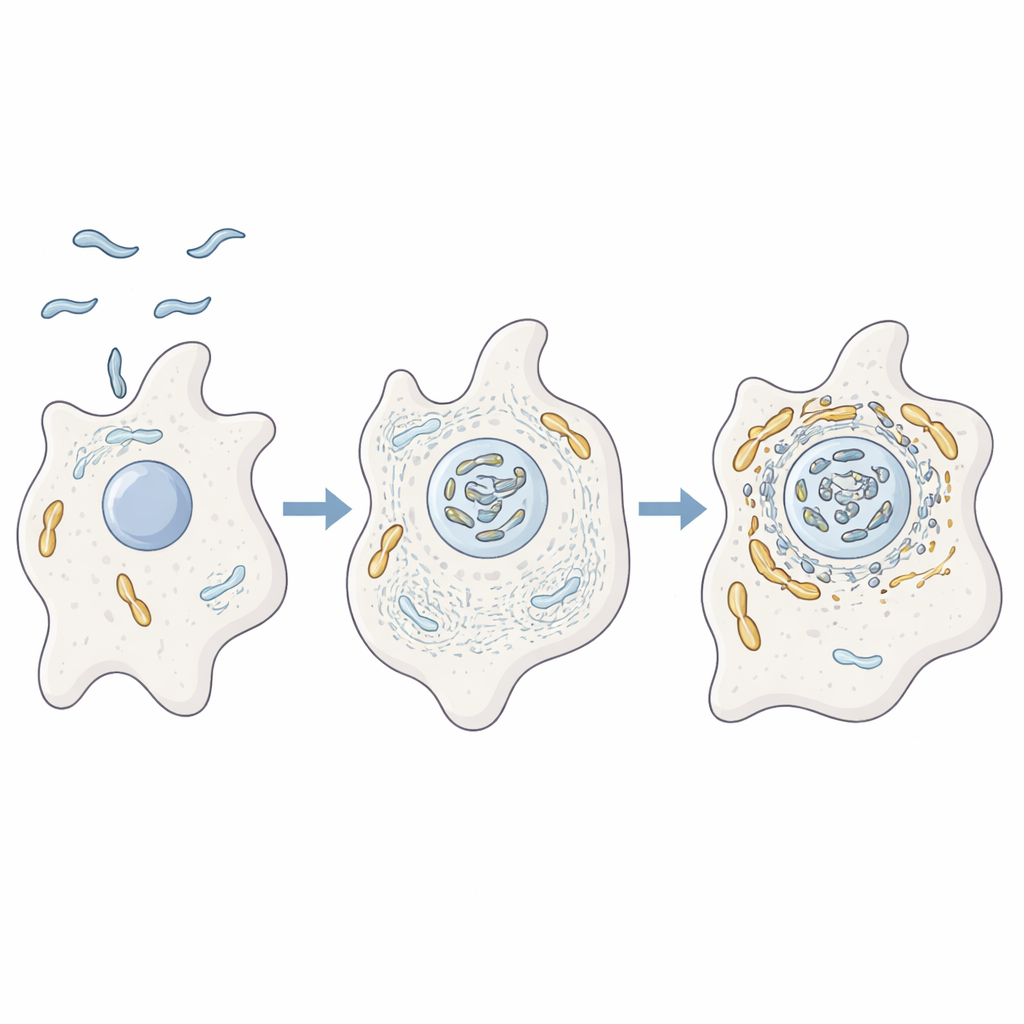
Микроб, тренирующийся внутри амёб
Авторы изучали поведение C. jejuni внутри амёбы Acanthamoeba castellanii, одноклеточного организма, обитающего в почве и воде. Эти амёбы служат тренировочными площадками для многих патогенных бактерий, обеспечивая защиту от неблагоприятных условий и дезинфектантов. С помощью продвинутого анализа белков, микроскопии и генетических мутантов исследователи показали, что при инфицировании амёб C. jejuni оказывается в тесной ассоциации с митохондриями хозяина. Одновременно вокруг этих митохондрий заметно обогащение актинового каркаса клетки и белков, регулирующих форму и подвижность, что наводит на мысль, что бактерия активно перестраивает внутреннюю архитектуру клетки хозяина.
Искривление клеточного скелета для перемещения «электростанций»
Чтобы проверить, действительно ли актин управляет этим взаимодействием, команда блокировала формирование актиновых филаментов и их разветвление в сети. При таких условиях митохондрии переставали собираться возле бактерий и оставались разбросанными точками, а выживание бактерий снижалось. Затем исследователи сосредоточились на двух бактериальных вспомогательных белках, CiaD и CiaI, которые вводятся в клетки хозяина через жгутик бактерии — хлестовидный хвост. Оказалось, что CiaD усиливает рост актиновых нитей и способствует образованию шиповидных выступов на поверхности амёбы, помогая клетке захватывать бактерии. После проникновения внутрь митохондрии наблюдали в виде скоплений вокруг везикулы с бактериями в актинозависимом режиме, помещая бактерию в привилегированную зону, богатую энергетическими компонентами хозяина.
Молекулярный переключатель, перестраивающий митохондрии
Если CiaD важен для проникновения, то CiaI контролирует последующие события. При удалении гена CiaI C. jejuni переставала вызывать выраженную агрегацию митохондрий и плохо выживала внутри амёб. Добавление очищенного CiaI, прикреплённого к крошечным шарикам, без живых бактерий было достаточным, чтобы вызвать слияние и кластеризацию близлежащих митохондрий и локальное истощение актина. Биохимические тесты показали, что CiaI кооперативно связывает молекулы, несущие энергию, действуя подобно молекулярному переключателю, который может включаться или выключаться в зависимости от условий внутри хозяина. Авторы предполагают, что после индуцированного CiaD роста актина, сближающего митохондрии, CiaI запускает локальное разрушение актина и перестраивает митохондриальную сеть в плотные агрегаты, окружающие компартмент с бактерией.
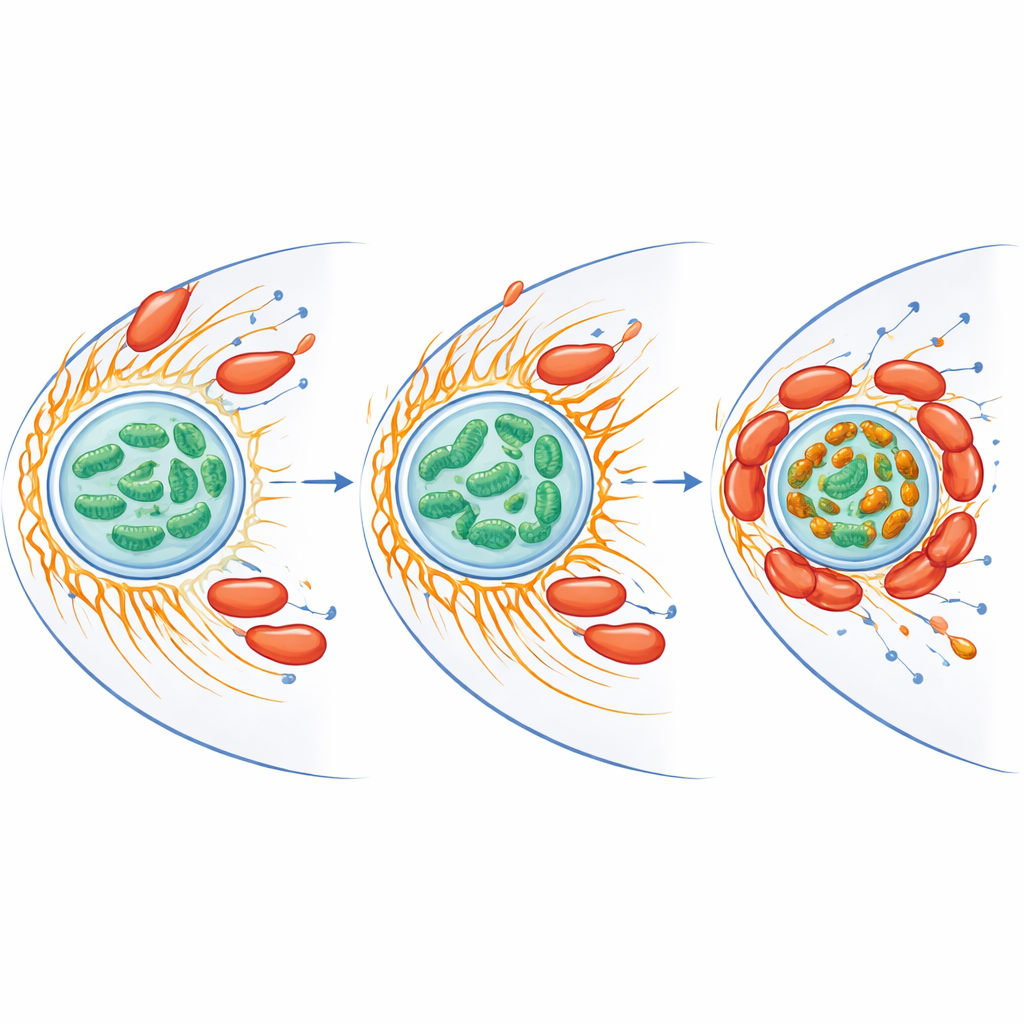
Перенацеливание железа и стресс‑реакций внутри клетки хозяина
Митохондрии выполняют не только энергетические функции — они также управляют запасами железа и производят реактивные формы кислорода, химически агрессивные виды кислорода, которые могут уничтожать микробов. Исследователи обнаружили, что при инфекции общий уровень свободного железа в митохондриях снижался, но одновременно появлялись яркие железосодержащие кластеры там, где митохондрии агрегировались вокруг бактерий. Белки, участвующие в обращении с железом и защите от окислительного стресса, повышались как в клетке хозяина, так и в бактерии. Когда команда удаляла свободное железо хелатирующим соединением, всплеск реактивных форм кислорода у амёбы снижался, а выживаемость C. jejuni существенно возрастала. Митохондрии в инфицированных клетках также демонстрировали повышенный мембранный потенциал, признак усиленной активности, что указывает на то, что бактерия подталкивает энергетические «электростанции» хозяина в состояние, благоприятное для её персистенции, одновременно ограничивая вредную кислородную химию.
Что это значит для безопасности пищевых продуктов и инфекций
В совокупности результаты подтверждают двухэтапную стратегию: сначала CiaD стимулирует рост актина, помогая бактерии проникнуть в амёбу и притянуть митохондрии к месту входа; затем CiaI локально разрушает актин и перестраивает митохондрии в богатые железом кластеры, окружающие мембранный компартмент с бактерией, одновременно притупляя окислительную защиту хозяина. Эта тонко настроенная координация формы клетки, использования энергии и металлообмена помогает C. jejuni выживать внутри амёб и, вероятно, способствует её способности сохраняться в окружающей среде и позднее инфицировать людей. Выявление ключевых участников этой микроскопической борьбы указывает на новые мишени — такие как белки Cia, контакты актин–митохондрии или пути обращения с железом — которые можно было бы нарушить для снижения загрязнений и заболеваемости.
Цитирование: Nasher, F., Wren, B.W. A two-step actin-mediated strategy enables Campylobacter jejuni to promote mitochondrial aggregation and iron homeostasis, for intracellular survival and persistence. Commun Biol 9, 431 (2026). https://doi.org/10.1038/s42003-026-09713-9
Ключевые слова: Campylobacter, амёбы, митохондрии, актиновый цитоскелет, гомеостаз железа