Clear Sky Science · ru
Многослойная регуляция каинатных рецепторов GluK3 опосредована субъединицами Neto и цинком
Почему важны крошечные переключатели мозга
Каждая мысль, воспоминание и настроение в мозге зависят от микроскопических переключателей, которые пропускают заряженные частицы внутрь и наружу нейронов. В этом исследовании рассматривается один такой переключатель — малоизвестный рецептор GluK3. Раскрывая, как вспомогательные белки и ионы цинка тонко настраивают поведение GluK3, работа даёт подсказки о том, как нейронные цепи сохраняют баланс — и как этот баланс может нарушаться при таких расстройствах, как эпилепсия, депрессия и шизофрения.
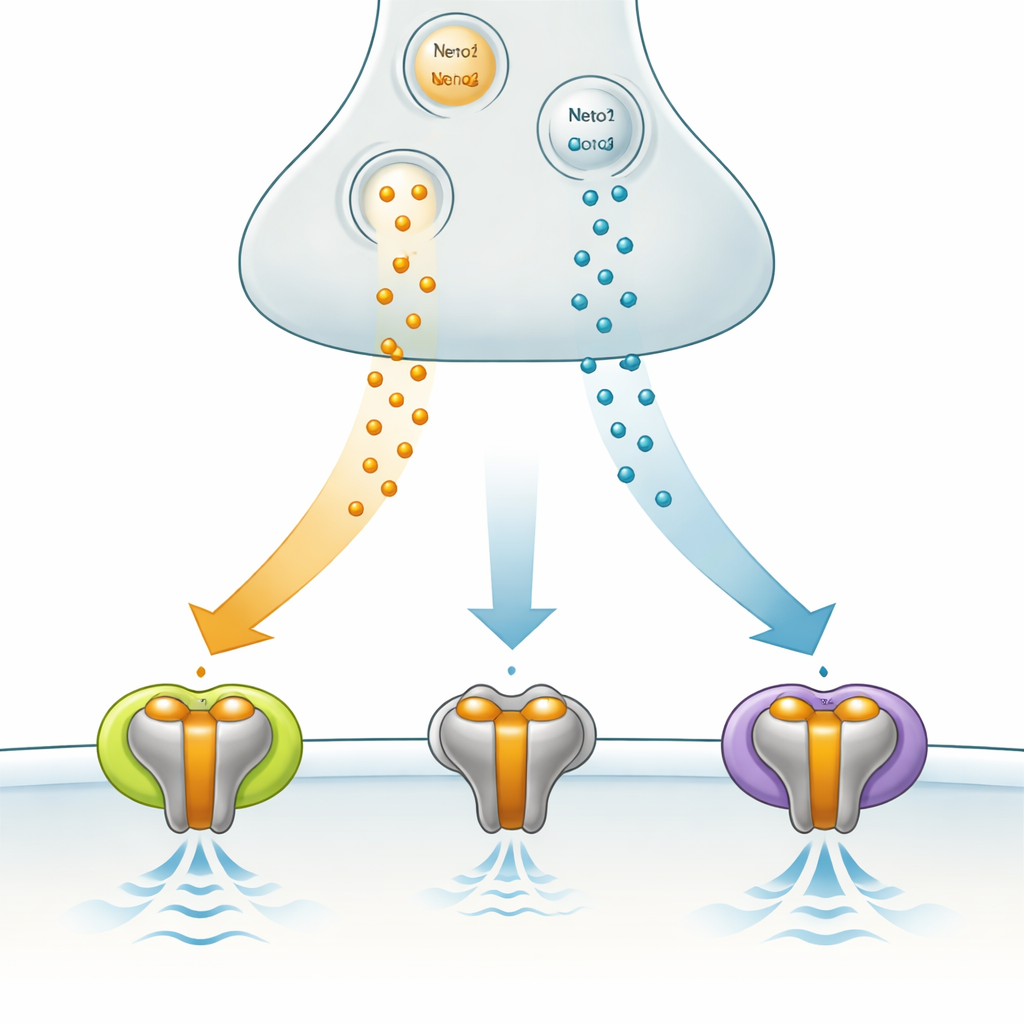
Специализированный сигналовый затвор в мозге
GluK3 принадлежит к семейству каинатных рецепторов, которое входит в более широкую группу глутаматных рецепторов, опосредующих быструю связь между нейронами. В отличие от некоторых своих «собратьев», GluK3 не просто включает или выключает сигнал; он скорее действует как фильтр, лучше всего реагирующий на короткие сильные всплески химического посланца глутамата. Он обогащён в таких областях мозга, как гиппокамп, который имеет ключевое значение для памяти и формирования ритмов сети, и изменения в функции GluK3 связывают с тревожным поведением. Эти особенности делают GluK3 перспективной, но ещё малоизученной мишенью для модуляции активности мозга в норме и при заболеваниях.
Вспомогательные белки, держащие нити
Авторы изучали, как два вспомогательных белка, Neto1 и Neto2, меняют поведение GluK3 в человеческих клетках, генетически настроенных на синтез этих компонентов. Оба белка замедляли, насколько быстро GluK3 закрывается после активации, и оба уменьшали естественную форму внутриклеточной блокировки, которая обычно ограничивает ток. Однако они оказывали противоположное влияние на скорость восстановлению рецептора. В присутствии Neto1 рецепторы быстро восстанавливались и были готовы отвечать на быстрые повторяющиеся сигналы. С Neto2 восстановление становилось значительно медленнее, что способствовало интеграции сигналов на более длинных интервалах. По сути, выбирая разные вспомогательные белки, синапс может решать, будет ли GluK3 вести себя как детектор быстрой стрельбы или как более медленный усредняющий сенсор.
Цинк как второй уровень контроля
Многие терминали, выделяющие глутамат, также выделяют цинк, который может связываться с рецепторами и изменять их работу. Предыдущие работы показали, что цинк необычно усиливает активность GluK3, тогда как для других типов рецепторов он чаще действует угнетающе. Здесь авторы обнаружили, что это усиление сильно зависит от того, какой белок Neto присутствует. Когда GluK3 действует в одиночку, цинк примерно удваивает время, в течение которого рецептор остаётся активным, и умеренно увеличивает ток. Добавление Neto1 притупляет этот эффект. Напротив, в сочетании с Neto2 цинк и Neto2 совместно сильно усиливают ток, гораздо больше, чем каждый по отдельности. Это указывает на то, что синапсы, богатые Neto2 и цинком, могут значительно усиливать сигналы, опосредованные GluK3, при интенсивной активности, тогда как синапсы с преобладанием Neto1 остаются более сдержанными.
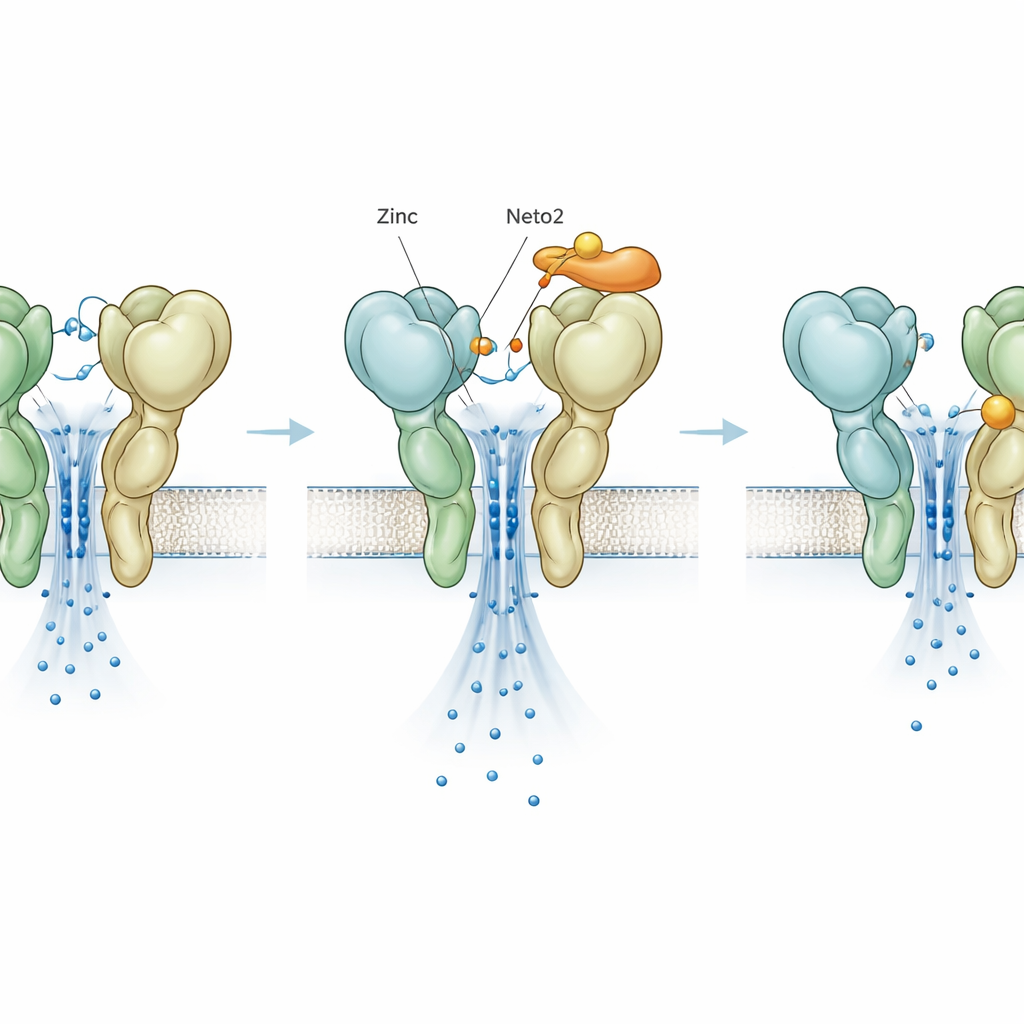
Скрытый тормоз, выявленный мутацией
Чтобы отделить действия цинка от влияния вспомогательных белков, исследователи внесли в GluK3 замену одной аминокислоты, названную D759G, которая удаляет известное место связывания цинка. Как и ожидалось, сама по себе эта мутация делала рецептор более стабильным и медленнее закрывающимся, имитируя обычный эффект цинка. Удивительно, но при добавлении цинка к этому мутанту он больше не усиливал активность; напротив, он ускорял закрытие и снижал ток, выявляя второе, ранее скрытое место связывания цинка, которое действует как тормоз. Neto1 и Neto2 по-прежнему проявляли свои характерные эффекты на мутанте, показывая, что их основное влияние не зависит от исходного места связывания цинка. Тем не менее даже это вновь обнаруженное ингибирующее действие цинка по‑разному настраивалось двумя помощниками, добавляя ещё одну регулируемую «ручку» в систему.
Структура, объясняющая поведение
Чтобы связать функцию с формой, команда использовала криоэлектронную микроскопию для визуализации мутантного рецептора GluK3, замороженного в неактивном состоянии. Снимки показали, что область, связывающая глутамат, образует более компактный, плотно упакованный модуль в мутанте D759G по сравнению с нормальным GluK3. Это структурное уплотнение, вероятно, затрудняет переход рецептора в форму, закрывающую канал, что объясняет, почему мутант, как и GluK3, связанный с цинком, остаётся активным дольше. В то же время изображения показали, что не все части рецептора зафиксированы в одном положении, указывая на по своей сути гибкую архитектуру, особенно чувствительную к небольшим химическим воздействиям.
Что это значит для здоровья мозга
В совокупности исследование изображает GluK3 не как простой выключатель, а как тонко настраиваемый узел, где сходятся глутамат, вспомогательные белки и цинк. Neto1 и Neto2 задают, как быстро угасают сигналы и как быстро рецепторы могут снова отвечать, тогда как цинк может либо дополнительно усиливать, либо при определённых условиях сдерживать активность через несколько сайтов связывания. Поскольку GluK3, белки Neto и цинк сосуществуют на синапсах, вовлечённых в память, и связаны с эпилепсией и психиатрическими состояниями, понимание этой многослойной регуляции может направить будущие терапии, которые мягко перенастраивают синаптическую передачу, а не полностью её подавляют.
Цитирование: Vinnakota, R., Dawath, B.K., Assaiya, A. et al. Multilayered regulation of GluK3 kainate receptors is mediated by Neto subunits and zinc. Commun Biol 9, 420 (2026). https://doi.org/10.1038/s42003-026-09707-7
Ключевые слова: каинатные рецепторы, GluK3, белки Neto, синаптический цинк, синаптическая пластичность