Clear Sky Science · ru
Злоупотребление наркотиками, вызывающими привыкание, и депрессия — акцент на эпигенетике
Почему это исследование важно для повседневной жизни
Наркотики, вызывающие зависимость, и депрессия часто рассматриваются как отдельные проблемы, но нередко встречаются вместе у одного и того же человека. В этом обзоре объясняется, как длительное употребление таких веществ, как метамфетамин, кокаин, опиоиды и каннабис, может оставлять длительные «молекулярные шрамы» в мозге, повышающие риск депрессии. Выявляя эти скрытые изменения, статья указывает на возможные будущие тесты, которые помогут определить наиболее уязвимых людей, — и на более точные методы лечения, способные восстанавливать повреждения, а не только маскировать симптомы.
Как зависимость и упадок настроения переплетаются
Авторы начинают с описания тесной клинической связи между злоупотреблением наркотиками и депрессией. Люди, регулярно употребляющие психоактивные вещества, значительно чаще сообщают о длительной печали, утрате удовольствия, нарушениях сна и суицидальных мыслях. Ключевые участки мозга, контролирующие вознаграждение, мотивацию, память и принятие решений — вентральная тегментальная область, прилежащее ядро, префронтальная кора и гиппокамп — играют центральную роль в обоих состояниях. Хроническое воздействие наркотиков нарушает баланс таких нейромедиаторов, как дофамин и серотонин, гормонов стресса, регулируемых гипоталамо-гипофизарно-надпочечниковой осью, иммунных сигналов и энергетического обеспечения нейронов. В совокупности эти изменения снижают стрессоустойчивость мозга и делают его более подверженным депрессивным состояниям, даже спустя длительное время после последней дозы.
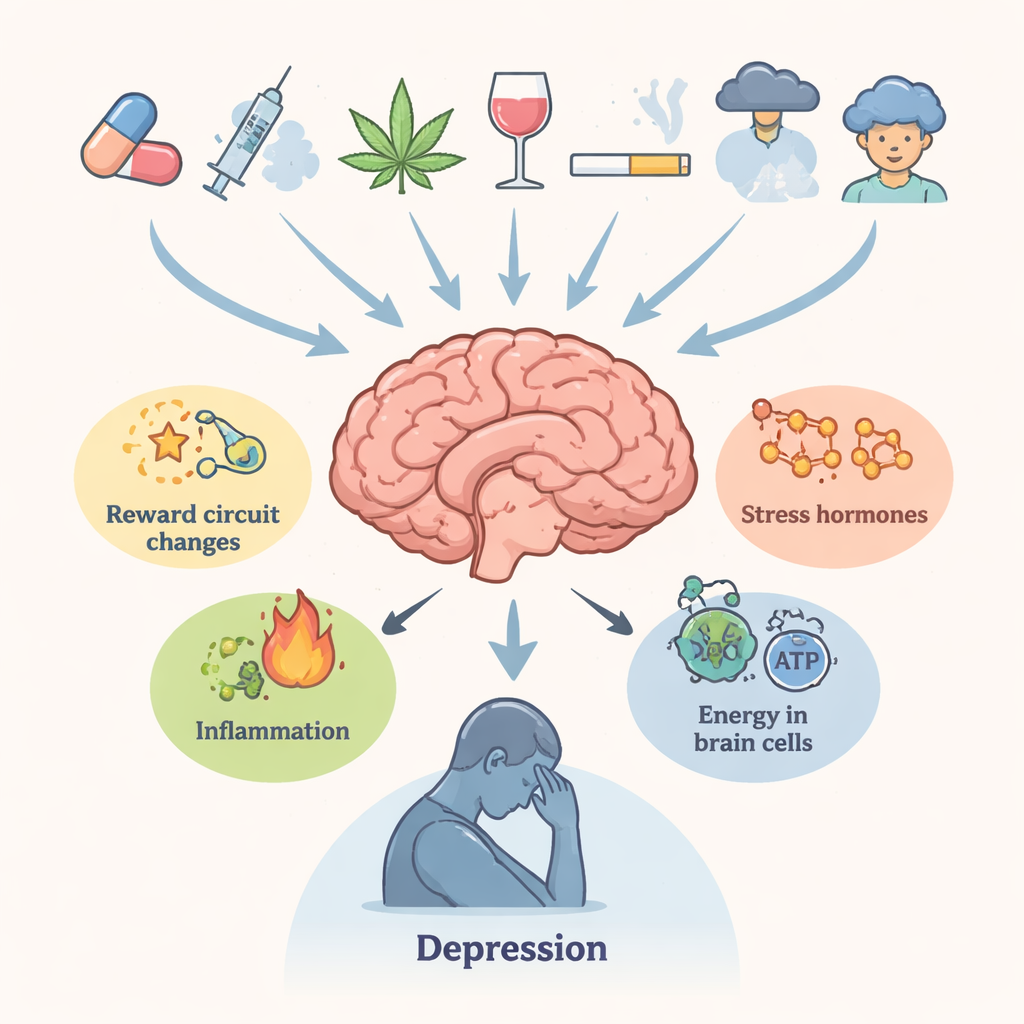
Вещества, перестраивающие химию мозга
Обзор охватывает несколько основных классов наркотиков. Амфетаминоподобные стимуляторы и их аналоги, включая синтетические «соляные» смеси, вызывают мощные всплески дофамина и других трансмиттеров, которые со временем повреждают нервные окончания, нарушают баланс глутамата, перегружают эндоплазматический ретикулум и стимулируют вредные процессы самопереваривания клеток (аутофагию). Употребление каннабиса в подростковом возрасте связано с повышенным риском депрессии и суицида в дальнейшем, вероятно, за счёт долговременных изменений в рецепторах каннабиноидов, структуре белого вещества и чувствительности дофаминовых цепей. Опиоиды, хотя и облегчают боль, могут вызывать воспаление, сбои митохондрий и снижение сигнальной поддержки роста, например фактора нейротрофического происхождения мозга (BDNF). Кокаин многократно активирует систему стресса и изменяет ключевые регуляторы, такие как FKBP5, что способствует тревоге и подавленному настроению в период отмены. Во всех этих случаях биологические нарушения имеют тенденцию сохраняться, помогая объяснить, почему эмоциональные симптомы могут длиться дольше видимого опьянения.
Эпигенетика: память о воздействии
Чтобы понять, почему эффекты наркотиков сохраняются, авторы сосредотачиваются на эпигенетике — химических метках и молекулярных переключателях, которые регулируют активность генов без изменения букв ДНК. Наркотики, вызывающие зависимость, изменяют метилирование ДНК (метка на основаниях цитозина), модифицируют химические группы на гистонах, упаковывающих ДНК, и влияют на некодирующие РНК, тонко настраивающие синтез белков. Например, метамфетамин и кокаин изменяют паттерны метилирования в зонах, связанных с системой вознаграждения, меняя уровни ферментов, добавляющих или удаляющих эти метки. Опиоиды и стимуляторы перестраивают ацетилирование и метилирование гистонов на генах, управляющих глутаматными рецепторами, стрессовой сигнализацией и синаптической структурой. Десятки микроРНК, длинных некодирующих РНК и циркулярных РНК увеличиваются или уменьшаются при воздействии наркотиков, в совокупности влияя на воспаление, рост нейронов и прочность синапсов. Эти эпигенетические изменения действуют как молекулярная «память» истории воздействия наркотиков.
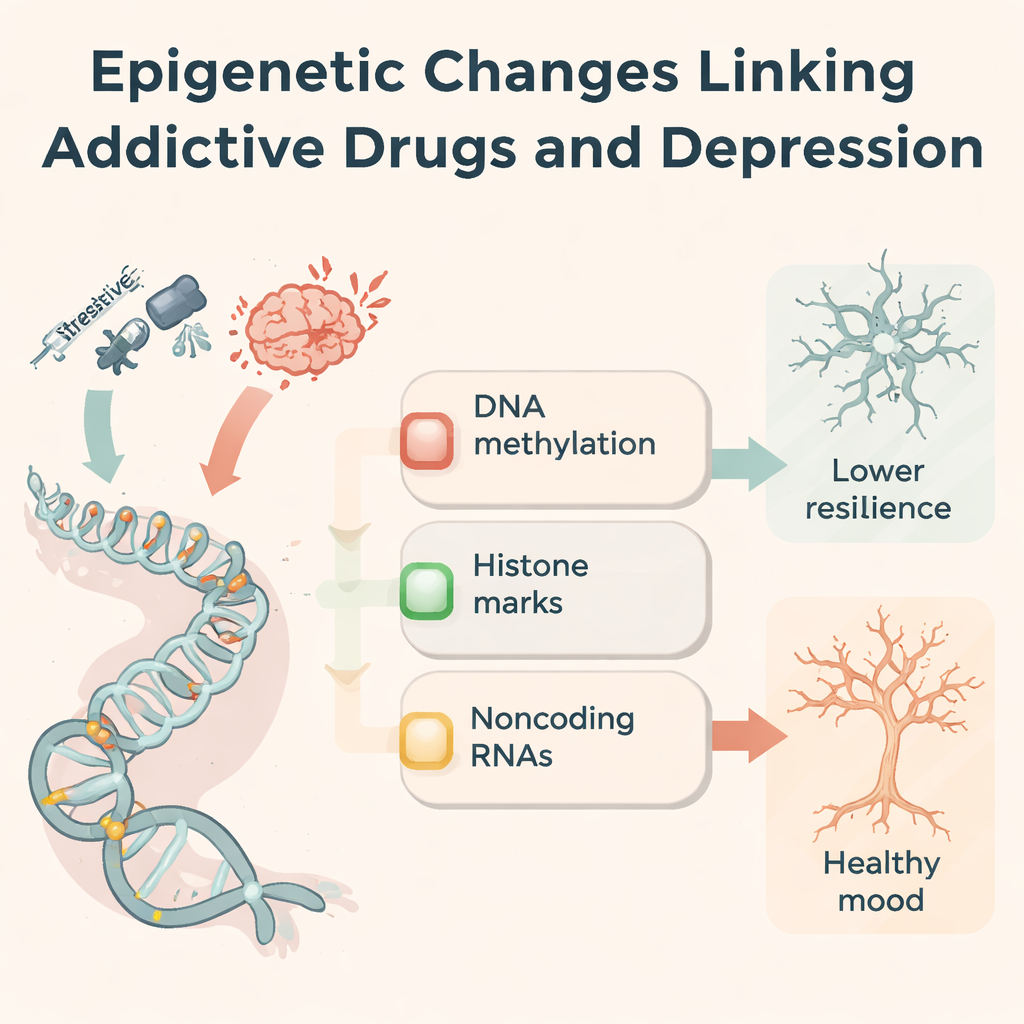
Общие молекулярные пути при депрессии и зависимости
Та же эпигенетическая «аппаратура» обнаруживается и у людей и животных с депрессией, которые никогда не принимали наркотиков. Стрессовые события могут менять метилирование рецепторов гормонов стресса (таких как NR3C1 и FKBP5), уменьшать полезные факторы роста вроде BDNF и перестраивать иммунные и глутаматные пути. Многие из тех же некодирующих РНК, изменяющиеся под действием наркотиков, также дисрегулированы при депрессии, влияя на нейрогенез, реакцию микроглии на воспаление и прочность синаптических связей. Авторы предлагают трехчастную рамку: регуляция реакции на стресс, перестройка цепей вознаграждения и синаптическая пластичность. По этим осям зависимость и депрессия неоднократно сходятся на небольшом наборе генов и меток, что указывает на биологическую причину частого сосуществования этих расстройств.
Что это значит для профилактики и лечения в будущем
В заключение обзор утверждает, что эпигенетические изменения могут стать маркерами раннего предупреждения и мишенями для лекарств нового поколения. Широко действующие препараты, стирающие эпигенетические метки, уже показали некоторые антидепрессивные эффекты у животных, но они слишком грубые для рутинного применения у людей. Новые инструменты — такие как редакторы эпигенома на базе CRISPR и терапии, модулирующие конкретные микроРНК или длинные РНК — возможно, однажды позволят скорректировать проблемные гены в отдельных клетках мозга, не затрагивая другие. Авторы предостерегают, что большая часть текущих данных получена на грызунах и в цельной ткани мозга, а человеческая биология сложнее. Тем не менее, показывая, как наркотики, вызывающие зависимость, и депрессия записываются в одну и ту же молекулярную «тетрадь», эта работа предлагает обнадеживающий путь к более персонализированным и длительным методам терапии.
Цитирование: Zhang, W., Xu, M., Wang, C. et al. Addictive drug abuse and depression-a focus on epigenetics. Commun Biol 9, 297 (2026). https://doi.org/10.1038/s42003-026-09705-9
Ключевые слова: зависимость и депрессия, эпигенетика, злоупотребление наркотиками, метилирование ДНК, некодирующая РНК