Clear Sky Science · ru
Тао необходим для нарушения гематоэнцефалического барьера, вызванного Pseudomonas aeruginosa
Когда инфекции легких достигают мозга
Пневмонию обычно рассматривают как заболевание легких, но многие люди, пережившие тяжелые легочные инфекции, затем сталкиваются с проблемами памяти и мышления или даже развивают деменцию. В этом исследовании поставлен внешне простой, но важный вопрос: как инфекция в легких может так быстро нарушить защитный гематоэнцефалический барьер мозга и создать условия для долгосрочного повреждения? Сосредоточившись на белке тау — наиболее известном по исследованиям болезни Альцгеймера — авторы выявляют неожиданный мост между пневмонией, мозговыми сосудами и изменениями, связанными с деменцией.
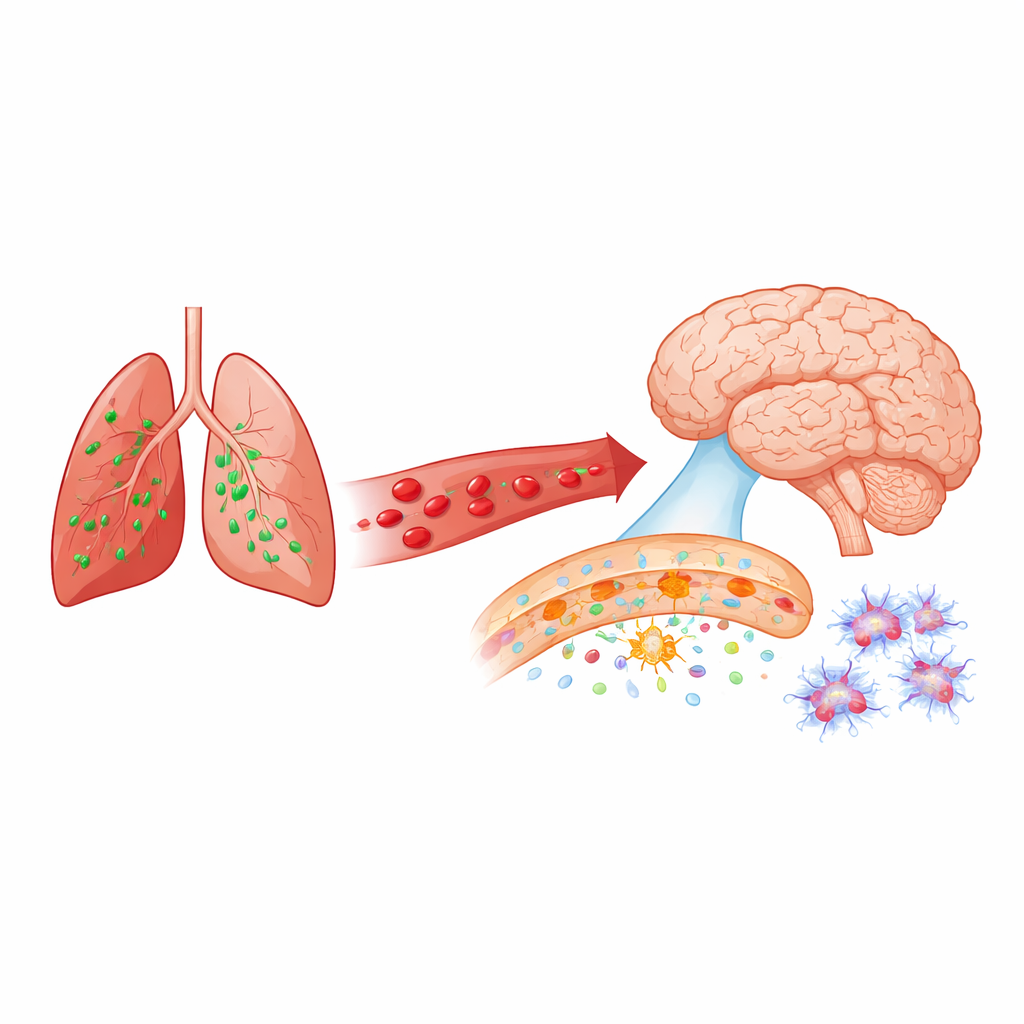
Защитник мозга под нагрузкой
Мозг отделен от остального тела гематоэнцефалическим барьером — плотной сетью клеток, выстилающих мелкие кровеносные сосуды. Этот барьер тщательно контролирует, что попадает в ткань мозга и выходит из нее. При многих заболеваниях мозга — от болезни Альцгеймера до инсульта — этот «страж» становится проницаемым на ранних стадиях. Исследователи использовали модель мышей с бактериальной пневмонией, вызванной Pseudomonas aeruginosa, микроорганизмом, часто провоцирующим тяжелые внутрибольничные инфекции легких. Они поставили вопрос, может ли такая инфекция, находящаяся далеко от головы, быстро ослабить гематоэнцефалический барьер и активировать клетки‑опоры в мозге.
Тао: от молекулы памяти до первичного реагента
Тао — это белок, который помогает стабилизировать внутриклеточные «рельсы» внутри нейронов. При болезни Альцгеймера и родственных расстройствах тау подвергается аномальным модификациям и образует клубки, тесно связанные с потерей памяти. Ранее эта группа показала, что легочные инфекции могут приводить к высвобождению повреждённого, токсичного тау из сосудов легких, и что этот материал может вредить нейронам. Опираясь на эти данные, текущее исследование проверяло, меняется ли тау внутри мозга после пневмонии и требуется ли сам тау для того, чтобы инфекция нарушила гематоэнцефалический барьер.
Что происходит в мозге после пневмонии
У нормальных мышей одна легочная инфекция вызвала быстрое, но селективное открытие гематоэнцефалического барьера в течение 24 часов. Крупные иммунные белки из крови проникали в гиппокамп и кору — области, важные для обучения и памяти — в то время как очень большие молекулы по‑прежнему оставались снаружи. Одновременно звездообразные клетки‑опоры, называемые астроцитами, становились более реактивными, а иммунные клетки мозга (микроглия) в течение следующих двух дней переходили в более активные формы. Тау внутри мозга также изменялся: несколько форм тау, ассоциированных с патологией Альцгеймера, стали сильнее модифицированы, и классический маркер Альцгеймера AT8 резко возрос, особенно к 48 часам. Эти сдвиги сопровождались изменениями в активностях сигнальных ферментов, известных как акторы тау, что указывает на то, что инфекция быстро перенастраивает биологию тау в мозге.
Удаление тау меняет исход
Наиболее впечатляющие результаты получены у мышей, генетически лишенных тау. Эти животные перенесли ту же легочную инфекцию и продемонстрировали аналогичные всплески провоспалительных мессенджеров в крови и мозге. Тем не менее, несмотря на этот воспалительный шквал, их гематоэнцефалический барьер оставался неповрежденным, и астроциты не становились реактивными. Микроглия по‑прежнему реагировала, и некоторые воспалительные сигналы в мозге даже усиливались у мышей без тау, но ключевого структурного повреждения барьера не наблюдалось. Ферменты, которые обычно модифицируют тау, изменяли активность и у этих животных так же, как у нормальных мышей, что указывает на то, что сигнальные каскады все же работали — но без тау барьер и астроциты в значительной степени были защищены.
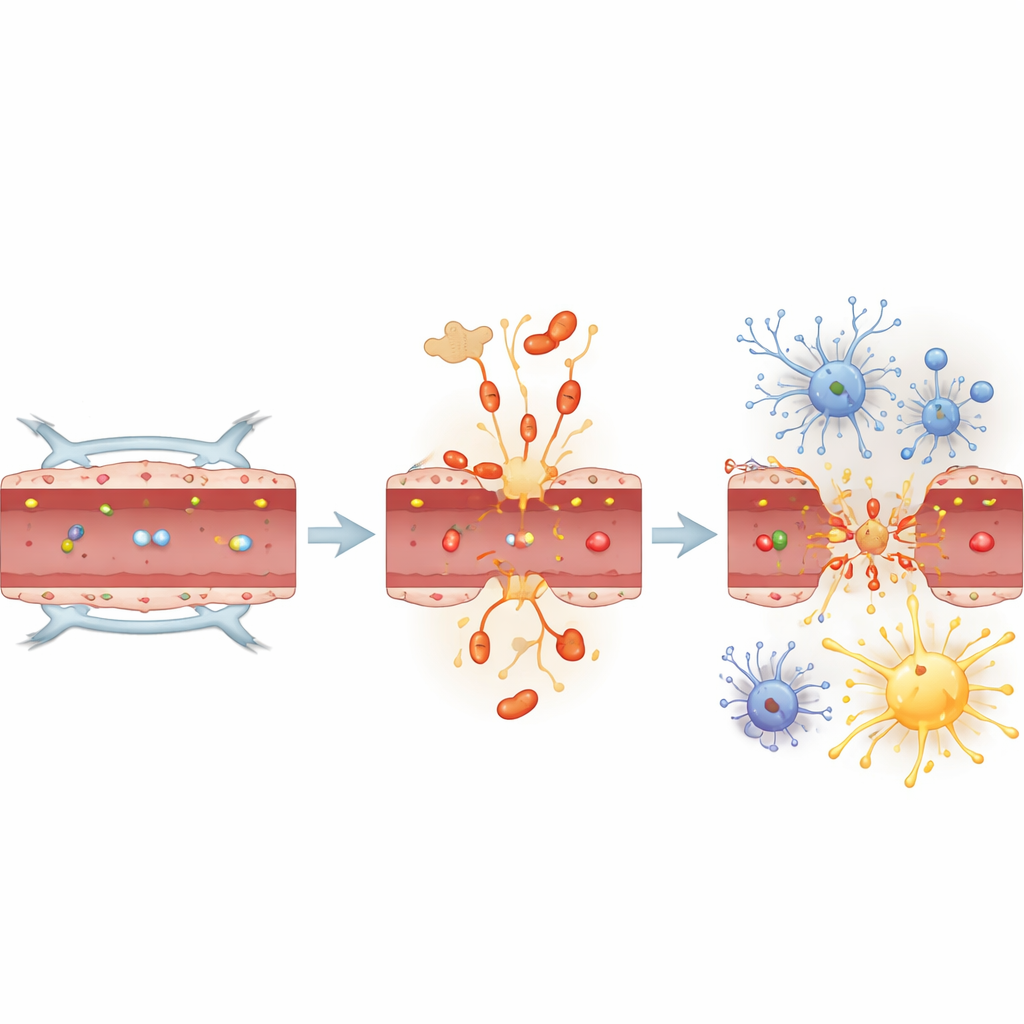
Почему это важно для деменции
В совокупности результаты указывают на то, что тау — не просто пассивная жертва при заболеваниях мозга, а активный участник, связывающий легочную инфекцию с ранними мозговыми изменениями. В данной модели пневмония быстро делала гематоэнцефалический барьер проницаемым, активировала клетки‑опоры и увеличивала формы тау, связанные с деменцией — но только при наличии самого тау. При его отсутствии одних только воспалительных сигналов было недостаточно, чтобы вызвать разрушение барьера. Для неспециалиста это означает: белок, долго ассоциировавшийся с болезнью Альцгеймера, возможно, также действует как молекула врожденного ответа при тяжелых инфекциях и помогает определить, оставит ли временная болезнь долговременные следы в мозге. Нацеливание на индуцированные инфекцией токсичные формы тау может однажды помочь защитить защитную «стену» мозга у пациентов с тяжелой пневмонией и, возможно, снизить их последующий риск когнитивного снижения.
Цитирование: Chaney, S.D., Bauman, A.J., Butlig, EA.R. et al. Tau is necessary for Pseudomonas aeruginosa-induced blood-brain barrier dysfunction. Commun Biol 9, 427 (2026). https://doi.org/10.1038/s42003-026-09703-x
Ключевые слова: пневмония, гематоэнцефалический барьер, белок тау, нейровоспаление, риск деменции