Clear Sky Science · ru
Энергетическая недостаточность митохондрий лежит в основе сенсорной невропатии, связанной с FLVCR1
Когда болевые нервы остаются без энергии
Некоторые люди рождаются практически неспособными чувствовать боль. На первый взгляд это может показаться даром, но быстро превращается в проклятие: без боли как сигнала предупреждения они получают ожоги, переломы, инфекции и даже слепоту. В этом исследовании изучается одна редкая форма таких расстройств утраты боли и обнаруживается неожиданный виновник: крошечные электростанции внутри нервных клеток, у которых серьёзно нарушено производство энергии.
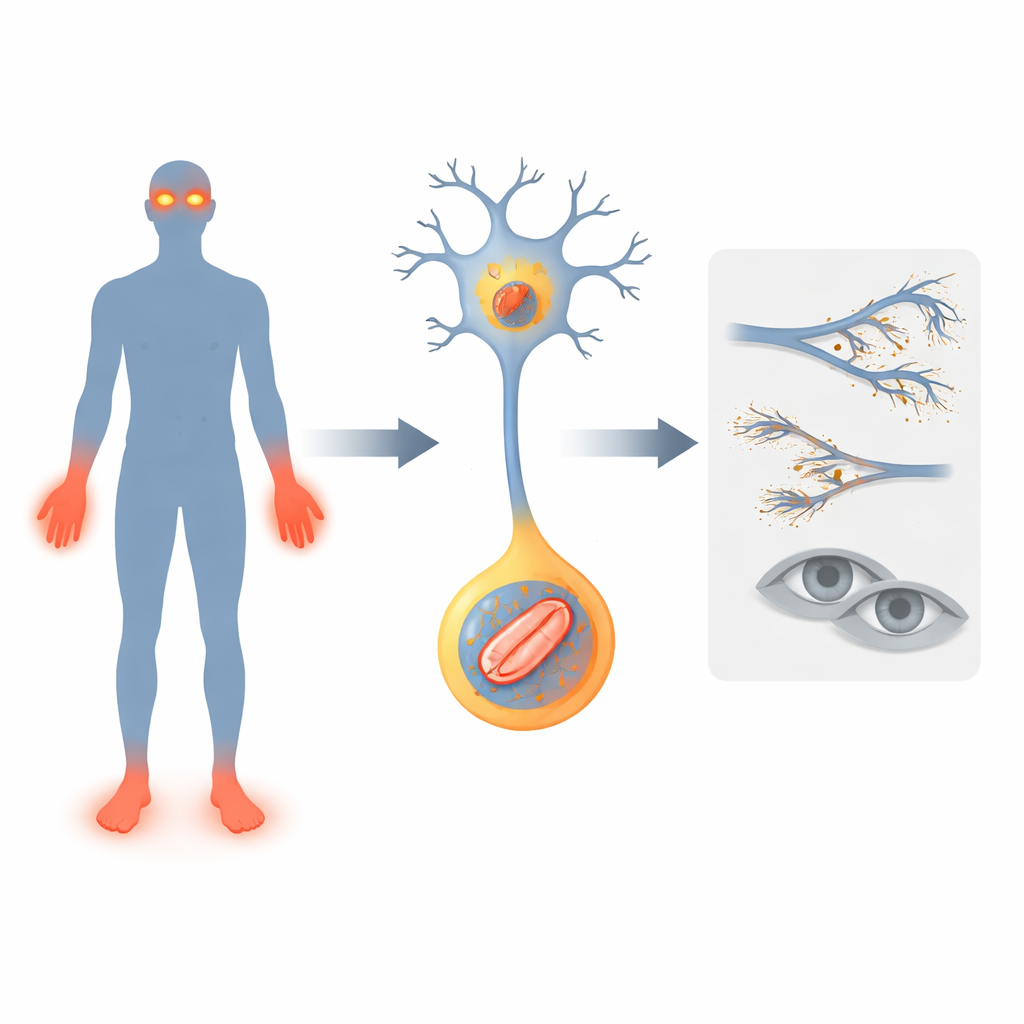
Ген, который отключает сигнал тревоги
Учёные сосредоточились на гене FLVCR1, который уже связывали с редкими нервными заболеваниями, при которых люди теряют болевую чувствительность, развивают нарушение координации ходьбы и иногда прогрессирующую потерю зрения. Они описывают двух новых пациентов с изменениями в FLVCR1. У обоих детей рано проявились проблемы: задержка моторного развития, частые падения, тяжёлые инфекции и самоповреждения пальцев рук и ног, потому что травмы оставались незамеченными. У одного ребёнка также развилось дегенеративное заболевание сетчатки — пигментный ретинит, приводящее к ночной слепоте. Эти случаи расширяют представление о том, как дефекты FLVCR1 могут проявляться у людей, и укрепляют идею о том, что этот ген необходим для выживания болевых нейронов и светочувствительных клеток сетчатки.
Моделирование болезни на крошечных рыбках
Чтобы понять, как FLVCR1 влияет на развивающиеся сенсорные нервы, команда обратилась к данио-рерио (зебровым рыбкам), чьи прозрачные эмбрионы позволяют прямо наблюдать нервные клетки. Они снизили уровень рыбьей версии гена, flvcr1a, с помощью генетических инструментов. У рыб с пониженным flvcr1a было меньше дорсальных ганглиев корней — кластеров нейронов, распознающих прикосновение и боль вдоль позвоночника. Поведенчески такие рыбы двигались меньше самостоятельно и плыли лишь короткие расстояния при лёгком касании хвоста, что указывает на притуплённый сенсорный ответ. Поскольку ранние модели на мышах погибали слишком рано, чтобы проанализировать их сенсорные нервы, эти зебровые рыбки стали первой живой системой, в которой можно детально проследить дефекты нервов и поведения, связанные с FLVCR1.
Три нарушенных пути сходятся на «электростанциях» клетки
FLVCR1 локализуется в мембранах клеток и управляет несколькими ключевыми веществами. Предыдущие работы указывали на его роли в обращении холина (строительного блока мембранных липидов), гемa (железосодержащего пигмента, необходимого многим ферментам) и в обмене кальцием между компартментами клетки. Учёные собрали кожные клетки (фибробласты) от четырёх пациентов с разными мутациями FLVCR1 и сравнили их с клетками здоровых людей и бессимптомными носителями. Они обнаружили пониженные уровни холина и более текучие клеточные мембраны у пациентов — изменения, которые могут нарушать тонкую липидную среду, необходимую митохондриям, органеллам по выработке энергии. Также оказалось, что активность ключевого фермента синтеза гема в митохондриях, ALAS1, была снижена, хотя общий уровень гема выглядел почти нормальным. Одновременно контакты между эндоплазматическим ретикулумом и митохондриями — места, через которые кальций обычно поступает в митохондрии — были короче и встречались реже, а поступление кальция в митохондрии уменьшилось. Три проблемы — дефицит холина, замедлившийся синтез гема и ослабленная передача кальция — все указывали на нарушение работы митохондрий.
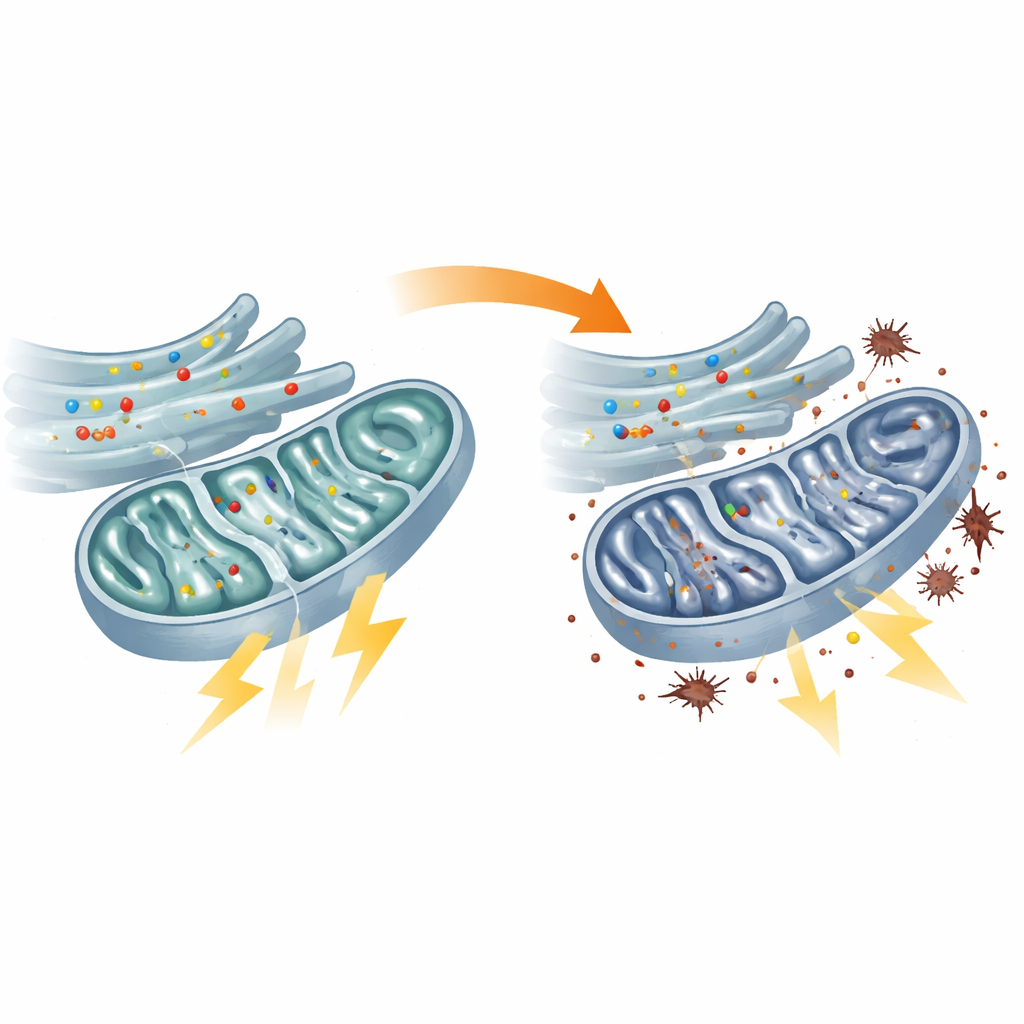
Голодные митохондрии и перегруженные резервные системы
Прямые тесты энергетического обмена подтвердили, что митохондрии в фибробластах пациентов работают с пониженной производительностью. Центральный энергетический цикл (цикл Кребса/TCA) проходил медленнее, активность нескольких его ключевых ферментов была снижена, а цепь реакций, которая обычно превращает топливо в АТФ — «валюту» энергии клетки — была ослаблена. В результате уровень АТФ в митохондриях падал. Клетки пытались компенсировать это за счёт усиления гликолиза — менее эффективного, сахарозависимого пути вне митохондрий. Такая смена энергетической стратегии имела цену: из напряжённой митохондриальной аппаратуры «утекали» электроны, что вызывало повышение перекисного окисления липидов — форму окислительного повреждения клеточных мембран. Подобные дефекты наблюдались и у рыбок с уменьшенным flvcr1a, что напрямую связывает митохондриальную недостаточность с моделью сенсорной невропатии.
Намёки на будущие терапии через усиление клеточной энергетики
Обнадеживает, что некоторые из этих дефектов удалось частично исправить в лаборатории. Когда команда искусственно увеличивала поступление кальция в митохондрии, сверхэкспрессируя каналовый белок MCU в клетках пациентов, продукция энергии восстанавливалась, а признаки окислительного повреждения снижались. Поставка клеткам предшественника гема — 5-аминолевулиновой кислоты (ALA) — также улучшала активность цикла TCA, функцию дыхательной цепи и уровни АТФ, хотя длительное применение ALA в предыдущих исследованиях было вредным. Дополнительный холин нормализовал текучесть мембран и помог уменьшить липидное повреждение, но давал лишь скромный краткосрочный эффект на выработку энергии. Эти эксперименты по восстановлению указывают, что ни один путь не является единственным виновником; вместо этого сеть нарушений в обращении холина, гема и кальция загоняет митохондрии в хроническую недостаточность.
Почему эти результаты важны для пациентов
Проследив последствия мутаций FLVCR1 от молекул до клеток и целых организмов, работа предлагает, что энергетическая недостаточность митохондрий является движущей силой этой формы невропатии с потерей боли и сопутствующими нарушениями зрения. Сенсорные нервы и фоторецепторы особенно требовательны к энергии: они поддерживают длинные аксоны или постоянно обновляют светочувствительные структуры, поэтому особенно уязвимы, когда митохондриальная отдача падает. Модель на зебровых рыбках и клетки, полученные от пациентов, теперь представляют собой практическую платформу для тестирования терапий, укрепляющих митохондриальный метаболизм. Хотя такие подходы, как добавление холина, контролируемое повышение уровня гема или препараты, усиливающие поступление кальция в митохондрии, потребуют тщательной проверки на животных моделях и в клинических испытаниях, основной вывод ясен: восстановление «энергоснабжения» у уязвимых нейронов может однажды помочь защитить людей, рождающихся без самого важного природного сигнала предупреждения — боли.
Цитирование: Bertino, F., Zanin Venturini, D.I., Grasso, E. et al. Mitochondrial energetic failure underlies FLVCR1-related sensory neuropathy. Commun Biol 9, 429 (2026). https://doi.org/10.1038/s42003-026-09691-y
Ключевые слова: сенсорная невропатия, митохондриальная дисфункция, FLVCR1, анальгезия, энергетический обмен в нервах