Clear Sky Science · ru
Малонилирование лизина регулирует подвижность человеческих сперматозоидов
Почему движение сперматозоидов важно
Для многих пар с необъяснимым бесплодием ключевая скрытая проблема заключается в том, что сперматозоиды просто недостаточно хорошо плавают, чтобы добраться до яйцеклетки и оплодотворить её. В этом исследовании изучается тонкая химическая «метка» на белках сперматозоидов — малаяноилирование лизина — которая, по-видимому, действует как невидимый тормоз их движения. Выяснив, как эта метка изменяет энергоснабжение сперматозоидов и внутриклеточные сигналы, работа указывает на новые подходы к диагностике и потенциальному лечению распространённой формы мужского бесплодия, связанной с низкой подвижностью спермы.
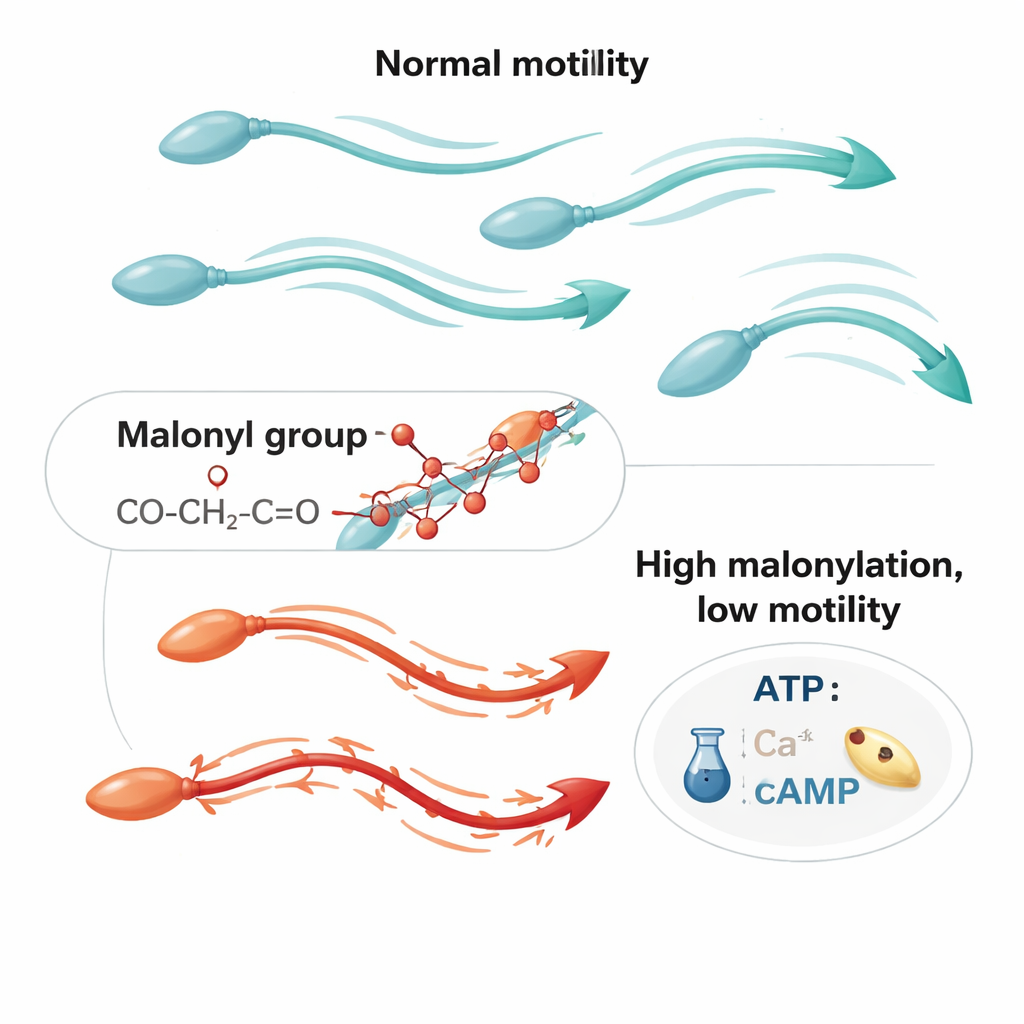
Новая химическая метка на белках сперматозоидов
Белки в наших клетках часто модифицируются после синтеза, приобретая небольшие химические группы, которые могут включать или выключать их активность. Одна из таких модификаций — малаяноилирование лизина — была обнаружена лишь в 2011 году и связывается с энергетическим метаболизмом во многих типах клеток. Авторы раньше показали, что в человеческих сперматозоидах присутствует множество малаонилированных белков, но было неясно, что это значит для фертильности. В новом исследовании они картировали расположение этой метки в сперме и обнаружили её концентрацию в хвосте — длинной хлыстообразной структуре, ритмичное биение которой обеспечивает движение вперёд. С помощью биохимических тестов и высокоразрешающей микроскопии они показали, что малаонилированные белки особенно многочисленны в митохондриях хвоста и в окружающей их среде — ключевых местах производства энергии и контроля движения.
Кто ставит и снимает тормоз
Дальше команда выясняла, какие молекулы устанавливают и удаляют эту малаонильную метку в человеческой сперме. Они получили данные, что фермент, известный как P300, действует как «писатель», помогая переносить малаонильные группы на остатки лизина, в то время как другой фермент, SIRT5, служит «стиральщиком», снимающим эти метки. При блокировании SIRT5 химическим ингибитором общая малаонилизация увеличивалась; при ингибировании P300 малаонилизация снижалась. Они также показали, что натриевая соль малоновой кислоты — малонат натрия — проникает в сперматозоиды и превращается в малонил-КоА, что повышает малаонилизацию, не нарушая при этом другие сходные химические метки. В совокупности эти результаты описывают регуляторную систему, в которой малонил-КоА снабжает метку, P300 её прикрепляет, а SIRT5 — удаляет, тонко настраивая белки хвоста сперматозоида, контролирующие движение.
Больше малаонилирования в плохо движущихся сперматозоидах
Чтобы понять, связано ли это с реальным бесплодием, исследователи сравнили сперму мужчин с нормальными показателями семенной жидкости и мужчин, у которых диагностирована астенозооспермия — состояние, характеризующееся слабой прогрессивной подвижностью. У сперматозоидов из группы с астенозооспермией уровни малаонилирования лизина были значительно выше, а уровни SIRT5 — ниже. По всем образцам больше малаонилирования сильно коррелировало с худшей прямолинейной скоростью движения и с пониженным содержанием клеточного АТФ, основного энергоносителя. В подгруппе мужчин с особенно высоким малаонилированием у спермы наблюдались заметно ослабленные показатели гликолиза — пути расщепления сахаров, который обеспечивает значительную часть топлива для движения человеческих сперматозоидов. Эти закономерности указывают на то, что избыточное малаонилирование связано и с нарушением производства энергии, и с ухудшением плавучести.
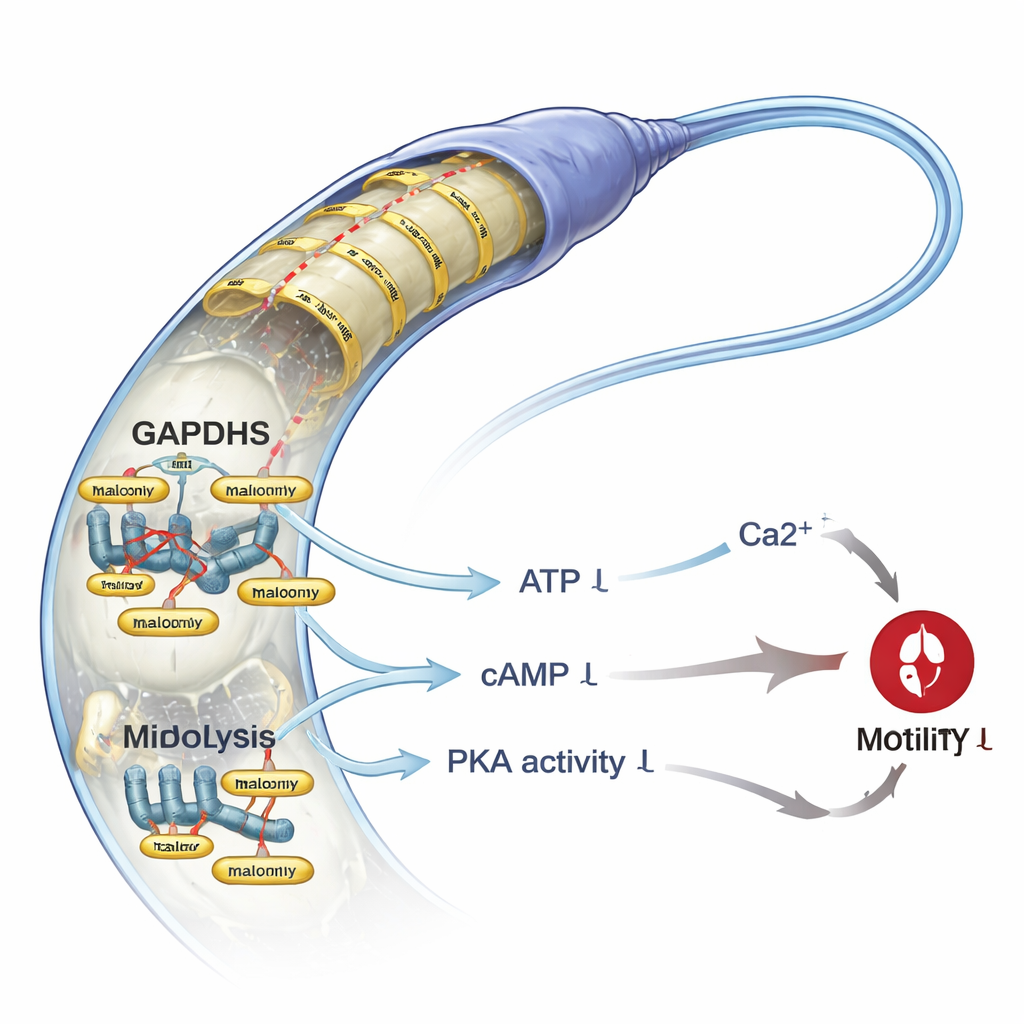
Экспериментальное наращивание тормоза
Учёные затем спросили, что произойдёт, если целенаправленно повысить малаонилирование в казалось бы здоровой сперме. Обработка образцов от мужчин с нормальными параметрами семенной жидкости малонатом натрия увеличивала уровни малаонилирования, но не приводила к гибели клеток. Тем не менее это значительно снижало общую и прогрессивную подвижность и ухудшало способность сперматозоидов продвигаться через вязкую среду, имитирующую женские репродуктивные пути. Механистические тесты объяснили причину: у сперматозоидов, обработанных малонатом натрия, снизился гликолитический выход, уменьшилось количество АТФ и сократилось содержание цАМФ — сигнальной молекулы, активирующей ключевой фермент PKA. Активность PKA упала, как и фосфорилирование белков-мишеней, поддерживающих подвижность. Одновременно внутриклеточный уровень кальция у сперматозоидов снизился примерно вдвое, хотя основной кальциевый канал спермы, CatSper, напрямую не затрагивался. Такое сочетание — меньше энергии, ослабленные сигналы и пониженный кальций — даёт согласованное объяснение наблюдаемой потери подвижности.
От молекулярных меток к мужской фертильности
Суммируя все данные, исследование предлагает, что малаонилирование лизина действует как отрицательный регулятор подвижности человеческих сперматозоидов. Когда уровни малаонилирования повышаются — из‑за низкого SIRT5, высокого малонил‑КоА или нарушения родственных путей — ключевые белки, обеспечивающие гликолиз и работу с кальцием, такие как GAPDHS и VDAC3, становятся чрезмерно помеченными. Это подавляет выработку энергии и критические сигнальные каскады в хвосте сперматозоида, приводя к вялому движению и сниженной способности проникать через вязкие среды. Для непрофессионального читателя основной вывод таков: сперме нужно не только достаточное количество, но и тонко отрегулированные химические системы управления, чтобы поддерживать плавание. Нарушения в небольшой обратимой метке, такой как малаонилирование, могут вносить вклад в иначе необъяснимое мужское бесплодие и в перспективе служить новыми биомаркерами или терапевтическими мишенями для восстановления жизнеспособности спермы.
Цитирование: Cheng, Y., Tian, Y., Chen, H. et al. Lysine malonylation regulates human sperm motility. Commun Biol 9, 178 (2026). https://doi.org/10.1038/s42003-026-09683-y
Ключевые слова: подвижность сперматозоидов, мужское бесплодие, посттрансляционная модификация, малонилирование лизина, энергетический метаболизм