Clear Sky Science · ru
Структурная основа распознавания рецептора летучих мышей SARS-CoV-2 и SARS2-подобными коронавирусами летучих мышей
Почему эта история о летучих мышах и вирусах все еще важна
Пандемия COVID-19 началась более шести лет назад, но ученые до сих пор складывают воедино картину того, как вирус, вызывающий ее — SARS-CoV-2 — стал столь успешен в заражении людей. Ключевая интрига — как этот вирус и его близкие родственники, найденные у летучих мышей, цепляются за белок ACE2 на поверхности клеток — первый и критический шаг для инфекции. Понимание этих микроскопических «замок‑и‑ключ» взаимодействий может прояснить происхождение вируса, пути его адаптации и то, что может произойти, если родственные вирусы вновь перейдут к человеку в будущем. 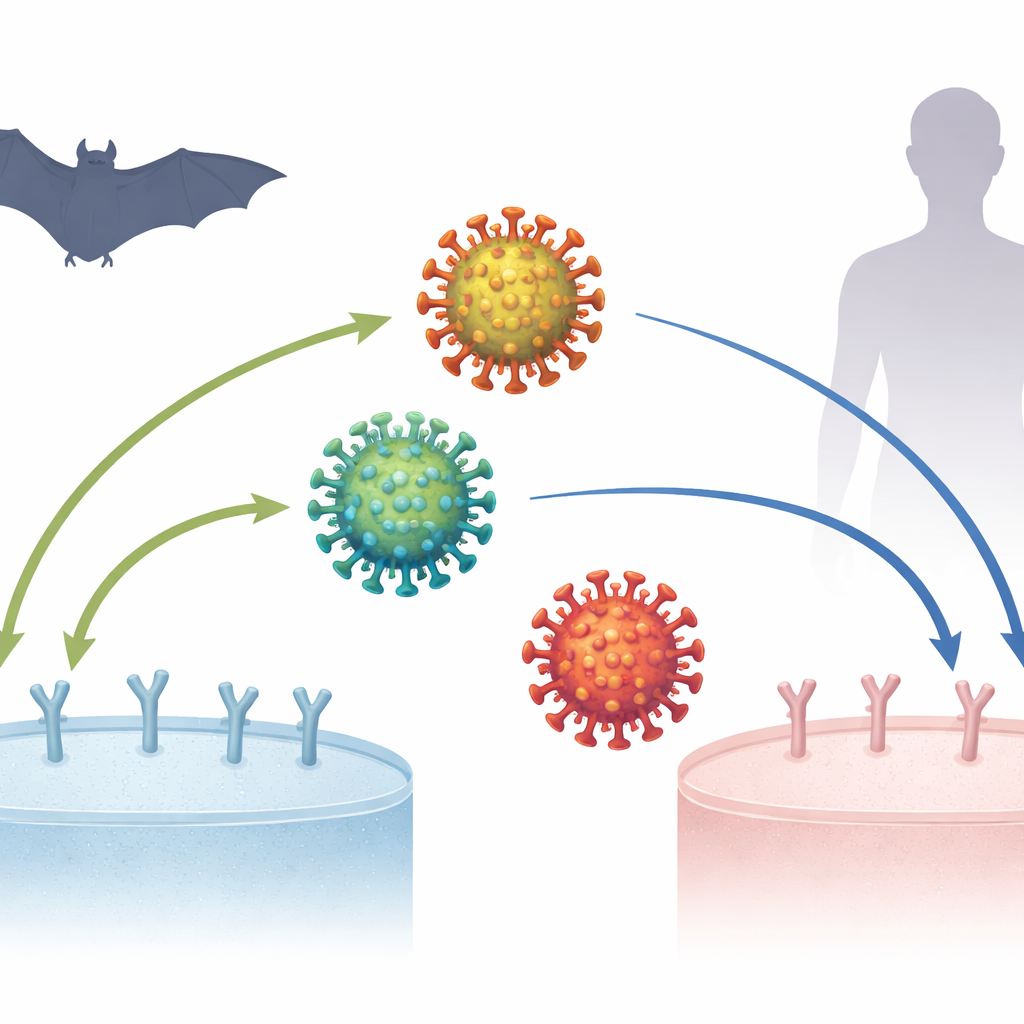
Взгляд на вирусное рукопожатие
Исследование сосредоточено на шиповом белке — венцеобразной структуре на поверхности вируса, которая захватывает ACE2. Небольшой участок шипа, домен связывания рецептора (RBD), действует как кончик пальца, захватывающий «ручку» ACE2. Ранее показали, что при переходах коронавирусов между видами — например, от летучих мышей к циветтам и человеку — RBD часто приобретает мутации, улучшающие захват ACE2 нового хозяина. Но SARS-CoV-2 вызывал вопрос: его исходная форма уже очень хорошо связывалась с человеческим ACE2, даже прежде чем прошло много времени для адаптации, а некоторые вирусы летучих мышей, родственные SARS-CoV-2, казались способными связывать человеческий ACE2 лучше, чем летучий. Это заставило некоторых усомниться, не является ли SARS-CoV-2 исключением из обычных эволюционных правил.
Проверяя рецепторы летучих мышей и человека
Чтобы разобраться в этой загадке, исследователи изучили два коронавируса летучих мышей, близких к SARS-CoV-2, известные как BANAL-52 и BANAL-236. Они сравнили, насколько сильно RBD этих вирусов и SARS-CoV-2 прикрепляются к ACE2 человека и нескольких видов летучих мышей. С помощью клеточных тестов на связывание, точных измерений на биосенсоре и испытаний инфекции с безвредными «псевдовирусами» они обнаружили четкую картину. RBD BANAL-52 связывался сильнее всего с ACE2 одного вида летучих мышей, Rhinolophus sinicus, и несколько слабее — с человеческим ACE2. RBD SARS-CoV-2, напротив, демонстрировал умеренное предпочтение человеческого ACE2 по сравнению с летучьим. В целом RBD BANAL-52 захватывал и летучий, и человеческий рецепторы сильнее, чем RBD SARS-CoV-2, но был наиболее точно настроен на тот конкретный летучий ACE2. 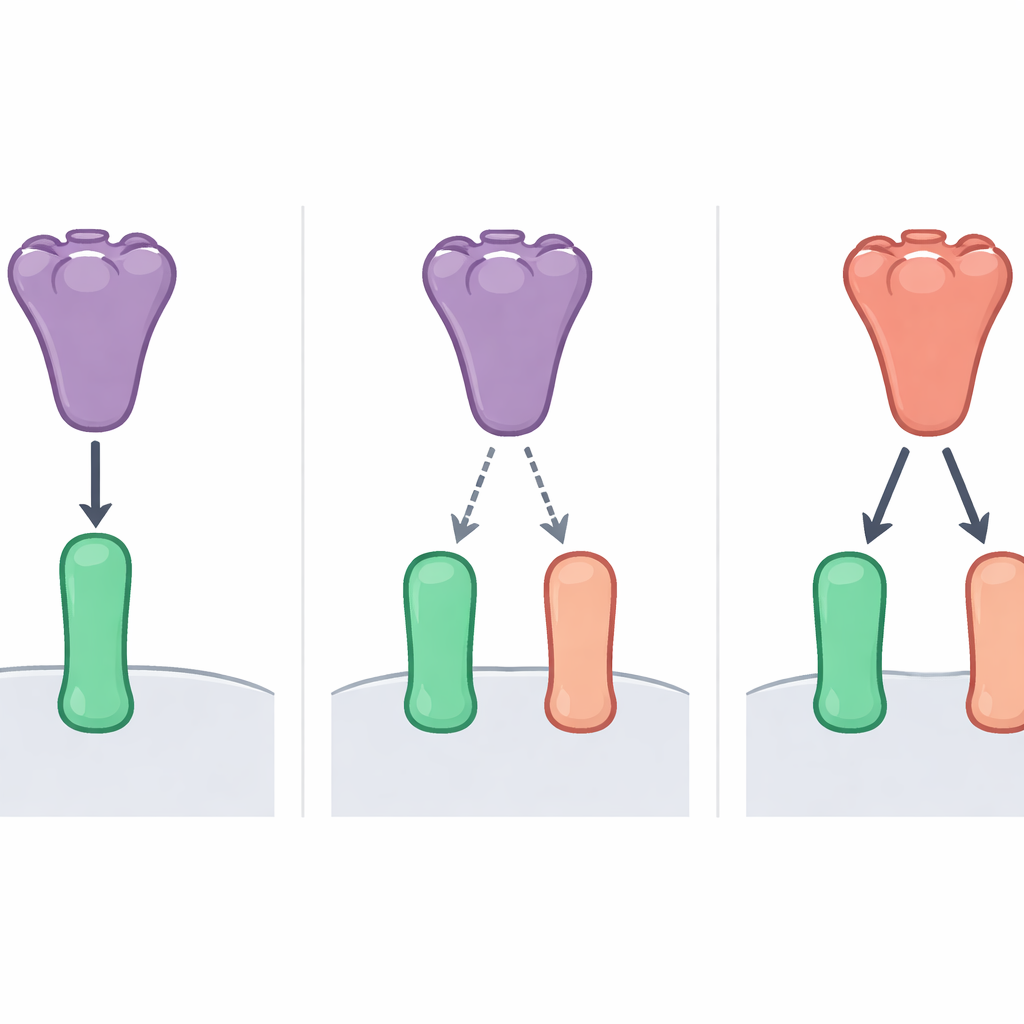
Как атомное изменение меняет расстановку сил
Далее команда обратилась к рентгеновской кристаллографии, которая показывает структуры на атомном уровне, чтобы увидеть, как именно «палец» вируса и «ручка» ACE2 соприкасаются. Они сосредоточились на двух ключевых позициях: одной в RBD вируса (остаток 498) и одной в ACE2 (остаток 41). В BANAL-52 и в соответствующем участке ACE2 летучей мыши обе эти позиции содержат один и тот же строительный блок — гистидин, что позволяет очень плотному, многослойному взаимодействию — укладыванию наподобие двух монет и образованию водородной связи. В человеческом ACE2 на этом месте находится родственный, но немного иной аминокислотный остаток — тирозин, который по-прежнему хорошо укладывается с гистидином BANAL-52, но лишен дополнительной водородной связи. SARS-CoV-2 же использует глутамин в этой вирусной позиции, который не может стэковаться так же, что приводит к более слабому связыванию с ACE2 и летучих мышей, и человека. Путем целенаправленной замены этих аминокислот в летучьем ACE2 исследователи подтвердили, что усиление или ослабление именно этого контакта может изменить, какой вирус или хозяин оказывается предпочтительным.
Почему человеческий ACE2 так гостеприимен
Кроме этого отдельного контакта авторы изучили, почему человеческий ACE2 в целом является таким эффективным входом для коронавирусов. Сравнивая летучий и человеческий ACE2 бок о бок, они выделили несколько человеческих особенностей, которые улучшают вирусное рукопожатие. Две позиции в человеческом ACE2, содержащие аминокислоты гистидин (в позиции 34) и метионин (в позиции 82), создают более сильные водородные связи и гидрофобные «зоны», помогающие RBD вируса плотнее устроиться. Еще один человеческий остаток, треонин в позиции 27, фактически делает связывание немного слабее, чем в версии летучей мыши, но в целом добавленные благоприятные контакты перевешивают. Эти детали согласуются с предыдущими работами, показывающими, что у человеческого ACE2 есть несколько «горячих точек», которые делают его естественно привлекательным рецептором для широкого круга коронавирусов.
Пересмотр истории происхождения
Собрав все данные вместе, исследование утверждает, что SARS-CoV-2 и его родственные летучие вирусы по-прежнему следуют обычному эволюционному сценарию. Шип BANAL-52, по-видимому, лучше всего адаптирован к ACE2 некоторых летучих мышей и при этом совместим с человеческим ACE2. Шип SARS-CoV-2, в свою очередь, лучше настроен на человеческий ACE2, чем на летучий, чему способствуют особые контакты на человеческом рецепторе. Небольшие изменения всего в нескольких позициях — особенно в вирусном остатке 498 и соседних участках — могут сместить баланс в пользу того или иного хозяина. Для неспециалистов главный вывод таков: нет необходимости прибегать к экзотическим объяснениям — стандартные, хорошо понятые структурные принципы белок–белковых взаимодействий достаточно объясняют, как эти вирусы распознают клетки летучих мышей и человека, и подтверждают близкую эволюционную связь между SARS-CoV-2 и родственными коронавирусами летучих мышей.
Цитирование: Hsueh, FC., Shi, K., Aihara, H. et al. Structural basis for bat receptor recognition by SARS-CoV-2 and bat SARS2-like coronaviruses. Commun Biol 9, 398 (2026). https://doi.org/10.1038/s42003-026-09682-z
Ключевые слова: эволюция SARS-CoV-2, коронавирусы летучих мышей, рецептор ACE2, хозяин вируса, связывание шипового белка