Clear Sky Science · ru
Белок, кодируемый вирусом африканской чумы свиней MGF 505–3R, нарушает врожденный иммунитет через убиквитин-зависимое разрушение MyD88
Почему это важно для здоровья животных и не только
Африканская чума свиней уничтожила свиноводческие хозяйства по всему миру, угрожая продовольственным поставкам и нанося огромные экономические потери. Вирус во многом смертелен потому, что ускользает от ранних систем обнаружения организма. В этом исследовании раскрыт механизм, с помощью которого один вирусный белок, названный MGF 505–3R, тихо саботирует ключевой «тревожный переключатель» внутри клеток, и показано, что маленький фрагмент этого белка можно также превратить в мощный противовоспалительный инструмент у мышей.
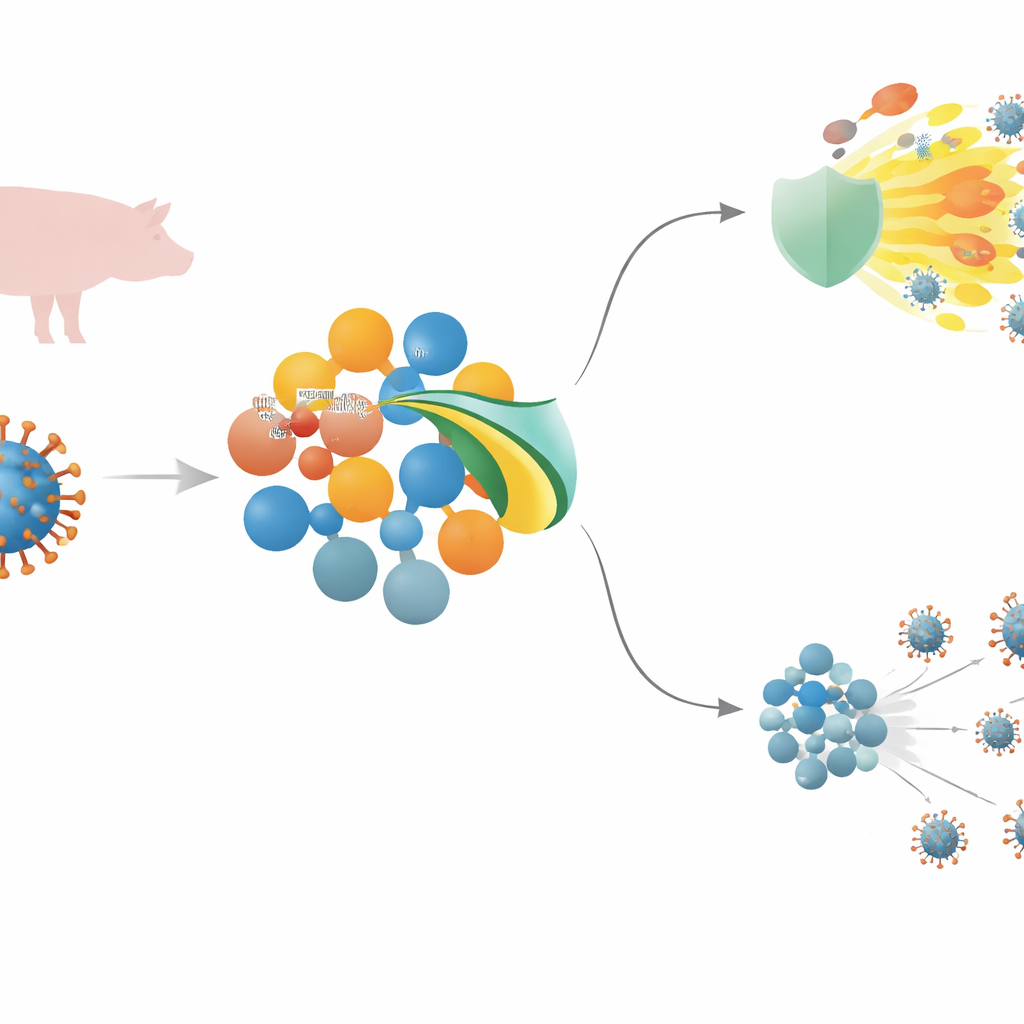
Смертоносный вирус свиней и первая линия защиты организма
Вирус африканской чумы свиней (ASFV) — крупный ДНК-вирус, который может убивать почти каждую заражённую свинью. Чтобы получить почву для размножения, он должен перехитрить врожденный иммунитет — быструю передовую защиту, которая распознаёт захватчиков и вызывает воспаление и выработку противовирусных молекул. В центре этой реакции находится сигнальная цепочка, включающая датчики на поверхности клетки, релейный белок MyD88 и главный переключатель NF–κB, которые вместе запускают синтез провоспалительных посредников и интерферонов. ASFV несёт множество генов, предположительно мешающих этим сигналам, но механизмы многих из них, включая MGF 505–3R, были недостаточно понятны.
Как вирус «перерезает провода» иммунного тревожного сигнала
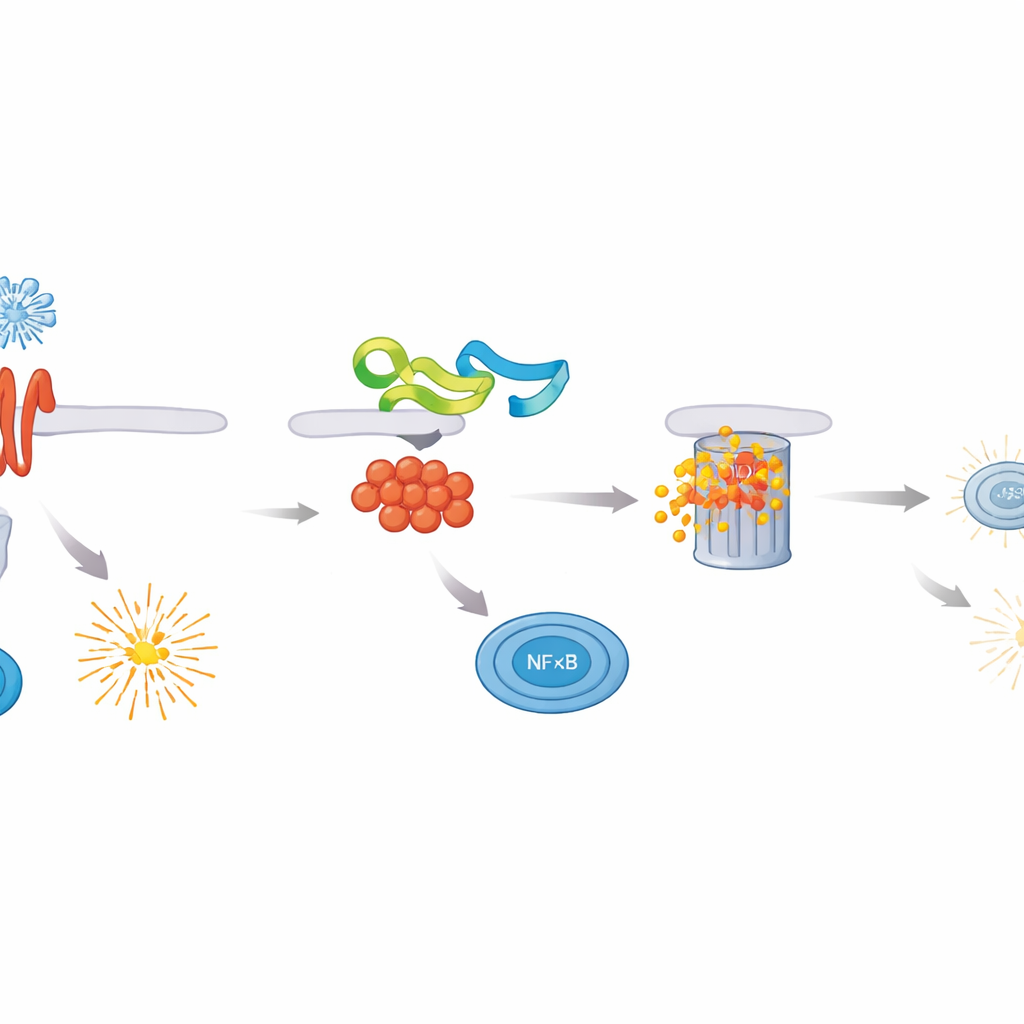
Исследователи проверили белки ASFV на способность подавлять активность NF–κB и обнаружили, что MGF 505–3R является особенно сильным ингибитором. В присутствии этого вирусного белка клетки, подвергшиеся разным иммунным триггерам, вырабатывали значительно меньше провоспалительных цитокинов и гораздо более низкие уровни интерферонов типа I и III. Более детальный анализ показал, что MGF 505–3R действует непосредственно на MyD88 — центральный адаптер, который соединяет многие иммунные сенсоры с NF–κB. MGF 505–3R связывается с MyD88 и помечает его для удаления через клеточный «шредер» белков, используя тип метки, называемый K48-связанной убиквитинацией. По мере разрушения MyD88 NF–κB не перемещается в ядро и не включает защитные гены, что делает клетки более восприимчивыми к размножению вируса.
Внимание на небольшой, но мощный фрагмент белка
Чтобы выявить критическую часть MGF 505–3R, команда создала укороченные версии белка и проверила их эффекты. Они обнаружили, что аминокислоты 89–277 одновременно необходимы и достаточны для связывания MyD88, стимулирования его убиквитинирования и блокирования активации NF–κB. С опорой на компьютерные предсказания структуры белка они выделили два коротких пептида из этой области. Один из них, pep3R–1, выделялся: он резко снижал активность NF–κB, блокировал фосфорилирование и перемещение в ядро субъединицы p65 NF–κB и уменьшал экспрессию провоспалительных цитокинов и интерферонов в иммунных клетках, стимулированных различными сигналами опасности. В культурe клеток и полный вариант MGF 505–3R, и pep3R–1 не только ослабляли противовирусную сигнализацию, но и позволяли тестовому вирусу более эффективно реплицироваться, подчёркивая, насколько мощно это препятствие для контроля инфекций.
Превращение вирусного трюка в потенциальное лекарство
Затем команда изучила, можно ли использовать пептид для подавления вредного воспаления, а не для помощи вирусам. В модели колита у мышей, вызванного химическим агентом DSS, животные обычно теряют вес, развивают кровавую диарею и демонстрируют серьёзные повреждения и инфильтрацию иммунных клеток в толстой кишке. Мыши, получавшие pep3R–1, перенесли болезнь значительно легче: баллы тяжести болезни были ниже, толстыe кишки были длиннее и здоровее, а микроскопическое исследование показало сохранённую структуру ткани с гораздо меньшим количеством воспалительных клеток. Уровни ключевых провоспалительных молекул, таких как TNF–α, IL–1β, IL–6, и фермент, связанный с притоком лейкоцитов, были снижены как в ткани толстой кишки, так и в крови. В отдельном эксперименте pep3R–1 также уменьшал воспалительный ответ на системный бактериальный токсин, указывая на способность подавлять как локальные, так и общесистемные воспалительные вспышки.
Что это значит для свиней, людей и будущих методов лечения
Эта работа показывает, что белок ASFV MGF 505–3R помогает вирусу выживать, разрушая центральный иммунный релей — MyD88, тем самым отключая как провоспалительные, так и интерферонные защиты. Одновременно небольшой фрагмент этого вирусного белка, pep3R–1, можно переориентировать для безопасного охлаждения чрезмерного воспаления у мышей, в том числе в модели заболевания кишечника. Хотя предстоит многое — улучшение стабильности, доставка и испытания в других моделях заболеваний — исследование выявляет как критическую уязвимость, на которую можно направить антивирусные стратегии, так и перспективную схему для разработки новых пептидных противовоспалительных препаратов, вдохновлённых вирусными механизмами уклонения от иммунитета.
Цитирование: Liu, H., Sun, L., Wang, F. et al. African swine fever virus–encoded protein MGF 505–3R impairs innate immunity via ubiquitin–mediated degradation of MyD88. Commun Biol 9, 407 (2026). https://doi.org/10.1038/s42003-026-09681-0
Ключевые слова: Африканская чума свиней, врожденный иммунитет, NF-kappaB, MyD88, противовоспалительный пептид