Clear Sky Science · ru
Нарушение железного гомеостаза опосредует повреждение кохлеарных волосковых клеток и потерю слуха у мышей с дефицитом Gprasp2
Почему это важно для повседневного слуха
Потерю слуха часто представляют как простое «изнашивание», но у многих людей её вызывают скрытые генетические дефекты. В этом исследовании показано, как малоизученный ген GPRASP2 защищает тонкие клетки восприятия звука внутреннего уха от повреждений, вызванных железом. Демонстрируя конкретные механизмы сбоев при отсутствии этого гена, работа открывает путь к более точной диагностике и будущим терапиям наследственных нарушений слуха и, возможно, сопутствующих расстройств настроения.
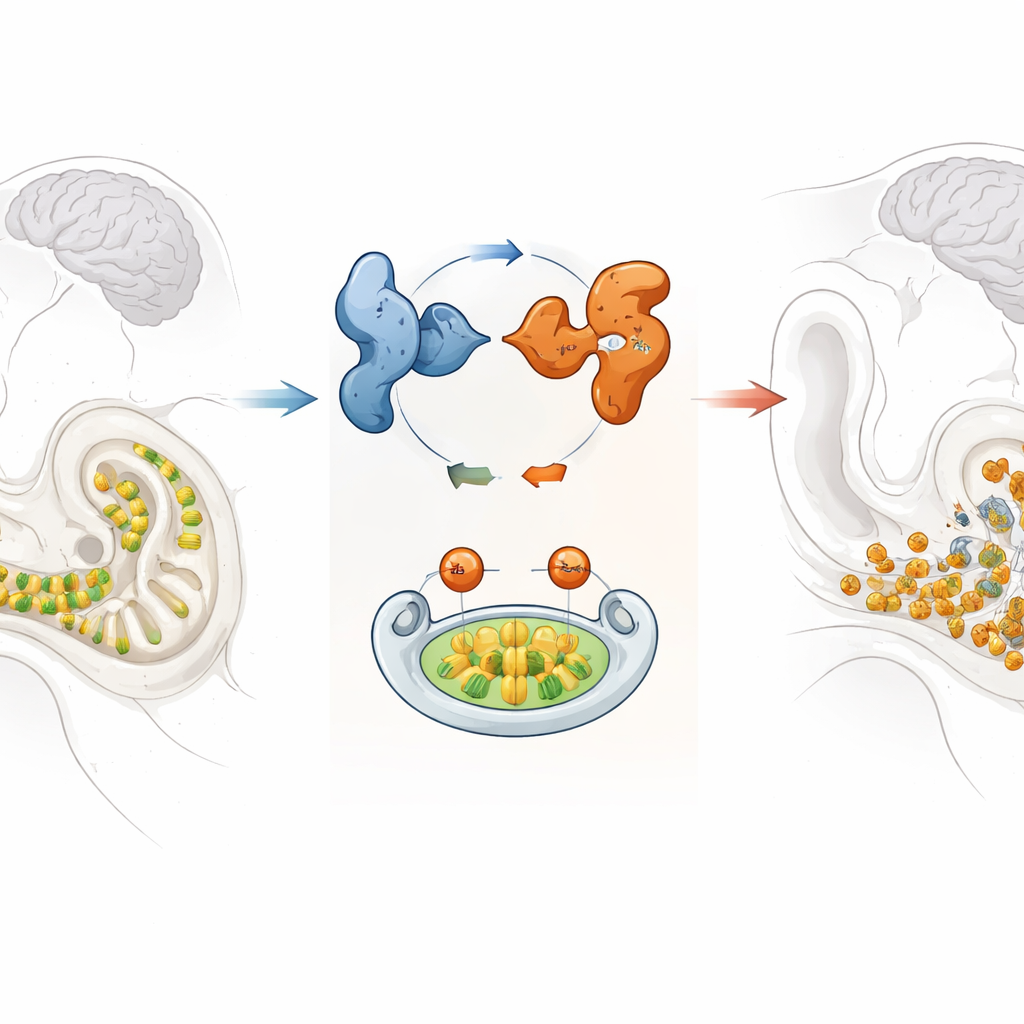
Хрупкий звуковой датчик во внутреннем ухе
В свернутой кохлее внутреннего уха располагаются ряды волосковых клеток, которые преобразуют едва заметные колебания в электрические сигналы, понятные мозгу. Потеря этих клеток необратима, поэтому их сохранение критически важно для слуха на протяжении жизни. Исследователи сосредоточились на GPRASP2 — гене, у которого ранее были обнаружены мутации в семье с Х-сцепленной синдромной потерей слуха, то есть состоянием, в основном поражающим мужчин и сопровождающимся дополнительными симптомами. Хотя GPRASP2 уже знали как активный в мозге и внутреннем ухе, его точная роль в слухе оставалась неясной.
Что происходит при отсутствии гена
Чтобы имитировать человеческое состояние, команда применила редактирование CRISPR и создала мышей без рабочей копии гена Gprasp2. Эти животные показывали явную потерю слуха в широком диапазоне частот при тестировании чувствительными электрическими записями от слухового нерва. Их реакции на внезапные громкие звуки были притуплены, однако равновесие и моторика были в основном нормальными, что указывает на специфическую проблему слуха, а не на общее нарушение движения. Интересно, что мыши также проявляли поведение, похожее на депрессию, в нескольких стандартных тестах, что намекает на связь этого гена со слухом и настроением через его функции в ухе и мозге.
Повреждения внутри кохлеи
При изучении внутреннего уха мышей с дефицитом Gprasp2 учёные обнаружили, что многие наружные волосковые клетки отсутствовали или были смещены, а у оставшихся клеток часто имелись деформированные пучки крошечных отростков, которые обычно действуют как камертоны. Они также заметили изменения в stria vascularis — высокоактивной ткани, поддерживающей особую жидкостную и электрическую среду, необходимую для слуха. На микроскопическом уровне маркеры гибели клеток и окислительного стресса были повышены в наружных волосковых клетках и соседних нервных элементах, что указывает на сильное воздействие реактивных молекул и повышенную вероятность гибели этих структур.
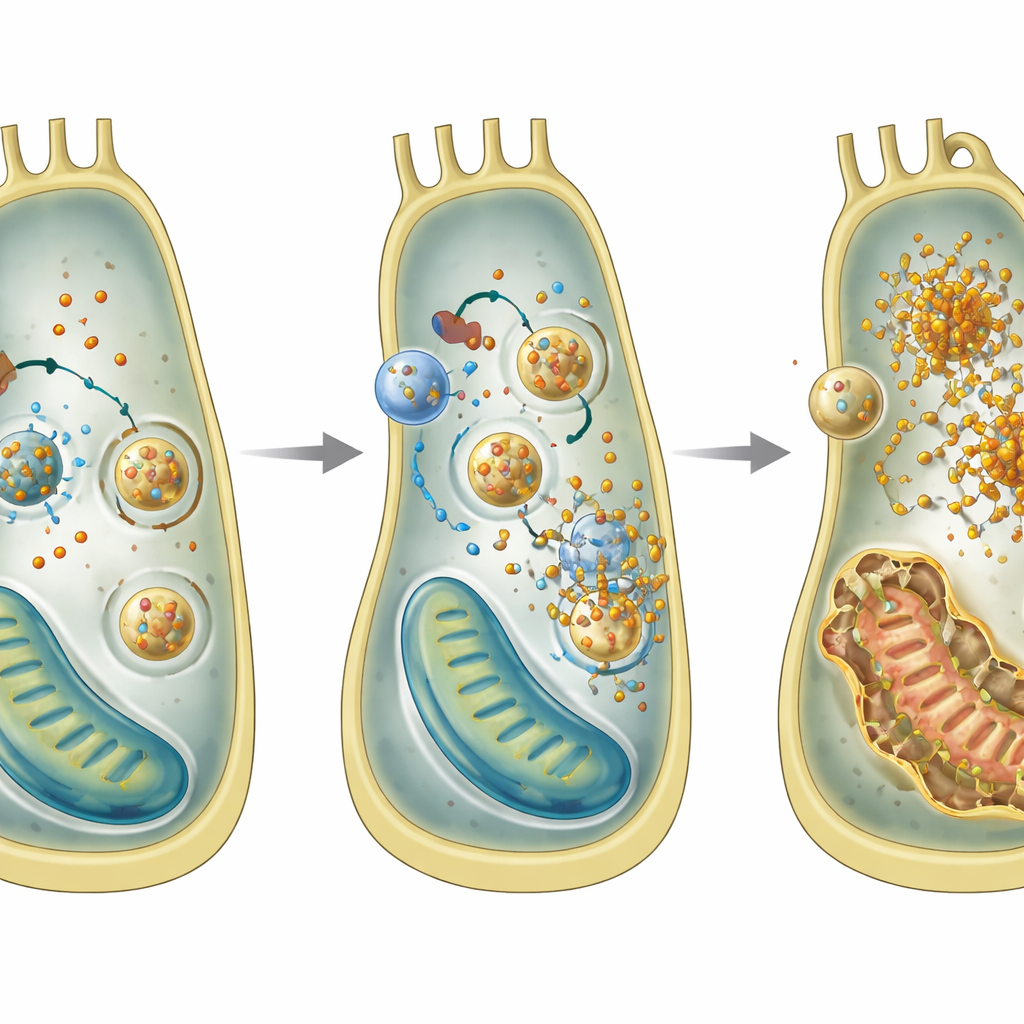
Перегрузка железом и неконтролируемая переработка
Углубившись, команда использовала линию клеток внутреннего уха, чтобы выяснить, что происходит внутри отдельных клеток при отсутствии GPRASP2. Они обнаружили картину, характерную для формы гибели клеток, называемой ферроптозом, которая вызывается железом и перекисным окислением липидов. Клетки без Gprasp2 накапливали больше двухвалентного железа, производили больше реактивных форм кислорода, имели пониженные уровни антиоксиданта глутатиона и показывали повреждение митохондрий. Анализы генов и белков указали на повышение ферритинопагии — процесса, при котором частицы хранения железа доставляются в перерабатывающие компартменты и разрушаются, высвобождая дополнительное железо в клетку. Блокирование этого шага переработки уменьшало накопление железа, что поддерживает идею о том, что чрезмерная ферритинопагия является ключевой для повреждений.
Ключевой белок-партнёр, удерживающий железо под контролем
Далее исследователи спросили, как GPRASP2 контролирует эту систему обращения с железом. Проследив белки, взаимодействующие с GPRASP2, они идентифицировали NCAM1 — молекулу клеточной адгезии, наиболее известную по ролям в обучении, памяти и настроении. Они показали, что GPRASP2 физически связывается с NCAM1, и что потеря GPRASP2 приводит к снижению уровней NCAM1 в волосковых клетках и в культивируемых слуховых клетках. Низкий уровень NCAM1 связывался с усилением ферритинопагии и перегрузкой железом. Восстановление NCAM1 в клетках с дефицитом Gprasp2 уменьшало уровни железа и подавляло ключевые регуляторы ферритинопагии, несмотря на то, что общий аутофагический процесс оставался активным. Это указывает на то, что GPRASP2 точно регулирует специфический путь переработки железа через NCAM1, а не просто включает или выключает всю систему переработки.
Что это значит для слуха и не только
Проще говоря, работа показывает, что GPRASP2 действует как менеджер безопасности для железа внутри кохлеарных волосковых клеток. Когда GPRASP2 присутствует, он взаимодействует с NCAM1, чтобы предотвратить чрезмерный выброс запасённого железа обратно в клетку, удерживая окислительные повреждения под контролем. При нарушении гена обращение с железом выходит из равновесия, клетки «ржавеют» изнутри, и критически важные волосковые клетки умирают, что приводит к потере слуха. Поскольку GPRASP2 и NCAM1 также функционируют в мозге, тот же путь может объяснять изменения настроения у некоторых пациентов. Понимание этого железозависимого механизма разрушения даёт ясную мишень для будущих лекарств или генотерапий, направленных на сохранение слуха у людей с нарушениями, связанными с GPRASP2, или схожими генетическими расстройствами.
Цитирование: Lu, Y., Sheng, F., Yao, J. et al. Abnormal iron homeostasis mediates cochlear hair cell impairment and hearing loss in Gprasp2-deficient mice. Commun Biol 9, 425 (2026). https://doi.org/10.1038/s42003-026-09679-8
Ключевые слова: наследственная потеря слуха, кохлеарные волосковые клетки, железный гомеостаз, ферроптоз, GPRASP2