Clear Sky Science · ru
Практическое руководство по методам таргетного секвенирования РНК на уровне отдельных клеток
Почему важно изучать отдельные клетки
Каждая клетка вашего тела несёт одинаковую ДНК, но разные клетки ведут себя по‑разному. Они делают это, включая или выключая определённые гены и модифицируя РНК молекулы тонкими способами. Современные методы секвенирования РНК по одиночным клеткам могут считывать, какие РНК присутствуют в тысячах клеток одновременно, но при этом они упускают большую часть информации. В этом обзоре поясняется, где современные методики теряют данные и как новые «таргетные» подходы разрабатываются для того, чтобы прицельно рассматривать наиболее важные участки РНК молекул в исследованиях, диагностике и при проектировании терапии.
В чём ограничения современных методов
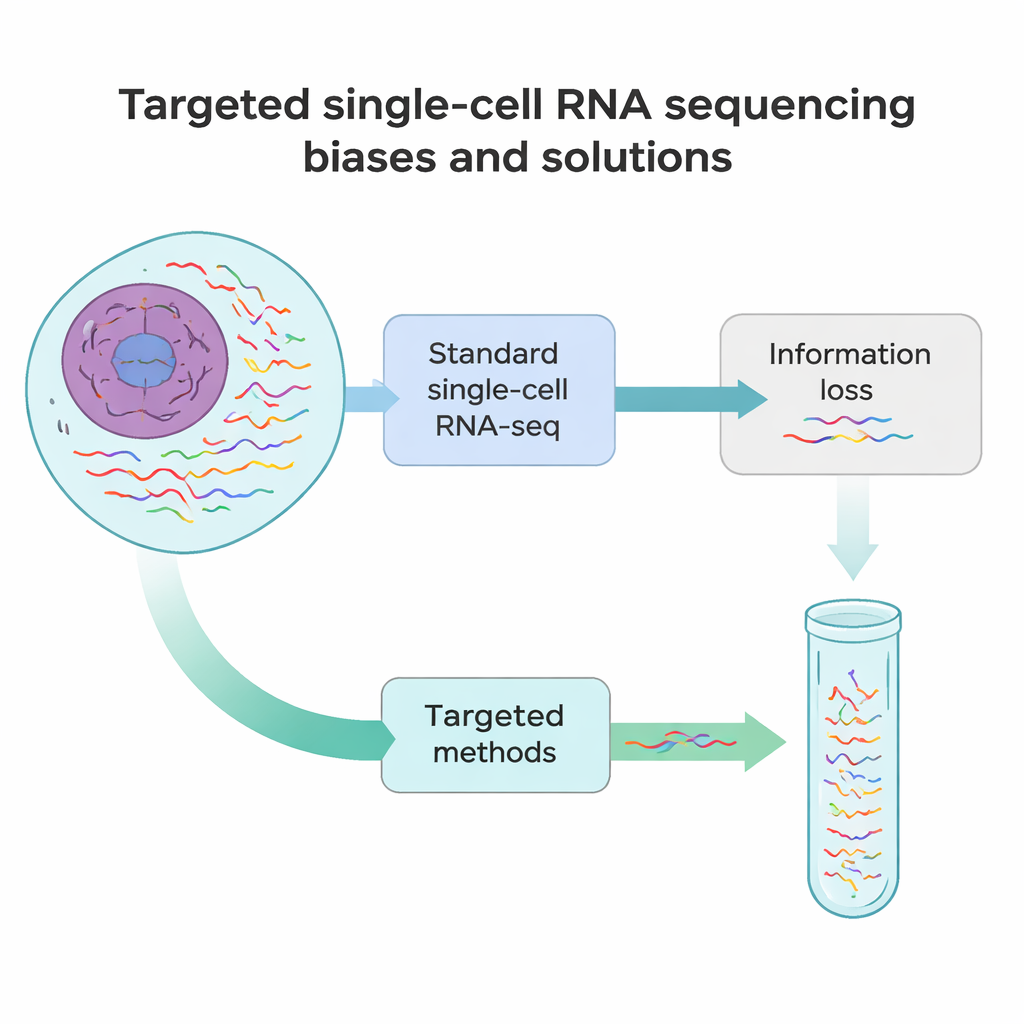
Стандартное секвенирование РНК по одиночным клеткам работает скорее как быстрый снимок каждого сообщения в клетке, чем как полноценный фильм. В большинстве экспериментов обнаруживается лишь около 10–40% всех РНК в клетке, и читается только их начало или конец. Это означает, что многие редкие, но важные РНК — например маркеры, определяющие тип клетки, или варианты генов с патогенными мутациями — легко пропускаются. Кроме того, несколько технических этапов, от разрушения ткани до получения одиночных клеток и до обратной транскрипции и амплификации РНК, вносят систематические искажения. Некоторые РНК обрезаются преждевременно, некоторые оказываются сверхпредставлеными, а другие вовсе исчезают из данных.
Почему важны внутренние детали РНК
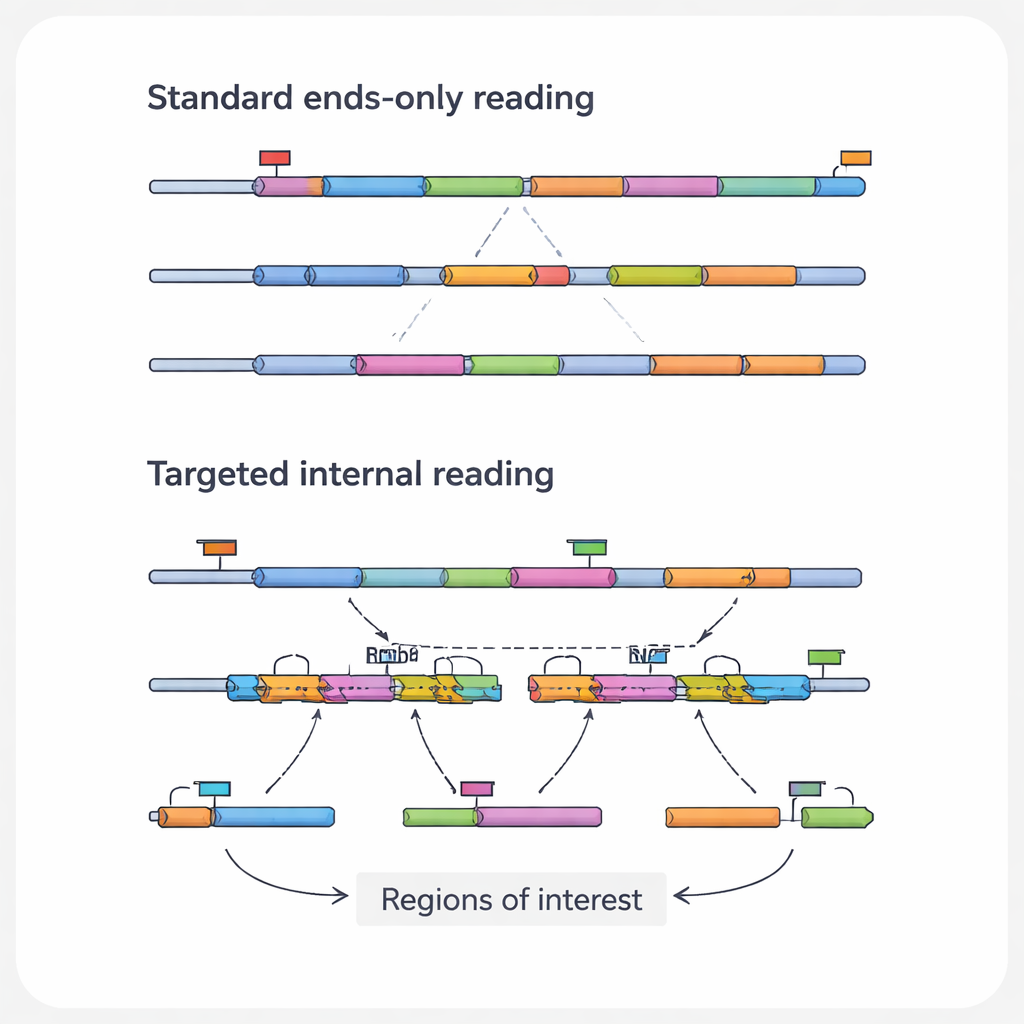
Наиболее медицински значимая информация в молекуле РНК часто содержится во внутренних её областях, а не на концах, которые видят стандартные методы. Внутренние участки могут включать точечные мутации, приводящие к раку, точки слияния двух генов, а также сплайс‑соединения, создающие разные белковые варианты из одного гена. Там же могут оставаться следы работы инструментов редактирования генома, таких как CRISPR. Авторы называют такие специфические элементы «областями интереса», а РНК, несущие их, — «транскриптами интереса». Поскольку распространённые платформы высокого пропускного способа в основном читают «концы» РНК, они регулярно упускают эти важные детали, особенно в длинных или мало представленных транскриптах.
Новые способы нацеливания внимания
Чтобы преодолеть эти «слепые» зоны, исследователи разработали набор таргетных подходов к секвенированию РНК одиночных клеток. Вместо попыток читать все РНК поровну, эти методы целенаправленно обогащают выбранные транскрипты или участки. Некоторые стратегии перепроектируют захватные бусины, чтобы они сцеплялись с внутренними последовательностями РНК, а не только с хвостом, привлекая нужные сообщения в библиотеку уже на первом этапе. Другие добавляют пользовательские праймеры, которые начинают синтез с внутренней точки, или дополнительные этапы ПЦР, которые специфически амплифицируют короткий список генов из уже готовой библиотеки. Ещё одна группа методов использует ДНК‑зонды, гибридизующие с целевыми РНК или их копиями, после чего их выбирают, часто с простыми химическими метками. Каждая категория предполагает компромисс между чувствительностью, количеством клеток, числом целей и стоимостью, но у всех одна цель: восстановить более значимые детали при тех же или меньших объёмах чтений секвенирования.
Применения: от вирусов до опухолей
Эти таргетные методы уже меняют несколько областей биологии и медицины. При инфекциях они позволяют уловить вирусные или бактериальные РНК, лишённые поли(А)‑хвостов, которые стандартные протоколы обычно не замечают, показывая, в каких клетках хозяина они находятся и как меняют активность генов хозяина. В онкологии таргетное секвенирование по одиночным клеткам даёт возможность точно определить, в каких типах клеток присутствуют конкретные мутации или генные слияния, и связать это с изменёнными программами экспрессии, помогая понять, почему некоторые клетки становятся резистентными к терапии. Другие методы фокусируются на альтернативном сплайсинге, раскрывая, какие изоформы каких клеточных типов используются, или на редких популяциях клеток и тонких маркерах, которые в противном случае остаются ниже порога обнаружения. В пуловых CRISPR‑скринингах улучшенный захват гайд‑РНК позволяет связать каждое генетическое возмущение с его точным клеточным ответом.
Как выбрать инструмент и что впереди
Поскольку сейчас доступен широкий набор таргетных подходов, авторы предлагают дерево решений, помогающее исследователям выбрать метод. Ключевые вопросы: требуется ли профилирование всего транскриптома, какое число генов или участков нужно таргетировать, насколько далеко эти участки находятся от концов РНК и сколько клеток планируется обработать. Взгляд в будущее показывает, что наибольшие выигрыши принесут улучшения в самых первых шагах захвата, расширение продуманных зонд‑ориентированных стратегий и сочетание таргетирования с развивающимися платформами для секвенирования длинных чтений и прямого чтения РНК. Пока чтение каждой РНК в каждой клетке «с конца в конец» остаётся непрактичным, таргетное секвенирование РНК одиночных клеток будет необходимым средством для выявления тех частей клеточного сообщения, которые наиболее важны для биологии и медицины.
Цитирование: Moro, G., Brunner, E. & Basler, K. A practical guide to targeted single-cell RNA sequencing technologies. Commun Biol 9, 250 (2026). https://doi.org/10.1038/s42003-026-09675-y
Ключевые слова: секвенирование РНК по одиночным клеткам, таргетное секвенирование, транскриптомика, мутации при раке, пространственная транскриптомика