Clear Sky Science · ru
Природно встречающийся динактин нацелен на белок cpsA и убивает Mycobacterium tuberculosis, нарушая протонный движущий фактор
Новая надежда против упорного легочного убийцы
Туберкулез по‑прежнему остается одним из самых смертоносных инфекционных заболеваний в мире, при этом распространяются штаммы, устойчивые к нескольким антибиотикам. В этом исследовании представлен природный компонент — динактин, продуцируемый почвенными бактериями, который способен убивать Mycobacterium tuberculosis, включая лекарственно‑устойчивые и дремлющие формы, особенно трудно устранимые. Исследователи, выяснив механизм действия динактина и его взаимодействие с существующими лекарствами, наметили многообещающую стратегию для сокращения и усиления терапии туберкулеза.
Поиск скрытого оружия в природе
Чтобы найти новые препараты против туберкулеза, команда просеяла более 6000 природных экстрактов из растений и микроорганизмов, оценивая их способность подавлять рост бактерий туберкулеза в целых клетках, а не на изолированных ферментах. Среди множества кандидатов выделился динактин. Он относится к семейству кольцевых молекул, известных как макротетролиды, и проявил сильную активность против стандартных лабораторных штаммов туберкулеза при очень низких дозах, не повреждая эритроциты. При сравнении динактина с близкородственными молекулами он оказался и более мощным, и более селективным, что сделало его лучшим кандидатом для дальнейшего изучения. 
Мощное действие против труднодоступных бактерий
Бактерии туберкулеза могут скрываться в нескольких трудноизлечимых состояниях: активно делиться в легких, находиться в дремлющем состоянии с замедленным метаболизмом или прятаться внутри иммунных клеток. Динактин атаковал их во всех трех состояниях. Он убивал активно растущие клетки туберкулеза с резким падением числа жизнеспособных бактерий и также был эффективен против голодающих, не реплицирующихся клеток, которые часто выживают при стандартной терапии. В модели на человеческих макрофагах динактин проникал в клетки хозяина и снижал число внутриклеточно локализованных бактерий примерно на два порядка. В инфицированных личинках восковой моли, используемых как модель in vivo, динактин в монорежиме увеличивал выживаемость и снижал бактериальную нагрузку, а при сочетании с существующими противотуберкулезными препаратами эффект был еще сильнее.
Вместе с существующими препаратами
Поскольку лечение туберкулеза основывается на комбинированной терапии, исследователи протестировали взаимодействие динактина с текущими антибиотиками, такими как рифампицин, изониазид, бедаквилин и другими. С помощью тестов шашечного типа они обнаружили, что динактин сильно усиливает действие большинства этих препаратов, особенно рифампицина и изониазида: добавление динактина позволяло значительно снизить эффективные дозы стандартных лекарств. Примечательно, что при применении к клиническим изолятам мультирезистентного туберкулеза динактин восстанавливал большую часть их чувствительности к рифампицину и изониазиду. В культурах в фазе покоя, имитирующих персистирующую инфекцию, комбинации динактина с рифампицином или изониазидом убивали значительно больше бактерий, чем любой препарат по‑отдельности, что указывает на то, что смеси на основе динактина могут помочь быстрее очистить упорные инфекции.
Как динактин подрывает энергетику бактерий
Чтобы понять, как динактин убивает бактерии туберкулеза, команда изучила его влияние на оболочку клетки и энергетические системы. Динактин действует как переносчик ионов, перемещая калий и натрий через бактериальную мембрану. Этот дополнительный поток ионов делает мембрану более проницаемой и текучей, визуально морщинит поверхность бактерий и облегчает проникновение красителей. Перемещая ионы, динактин разрушает протонный движущий фактор — электрический и химический градиент, который бактерии используют как крошечную батарею для синтеза АТФ. Замеры показали, что обе составляющие этого градиента — мембранный потенциал и разница протонов — исчезали после обработки динактином. В результате уровни АТФ внутри клеток резко падали, хотя аппаратура потребления кислорода продолжала функционировать, что указывает на рассогласование производства энергии и дыхания. Динактин также нарушал соотношение восстановленной и окисленной форм ключевого метаболического кофактора (NADH/NAD+) и вызывал вспышку реактивных кислородных видов внутри бактерий, дополнительно повреждая клеточные компоненты. 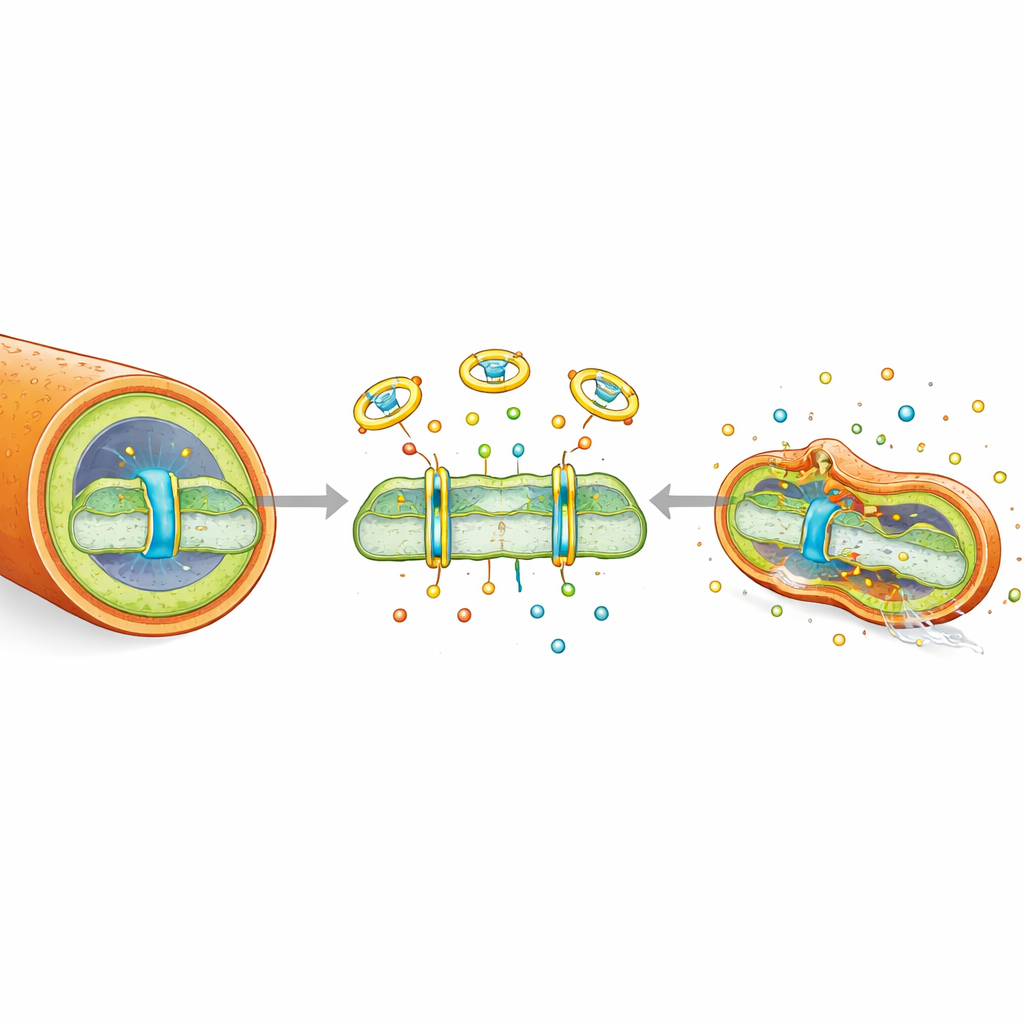
Атака на ключевой строитель клеточной стенки
Чтобы выделить конкретную молекулярную мишень, исследователи выделили редких родственников туберкулеза, которые спонтанно стали менее чувствительны к динакцину, и секвенировали их геномы. У большинства этих мутантов обнаруживали одно и то же изменение в гене cpsA, который кодирует белок из семейства LytR‑Cps2A‑Psr (LCP), участвующий в прикреплении основных компонентов клеточной стенки. При сверхэкспрессии cpsA или его партнерского белка бактерии становились более толерантными к динакцину; удаление cpsA делало клетки более устойчивыми на питательных средах, но также указывало на то, что у динактина, вероятно, есть дополнительные мишени. С помощью структурного моделирования и экспериментов связывания команда показала, что динактин прочно связывается с белком cpsA в конкретной области, а мутация, связанная с устойчивостью, значительно ослабляет это взаимодействие. Поскольку белки LCP широко распространены у грамположительных бактерий и отсутствуют у большинства грамотрицательных видов, такое нацеливание помогает объяснить, почему динактин преимущественно атакует туберкулез и родственные организмы.
Что это может значить для будущего лечения туберкулеза
Для неспециалистов основной вывод заключается в том, что динактин — природное соединение, которое поражает бактерии туберкулеза в их уязвимой точке: снабжение энергией и сборку клеточной стенки. Он ведет себя как крошечный ионный шаттл, который разряжает бактериальную «батарею», лишает клетки АТФ, нарушает их внутреннюю химию и мешает важному белку‑строителю клеточной стенки. При этом он работает в тандеме с передовыми противотуберкулезными препаратами, делая их более эффективными против устойчивых и дремлющих бактерий. Хотя предстоит еще много работы — в частности, испытания безопасности и исследования на млекопитающих моделях — это исследование ставит динактин и родственные молекулы в ряд перспективных строительных блоков для следующего поколения терапий против туберкулеза.
Цитирование: Wang, G., Dong, W., Bai, Y. et al. Naturally occurring dinactin targets cpsA protein and kills Mycobacterium tuberculosis by disrupting the proton motive force. Commun Biol 9, 417 (2026). https://doi.org/10.1038/s42003-026-09654-3
Ключевые слова: туберкулез, динактин, антибиотикорезистентность, энергетический метаболизм бактерий, белки клеточной стенки