Clear Sky Science · ru
Агентно‑ориентированное моделирование клеточной динамики в терапии с применением аутологичных иммунных клеток
Почему «цифровые» клетки важны для лечения рака
Терапии рака, использующие живые иммунные клетки, меняют медицину, но проверять каждую новую идею на животных и людях медленно, дорого и иногда рискованно. В этом исследовании представлена ABMACT — виртуальная лаборатория, которая создаёт «цифровые» раковые и иммунные клетки и позволяет им взаимодействовать на экране компьютера. Воспроизводя и расширяя реальные эксперименты, ABMACT помогает исследователям понять, какие свойства NK‑клеточных терапий наиболее важны, и как оптимизировать расписание лечения задолго до перехода в клинику. 
Превращение клеток в цифровых актёров
ABMACT основана на агентно‑ориентированном моделировании — подходе, в котором каждая клетка становится небольшим программным агентом, который может передвигаться, делиться, умирать или атаковать соседей по простым правилам. Авторы выделили четыре основных типа актёров: опухолевые клетки, агрессивные NK‑клетки, способные убивать опухоль, измотанные NK‑клетки, утратившие эффективность, и «бдительные» NK‑клетки, которые находятся в текучем состоянии, но могут восстановить активность. Правила роста, утомления, миграции и смены состояний этих клеток берутся из существующих лабораторных и животных исследований и кодируются в симуляцию, чтобы тысячи виртуальных клеток могли отыграть миниатюрный курс лечения.
Добавление внутриклеточной проводки
Современное одно‑клеточное секвенирование показывает, какие гены активны в каждой NK‑клетке, но перевести эту молекулярную детализацию в поведение целого организма сложно. ABMACT решает эту задачу, связывая паттерны активности генов с практическими свойствами — например, какова вероятность, что NK‑клетка убьёт опухолевую клетку, или сколько целей она сможет уничтожить прежде, чем истощится. Команда использовала данные по генам и путям сигнализации из моделей лимфомы и опухолей мозга у мышей, чтобы оценить, как конкретные гены сдвигают NK‑клетки в сторону более или менее сильного контроля опухоли. Эти генетически обусловленные эффекты случайным образом присваиваются отдельным виртуальным NK‑клеткам, создавая цифровую популяцию, отражающую естественный набор сильных и слабых киллеров, наблюдаемый в экспериментах.
Воспроизведение и расширение животных экспериментов
Исследователи проверили ABMACT на нескольких экспериментах, где инженерные NK‑клетки применялись для лечения гемопатий и глиобластомы у мышей. В моделях лимфомы симулятор корректно воспроизвёл превосходный контроль опухоли при использовании NK‑клеток, запрограммированных на экспрессию и рецептора, распознающего опухоль, и сигнала роста IL‑15, по сравнению с более простыми продуктами или немодифицированными клетками. Он не только совпал с измеренными размерами опухолей в отдельные моменты времени, но и заполнил покадровую картину ежедневного роста и уменьшения бремени опухоли, экспансии NK‑клеток, их истощения и появления бдительных клеток. В моделях глиобластомы ABMACT снова отслеживал наблюдавшийся контроль опухоли и даже предсказал результаты в отдельном ко‑культурном исследовании без перенастройки, что говорит о том, что его правила захватывают общие черты противостояния NK‑клеток и опухоли.
Тестирование вариантов лечения «что‑если» в кремнии
Поскольку ABMACT работает на компьютере, она может исследовать вопросы, которые было бы трудно или дорого проверять на животных. Авторы систематически варьировали свойства клеток и дозы, чтобы выяснить, какие рычаги сильнее всего влияют на контроль опухоли. Они обнаружили, что соотношение NK‑клеток и опухолевых клеток, способность каждой NK‑клетки многократно убивать множество целей и их базовая убойная сила важнее, чем просто продление жизни клеток. Симулированные повторные введения показали, что более ранние дополнительные дозы и продукты с более высокой силой убийства могут эффективнее предотвращать рецидив опухоли, чем поздние, скромные подкрепления. Модель также исследовала, как плохая хемотаксис NK‑клеток, плотные ткани или участки с низким содержанием кислорода могут задерживать встречи с опухолью и способствовать неудаче лечения. 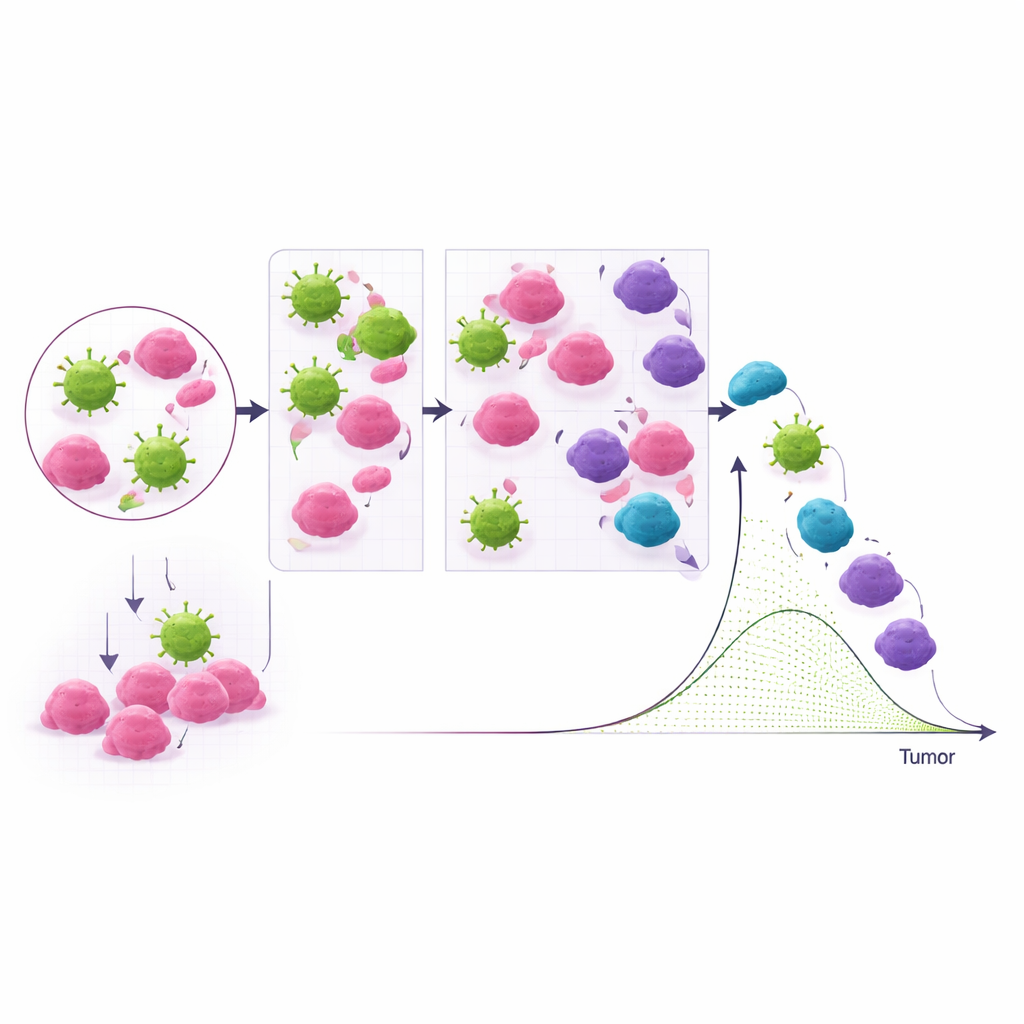
Что это значит для будущих клеточных терапий
Для неспециалиста ABMACT можно рассматривать как высокодетализированный тренажёр полёта для NK‑клеточных противоопухолевых терапий. Опираясь на реальные генетические и экспериментальные данные, эта платформа объясняет, почему одни инженерные NK‑продукты превосходят другие и почему увеличение дозы не всегда даёт лучшие результаты. Она указывает на практические правила проектирования: доставляйте достаточное количество NK‑клеток к опухоли, делайте их эффективными серийными киллерами и планируйте лечения рано и продуманно, вместо простого увеличения дозы. Хотя такие модели не могут заменить лабораторные и клинические испытания, они помогают сократить число вариантов, уменьшить зависимость от животных исследований и со временем — способствовать персонализации клеточных терапий в соответствии с биологией конкретных пациентов.
Цитирование: Wang, Y., Casarin, S., Daher, M. et al. Agent-based modeling of cellular dynamics in adoptive cell therapy. Commun Biol 9, 409 (2026). https://doi.org/10.1038/s42003-026-09653-4
Ключевые слова: терапия аутологичными клетками, киллерные NK‑клетки, агентно‑ориентированное моделирование, иммунотерапия рака, CAR‑NK