Clear Sky Science · ru
Выбор моделей в доклинических исследованиях нуклеиновых терапий
Преобразование генов в лекарства
Терапии на основе нуклеиновых кислот — это новый тип лекарств, которые действуют не за счёт блокирования белков, как большинство препаратов, а шагом раньше — на уровне наших генетических сообщений. В этом обзоре объясняется, как учёные выбирают подходящие лабораторные и животные модели для испытаний этих нацеленных на РНК препаратов до их применения у пациентов. Непрофессиональному читателю это важно, потому что грамотный выбор моделей может ускорить разработку, повысить безопасность и эффективность лечения генетических заболеваний, включая редкие детские расстройства и более распространённые состояния, например сердечно‑сосудистые болезни.
Чем эти генетические лекарства отличаются?
Нуклеиновые терапевтические средства (NATs) включают короткие цепочки, такие как антисенсовые олигонуклеотиды (ASO) и малые интерферирующие РНК (siRNA). Вместо опоры на форму и химические свойства белковых мишеней эти препараты распознают цель по правилам пар оснований — тем же соответствиям A‑T и G‑C, что лежат в основе ДНК. Это делает их программируемыми: узнав последовательность РНК, которую нужно изменить, часто можно быстро спроектировать множество кандидатов без многолетней традиционной химии. Сложность теперь заключается не столько в вопросе «Можем ли мы получить активное соединение?», сколько в «Как измерить, действительно ли это работает в реалистичном биологическом окружении?». Поскольку даже одна буква в последовательности может определить активность, выбор правильных систем тестирования становится критичным.
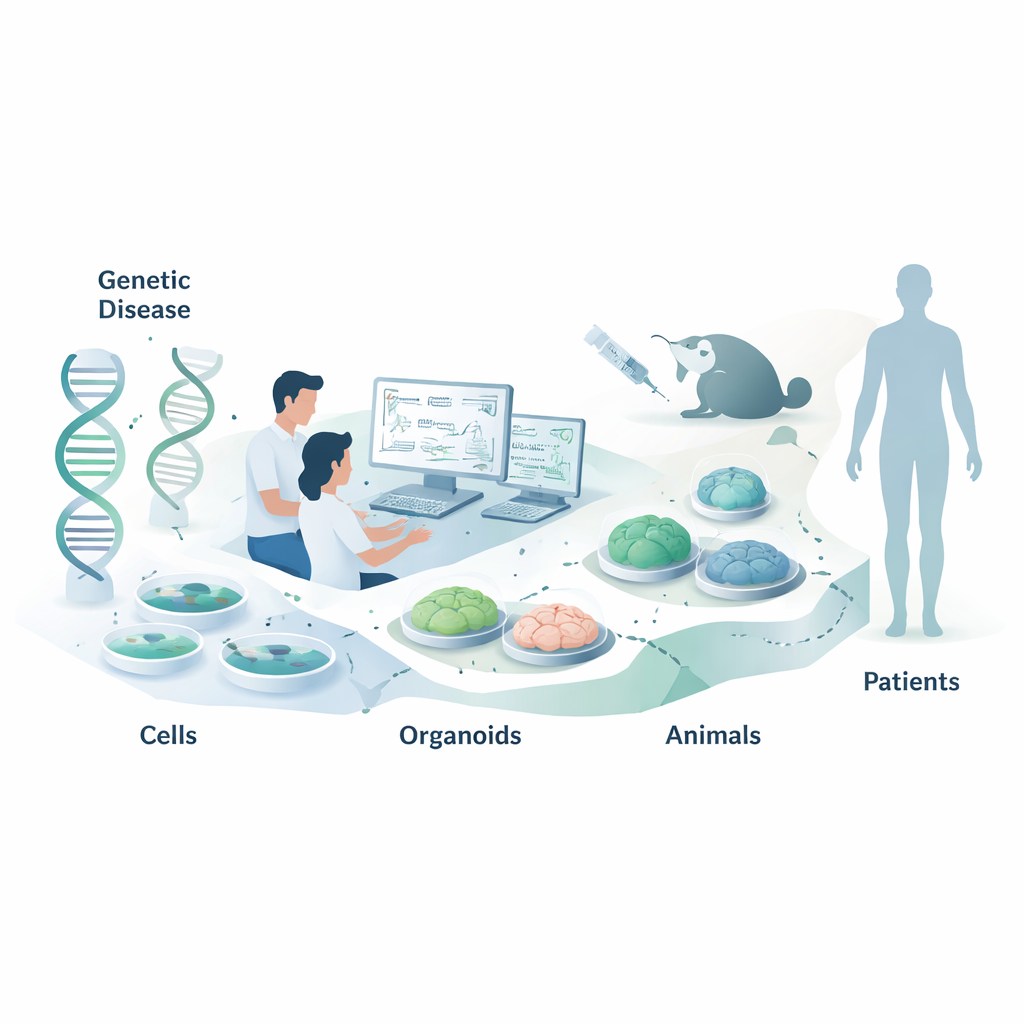
Простые клеточные тесты: быстро, но не вся картина
Первой остановкой для большинства NATs является панель относительно легко выращиваемых клеточных линий, таких как HeLa или HEK293, которые уже экспрессируют целевую РНК. Исследователи добавляют большие библиотеки кандидатов ASO или siRNA и затем измеряют, насколько снизились уровни целевой РНК и соответствующего белка, используя методы, такие как ПЦР и вестерн‑блот. Также работают с клетками, выделенными от пациентов, которые лучше отражают индивидуальный генетический фон и позволяют проверять «аллель‑селективные» препараты, отключающие только дефектную копию гена. Когда природный ген экспрессируется неудобно, учёные иногда вводят искусственные мини‑гены или репортерные плазмиды, которые светятся, когда РНК разрезана или правильно сплайсирована. Эти системы эффективны для быстрой сравнительной оценки множества дизайнов, но они могут не учитывать важные детали, такие как естественная структура РНК или клеточно‑типоспецифическая обработка, поэтому результаты нужно подтверждать в более реалистичных контекстах.
От молекулярного исправления к реальному поведению клетки
Многие NATs стремятся не просто уничтожить дефектную РНК, но и восстановить её, изменяя сплайсинг — процесс, который сшивает фрагменты генетического сообщения. Тщательно спроектированные ASO могут заставить клетку пропустить вредный экзон, восстановить утраченную часть или предотвратить вставку «псевдоэкзона», разрушающего код. Чтобы понять, действительно ли такие изменения улучшают функцию клетки, исследователи переходят от простых измерений уровней РНК и белка к функциональным тестам. В клетках, полученных от пациентов, они проверяют, возвращается ли активность фермента, нормализуется ли транспорт ионов в лёгочных клетках или правильно ли реагируют сигнальные пути в иммунных клетках. Всё чаще используют трёхмерные органоиды — мини‑ткани, выращенные из стволовых клеток пациентов, — которые могут имитировать сердечные сокращения, активность сетей мозга или иные сложные функции. Эти 3‑D модели ближе к настоящим органам, но их труднее, дольше и дороже поддерживать, поэтому команды вынуждены балансировать между реализмом и пропускной способностью.
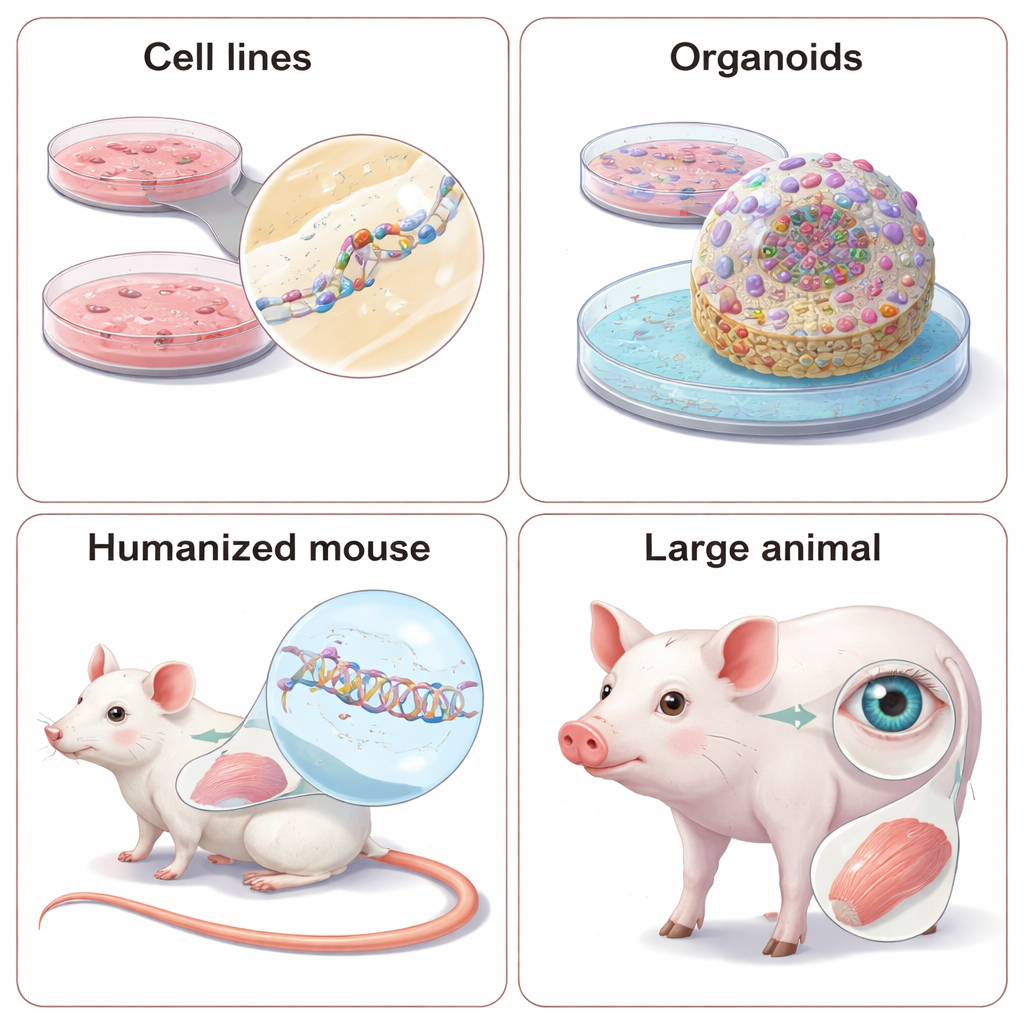
Почему животные всё ещё важны — и как их «очеловечить»
Некоторые проявления болезни, такие как обмен веществ всего организма, взаимодействия между органами или поведение, просто невозможно воспроизвести в культурах. Для этого NATs испытывают на живых животных. Поскольку эти препараты зависят от точных последовательностей РНК, исследователи сталкиваются с выбором: спроектировать «суррогатные» препараты, соответствующие версии гена у животного, либо реинженерить животное, введя человеческие генетические последовательности. Суррогатные ASO и siRNA могут показать, улучшает ли снижение уровня гена симптомы в проверенных мышиных моделях, но они не полностью имитируют препарат, нацеленный на человека. «Человечные» модели — мыши или даже мини‑свиньи с фрагментами или целыми копиями человеческих генов — позволяют тестировать реального клинического кандидата, но требуют значительных затрат времени и денег, и тонкие различия в регуляции генов между видами всё ещё могут привести к неожиданностям. В обзоре также отмечено растущее использование крупных животных, особенно для заболеваний глаза и мышц, где анатомия ближе к человеческой.
Взгляд вперёд: умные модели и меньше догадок
Авторы делают вывод, что не существует единой «лучшей» модели для нуклеиновых препаратов; вместо этого каждый проект требует индивидуального пути, который начинается с быстрых, простых анализов и продвигается к более сложным, релевантным человеку системам. По мере того как регуляторы и спонсоры призывают сокращать использование животных, ожидается, что сложные органоиды, устройства «орган‑на‑чипе» и компьютерные модели будут нести большую часть нагрузки, особенно в сочетании с инструментами машинного обучения, предсказывающими, какие последовательности и химические модификации будут работать лучше всего. В конечном счёте понимание сильных сторон и слепых зон каждой модели — и обмен лучшими практиками и данными в сообществе — позволит надёжнее превращать программируемые генетические идеи в безопасные и эффективные лекарства для пациентов.
Цитирование: Oliver, P.L., Hill, A.C. Model selection in preclinical nucleic acid therapeutics research. Commun Biol 9, 200 (2026). https://doi.org/10.1038/s42003-026-09650-7
Ключевые слова: нуклеиновые терапии, антисенсовые олигонуклеотиды, siRNA, доклинические модели, генная терапия