Clear Sky Science · ru
Wnt11 опосредует взаимодействие фибробластов и гладкомышечных клеток, способствуя нейрогенной фиброзной перестройке мочевого пузыря у крыс
Когда нервы дают сбой, мочевой пузырь рубцуется
Многие люди с повреждением спинного мозга, рассеянным склерозом или болезнью Паркинсона развивают «нейрогенный пузырь», при котором повреждённые нервы больше не могут нормально контролировать накопление и выделение мочи. Со временем стенка пузыря может утолщаться и становиться жёсткой из‑за рубцовой ткани, что угрожает здоровью почек и снижает качество жизни. Это исследование на крысах выявляет ключевой молекулярный фактор, ответственный за образование таких рубцов, и предлагает новые подходы для замедления или даже предотвращения повреждений.
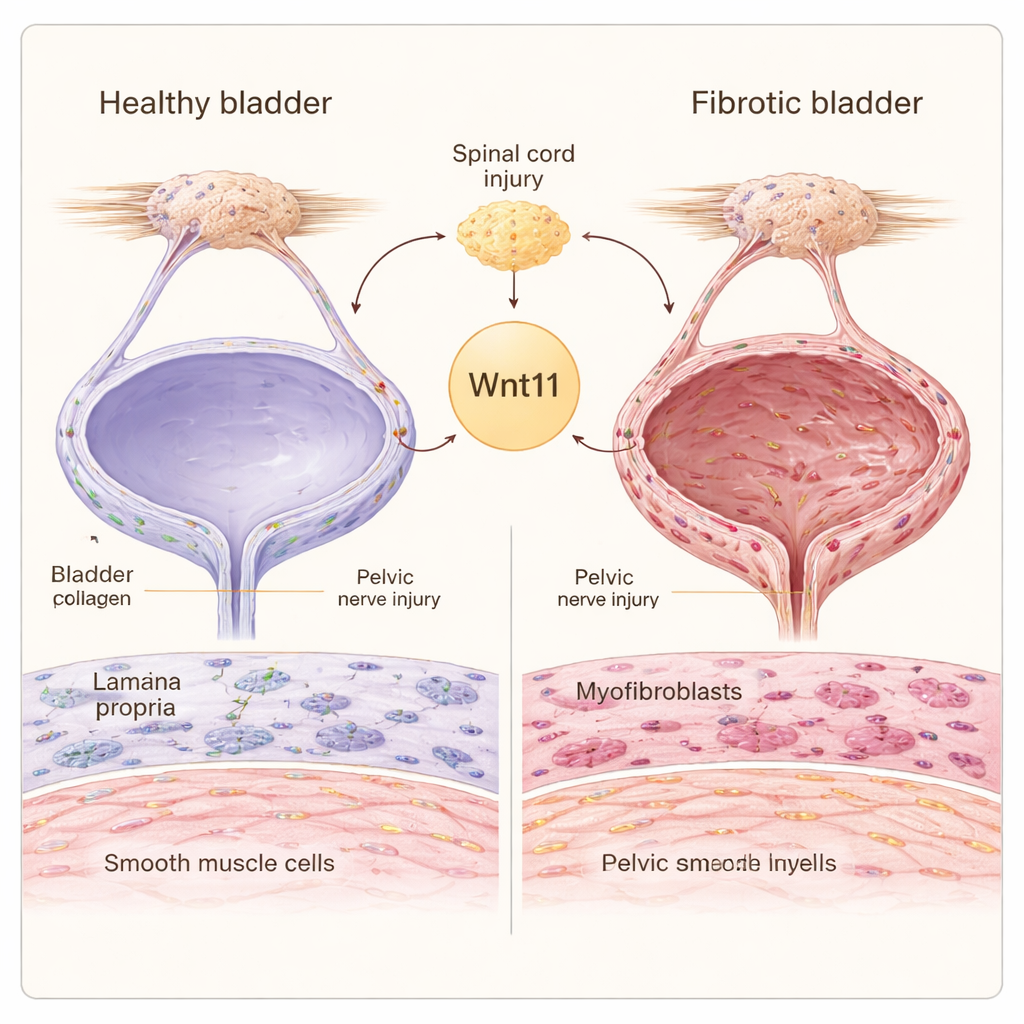
Скрытая цена повреждения нервов
Когда повреждаются нервы, обслуживающие мочевой пузырь, будь то в спинном мозге или вблизи таза, орган вынужден работать сильнее, чтобы справляться с мочой. Стенка пузыря содержит два основных типа опорных клеток: фибробласты, которые синтезируют матрикс вокруг клеток, и гладкомышечные клетки, которые сокращаются, чтобы выталкивать мочу. При нейрогенном пузыре фибробласты могут переходить в высокоактивные «миофибробласты», интенсивно продуцирующие коллаген, а гладкомышечные клетки переключаются из тонкого сократительного состояния в более объёмное, синтетическое. В совокупности эти изменения формируют жёсткую рубцовую ткань, уменьшающую растяжимость и способность пузыря опорожняться.
Сигнальная молекула выходит на первый план
Исследователи сосредоточились на семействе белков коммуникации между клетками — лигандах Wnt, известных регуляцией роста тканей и формированием рубцов в других органах. При скрининге пузырей крыс с повреждением нервов они обнаружили, что один из членов семейства, Wnt11, стабильно и значительно повышен в фиброзных пузырях, вызванных как травмой спинного мозга, так и ущемлением тазовых нервов. Уровни Wnt11 возросли и в фибробластах, и в гладкомышечных клетках, а количество Wnt11 коррелировало с тяжестью дисфункции пузыря. Когда нормальные клетки пузыря в культуре подвергали действию другого профиброгенного фактора, TGF-β1, они также усиливали выработку Wnt11, что указывает на подкрепляющий цикл между этими двумя сигналами.
От химического послания к стойкому рубцу
Чтобы проверить, является ли Wnt11 просто наблюдателем или активным драйвером процесса, команда добавляла экзогенный белок Wnt11 крысам с повреждением нервов и одновременно блокировала секрецию Wnt с помощью препарата LGK974. Дополнительный Wnt11 увеличивал размер пузырей, ухудшал показатели давления при наполнении и опорожнении, утолщал мышечный слой и усиливал отложение коллагена. Блокада секреции Wnt приводила к обратным эффектам: облегчению мочевых нарушений и снижению рубцевания. В изолированных клетках Wnt11 стимулировал переход фибробластов в миофибробласты и смещал гладкомышечные клетки в синтетический, способствующий фиброзу фенотип. Заглушение гена Wnt11 само по себе ослабляло эти изменения, ясно показывая, что Wnt11 является центральным ускорителем ремоделирования пузыря.
Как клетки «расшифровывают" сигнал фиброза
Углубляясь, исследование проследило путь от Wnt11 на поверхности клетки до изменений экспрессии генов в ядре. Было показано, что Wnt11 связывается с рецептором Vangl2 на фибробластах и гладкомышечных клетках пузыря. Это взаимодействие не использовало классический Wnt‑маршрут с участием β‑катенина; вместо этого активировался альтернативный каскад, называемый путем планарной клеточной полярности (PCP). Wnt11 и Vangl2 привлекают адаптерный белок DVL2, который затем включает фермент JNK. JNK, в свою очередь, активирует транскрипционные факторы c‑JUN и NFAT5, которые перемещаются в ядро и способствуют включению профибротических генов. Путь TGF‑β1, известный драйвер рубцевания, физически и функционально сходится с этим маршрутом Wnt11–Vangl2–JNK, так что два сигнала усиливают друг друга как на мембране клетки, так и в ядре.
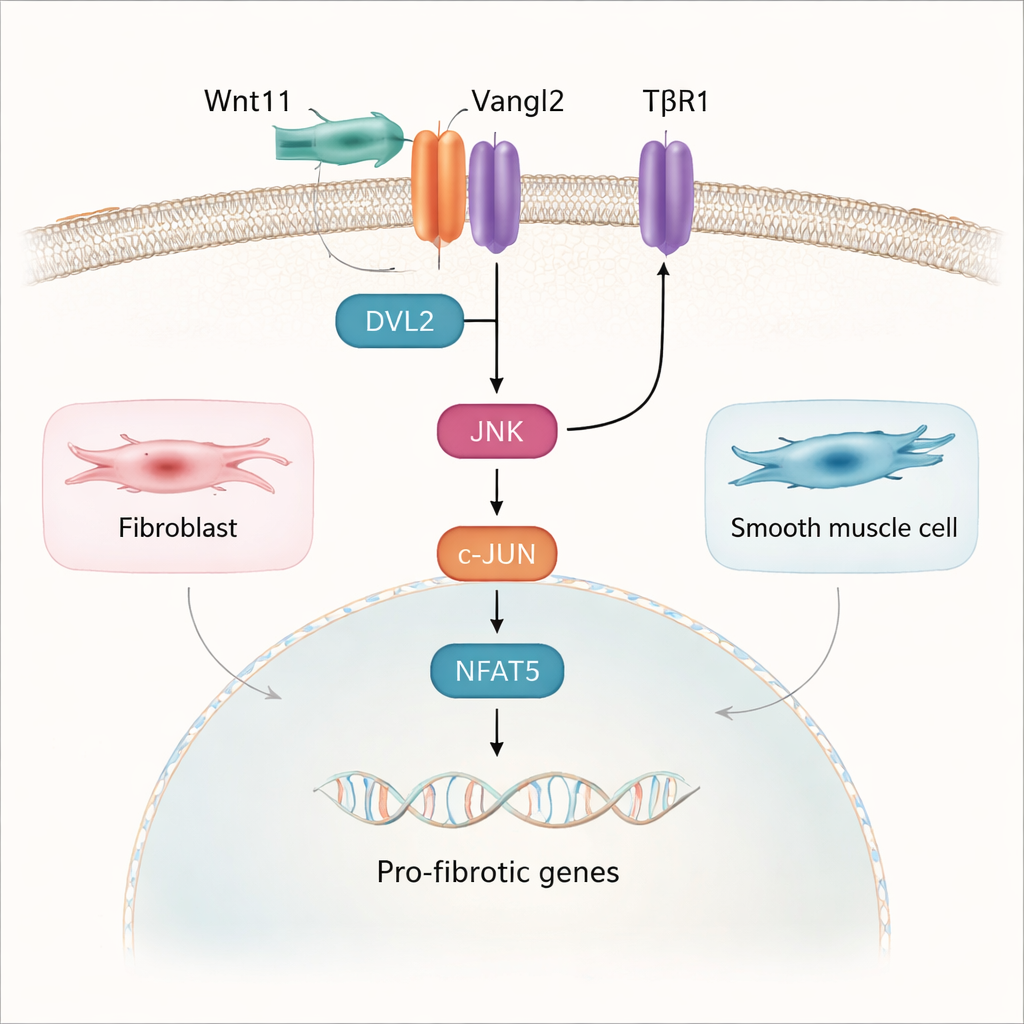
К более мягким и здоровым пузырям
Поскольку Wnt11 и TGF‑β1 работают совместно, чтобы уплотнять стенку пузыря, команда протестировала препараты, блокирующие ключевые звенья обоих путей. У крыс с нейрогенным пузырём комбинированное ингибирование рецептора TGF‑β (TβR1) и фермента JNK дало наилучшие результаты: меньшие по объёму пузыри, тоньше мышечные слои, меньше коллагена и улучшение функций хранения и выделения мочи по сравнению с монотерапией. Для неспециалиста главный вывод таков: сигнал, индуцируемый повреждением нервов — Wnt11 — способствует превращению обычных опорных и мышечных клеток в клетки, формирующие рубец. Прерывание этого сигнала, особенно в сочетании с классическими блокаторами TGF‑β, может лечь в основу будущих методов лечения, нацеленных не только на облегчение симптомов, но и на сохранение структуры и функции пузыря у людей с нейрогенным пузырём.
Цитирование: Ge, Q., Zhang, J., Fan, Z. et al. Wnt11 mediates fibroblast–smooth muscle cell interaction to promote neurogenic bladder fibrosis in rats. Commun Biol 9, 194 (2026). https://doi.org/10.1038/s42003-026-09647-2
Ключевые слова: нейрогенный пузырь, фиброз, Wnt11, гладкомышечные клетки, сигналы TGF-β