Clear Sky Science · ru
Параллельные пути, зависящие от Tbr2, регулируют развитие различных подтипов ipRGC
Как наши глаза определяют время и форму
Помимо формирования изображений, глаза тихо поддерживают работу внутренних часов организма, регулируют величину зрачка и помогают ощущать общую яркость. Небольшая популяция особых ганглиозных клеток сетчатки, называемых intrinsically photosensitive retinal ganglion cells (ipRGCs) — внутриклеточно фоторецепторными ганглиозными клетками — выполняет большую часть этой работы. Они реагируют на свет с помощью пигмента меланопсина и посылают сигналы глубоко в мозг. В этом исследовании поставлен фундаментальный вопрос с важными последствиями: как одна ранняя популяция развивающихся нейронов раскалывается на несколько различных типов ipRGC, каждый из которых проводит отдельную функцию?
Один главный переключатель, множество светочувствительных типов клеток
В сетчатке мыши все шесть известных подтипов ipRGC происходят из ранней популяции ганглиозных клеток, в которых включается ген Tbr2. Этот ген действует как главный переключатель, запускающий программы, необходимые для образования ipRGC и поддержания активности гена меланопсина Opn4. Но один главный переключатель сам по себе не объясняет, как возникают шесть разных вариантов ipRGC с уникальной формой, световой ответностью и проекциями в мозг. Авторы провели секвенирование РНК развивающихся сетчаток мыши, чтобы найти гены, активность которых зависит от Tbr2. Среди небольшого набора кандидатов выделились два: Irx1 и Tbx20, известные регуляторы идентичности клеток в других частях тела. 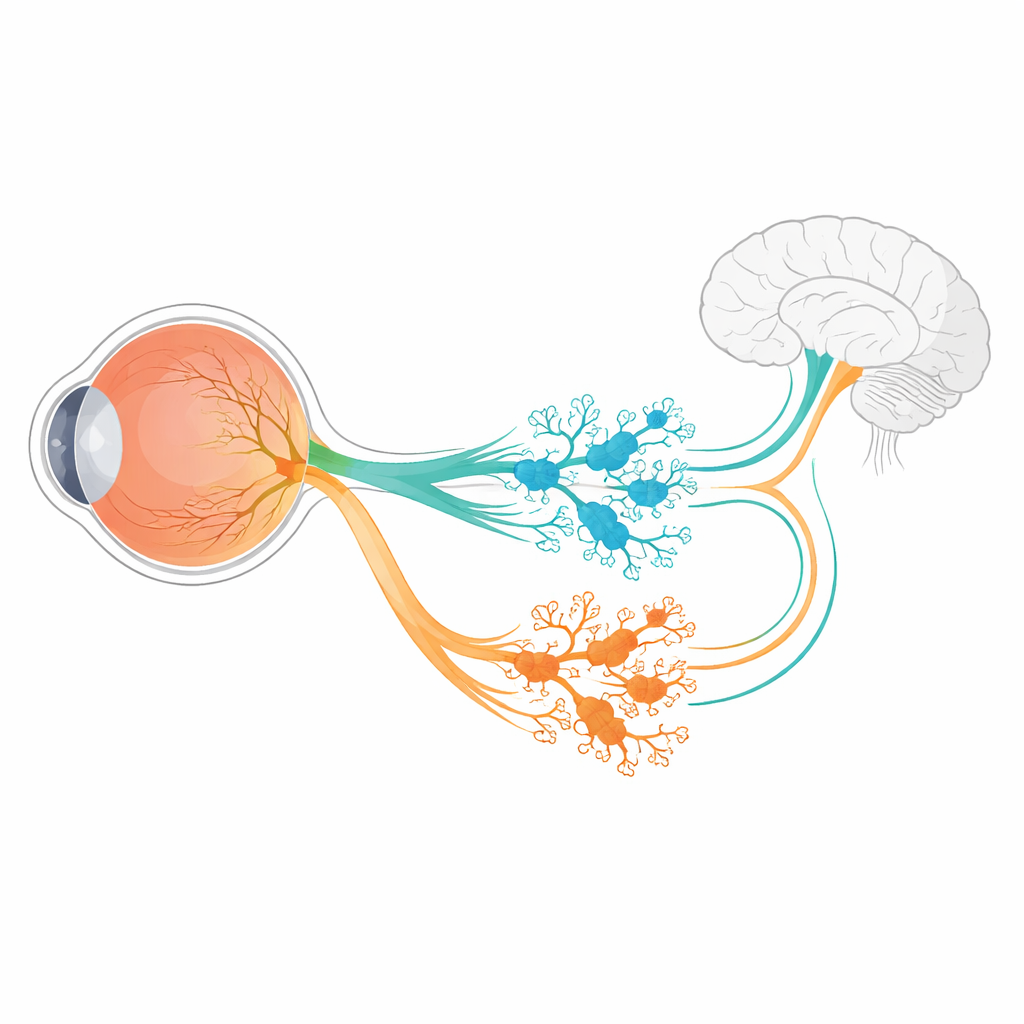
Два ответвления внутри сетчатки
Используя недавно созданные лини мышей, в которых клетки, продуцирующие Irx1 и Tbx20, помечены флуоресцентными или ферментными маркерами, исследователи проследили, где и когда включаются эти факторы. Они обнаружили, что Irx1 и Tbx20 появляются в перекрывающихся группах молодых ганглиозных клеток примерно в середине эмбриогенеза, но к взрослой стадии быстро разделяются на практически непересекающиеся популяции. Irx1 в основном присутствует в трех типах ipRGC, обозначенных M3, M4 и M5, тогда как Tbx20 сконцентрирован в клетках M1, M2 и M6, с лишь незначительным перекрытием в некоторых M3 и M5. Детализированная визуализация, электрические записи и трассировка проекций в мозг показали, что каждый фактор отмечает отдельный набор ipRGC с характерной dendritic-архитектурой, световыми ответами и схемами проекций в конкретные области мозга, участвующие в установке часов, рефлексах и обработке зрения.
Переключатели, которые настраивают светочувствительность и выживание клеток
Команда затем изучила, что происходит при удалении каждого фактора. Когда Irx1 был выведен из строя в развивающейся сетчатке, число и базовая структура Irx1-помеченных ipRGC в основном сохранялись, но уровни меланопсина у них резко снизились. Иными словами, Irx1 оказался необходим для полного включения светочувствительной программы Opn4 в клетках M3, M4 и M5, но не для их первоначального формирования. Tbx20 вел себя иначе. Удаление Tbx20 не только снижало экспрессию Opn4, но и практически вдвое сокращало число Tbx20-положительных ipRGC, а позднее уменьшало выживаемость этих клеток. Это указывает на то, что Tbx20 помогает как формировать, так и поддерживать определенные подтипы ipRGC, особенно M1, M2 и M6, одновременно поддерживая их меланопсин-зависимую светочувствительность. 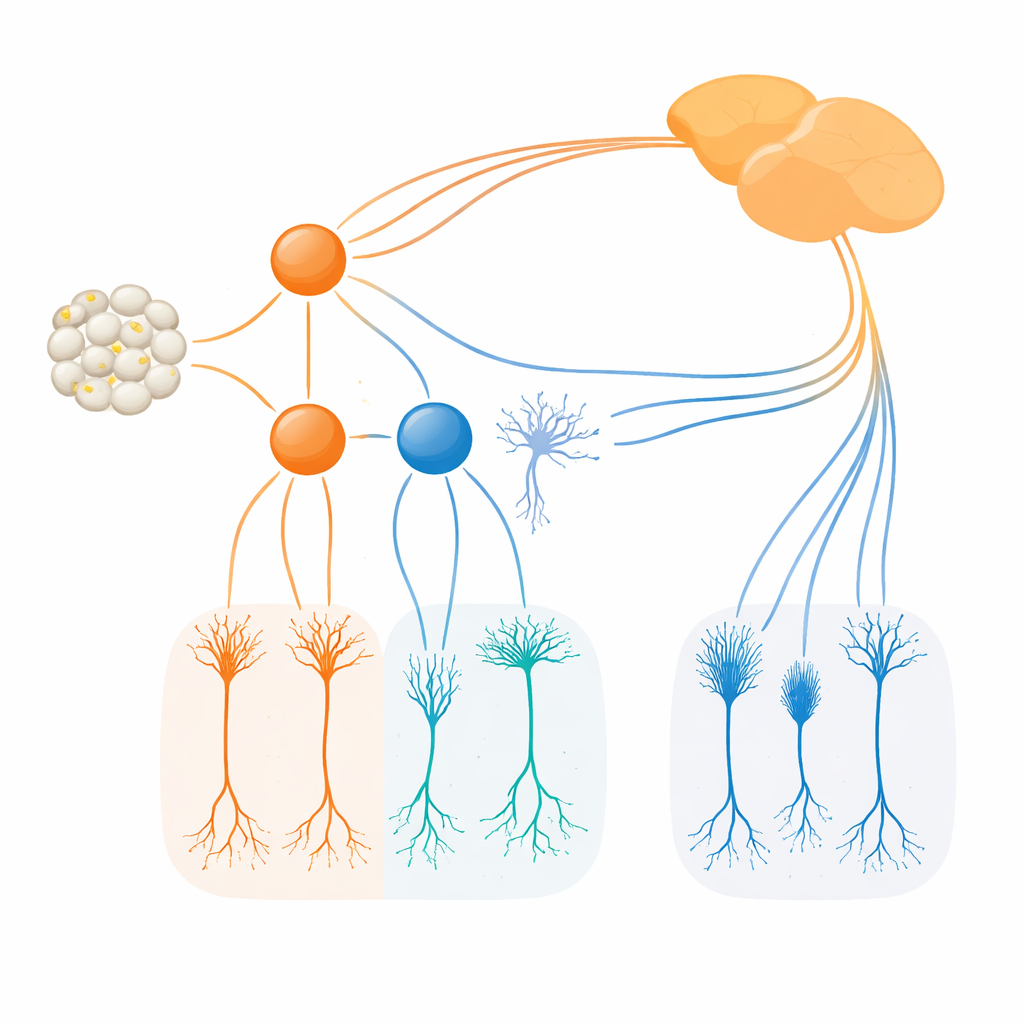
Временная развилка при разделении на разные семейства клеток
Кратковременно активируя генетические репортеры в точные эмбриональные дни, авторы могли «пометить временем» клетки, экспрессировавшие Irx1 или Tbx20, и проследить их судьбы до взрослого состояния. Эти эксперименты показали, что клетки, помеченные Tbx20, принимают окончательную ipRGC-идентичность немного раньше, чем помеченные Irx1, при этом большинство решений фиксируется незадолго до рождения. В течение короткого окна оба фактора могут одновременно экспрессироваться в некоторых клетках, и мыши с двойным нокаутом обоих генов демонстрировали гораздо более сильную потерю меланопсин-позитивных ipRGC, чем любой из одиночных мутантов. Это указывает на то, что два пути временно работают совместно, а затем расходятся, направляя разные подмножества ipRGC по отдельным траекториям развития.
Что это означает для понимания зрения и здоровья
Для неспециалиста основной вывод таков: один ранний ген, Tbr2, не действует в одиночку. Он запускает два параллельных контрольных пути — один сосредоточен вокруг Irx1, другой — вокруг Tbx20. Эти пути определяют, в какой тип ipRGC превратится молодая клетка, тонко настраивают силу ее световой чувствительности и определяют, будет ли она подключаться к областям мозга, отвечающим за настройку биологических часов, зрачковый рефлекс или другие визуальные функции. Работа проясняет схему проводки того, как строятся наши внутренние «светометры», и выделяет конкретные генетические этапы, которые могут участвовать при утрате или нарушении работы этих клеток, что имеет потенциальное значение для расстройств сна, сезонных изменений настроения и заболеваний, повреждающих сетчатку.
Цитирование: Kiyama, T., Chen, CK., Altay, H.Y. et al. Tbr2-dependent parallel pathways regulate the development of distinct ipRGC subtypes. Commun Biol 9, 347 (2026). https://doi.org/10.1038/s42003-026-09645-4
Ключевые слова: ганглиозные клетки сетчатки, меланопсин, нейронное развитие, циркадные ритмы, транскрипционные факторы