Clear Sky Science · ru
Структурный механизм блокирования ингибирующих рецепторов NK‑клеток анти‑MHC‑I антителом в противоопухолевом иммунитете
Активация «молчащих» киллеров организма
Наша иммунная система располагает мощными дозорными — клетками естественного киллерного ответа (NK), которые распознают и уничтожают раковые и вирус‑инфицированные клетки. Однако опухоли нередко учатся заглушать этих стражей. В этой работе на атомном уровне показано, как специально сконструированное антитело способно снять эту «кнопку выключения», пробудив NK‑клетки и заставив их эффективнее атаковать опухоль. Исследование сочетает передовые методы структурной биологии с опытами на мышах, демонстрируя, как одно антитело может дополнить существующие противораковые иммунотерапии.
Идентификационные метки иммунитета на наших клетках
Каждая клетка нашего организма выставляет на поверхности молекулярные «идентификационные метки» — молекулы MHC класса I. Эти метки помогают иммунной системе отличать нормальную ткань от опасных клеток, которые стали раковыми или инфицированными вирусами. NK‑клетки постоянно сканируют эти метки. Когда они распознают нормальные паттерны, ингибирующие рецепторы на NK‑клетках посылают сигнал «успокоиться», предотвращая атаку. Опухоли часто сохраняют эти метки видимыми и используют их как защитный щит: пока течёт ингибирующий сигнал, NK‑клетки сдерживаются и опухоль может расти.
Антитело, которое захватывает щит
Исследователи изучали моноклональное антитело под названием B1.23.2, которое прочно связывается со многими вариантами человеческих MHC класса I на опухолевых клетках. С помощью крио‑электронной микроскопии и рентгеновской кристаллографии они точно картировали, как это антитело размещается на поверхности MHC. B1.23.2 захватывает консервативный гребень молекулы MHC — α2‑спираль — не касаясь её лёгкой цепи и лишь слабо ощущая пептид, представленный молекулой. Это означает, что антитело может узнавать широкий набор человеческих молекул HLA‑A, ‑B и ‑C с очень высокой аффинностью, будучи относительно нечувствительным к конкретным коротким фрагментам белка, которые MHC показывает на своей поверхности.
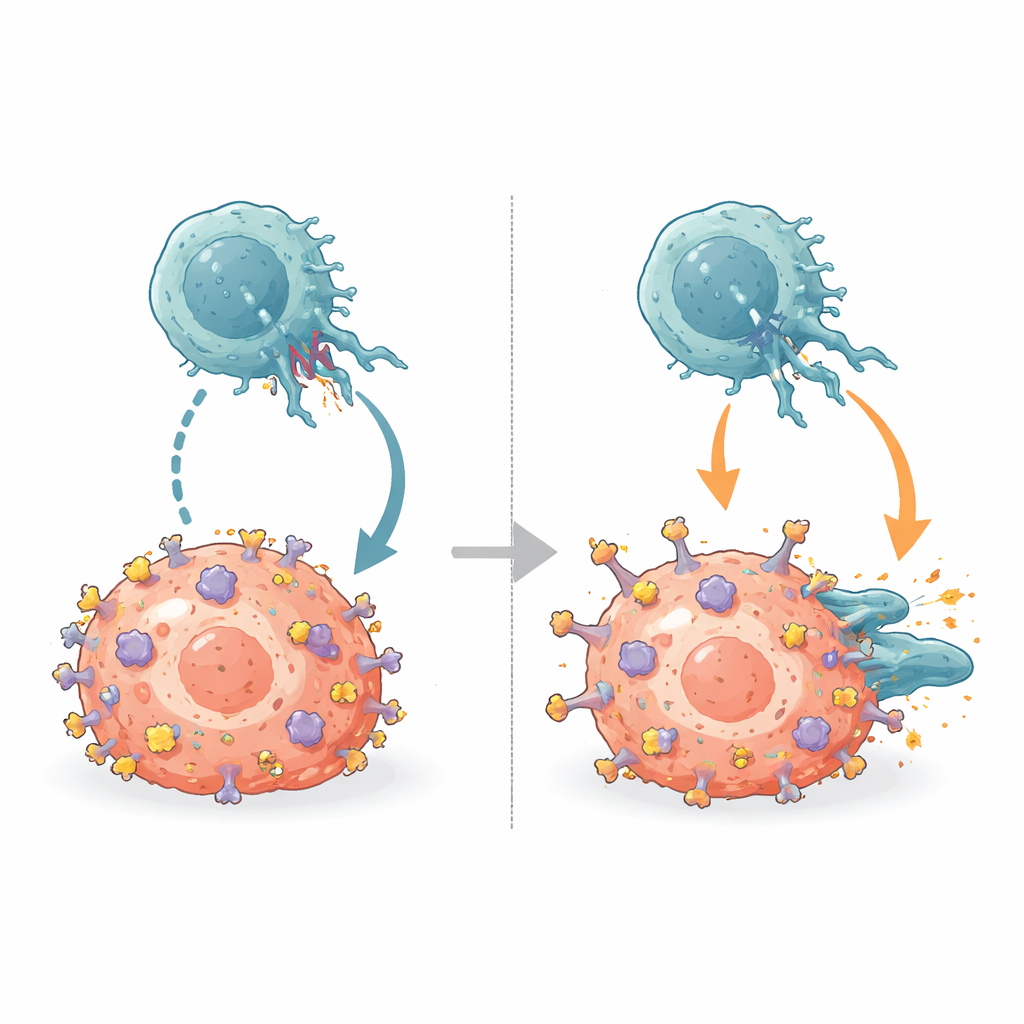
Перехватывая молекулярные тормоза
NK‑клетки несут ингибирующие рецепторы, называемые KIR, которые обычно «пристыковываются» к тому же α2‑гребню MHC. Совмещая новые структуры антитело–MHC с известными структурами KIR–MHC, команда показала, что B1.23.2 физически занимает ту самую область MHC, за которую цепляются KIR. Участки связывания антитела и следы контакта KIR настолько перекрываются, что оба не могут связаться одновременно. B1.23.2 также связывается с MHC сильнее, чем KIR, то есть выигрывает в этой молекулярной «перетяжке». В результате, когда антитело покрывает MHC на опухолевых клетках, KIR на NK‑клетках больше не могут передавать ингибирующие сигналы, что смещает баланс в сторону активации NK‑клеток.
Точная подгонка и широкий охват
Хотя B1.23.2 в основном нацелен на консервативную поверхность MHC, авторы обнаружили, что небольшие различия в пептиде, связанном с MHC, могут тонко регулировать силу связывания. Путём систематической замены одной аминокислотной позиции в пептиде они показали умеренные изменения аффинности — как правило, в пределах примерно десятикратного диапазона — без утраты общей узнаваемости. Они также исследовали, почему некоторые распространённые типы MHC, например HLA‑A*02:01, избегают связывания. Пересадив ключевые контактные остатки из реактивного варианта MHC в HLA‑A*02:01, команда создала версии, которые теперь распознаются антителом, точно подтвердив, какие позиции формируют критическую поверхность докинга. Эти наблюдения намекают, что в будущем можно будет спроектировать варианты антител для покрытия ещё большего числа типов MHC или для избирательного обхода некоторых из них.
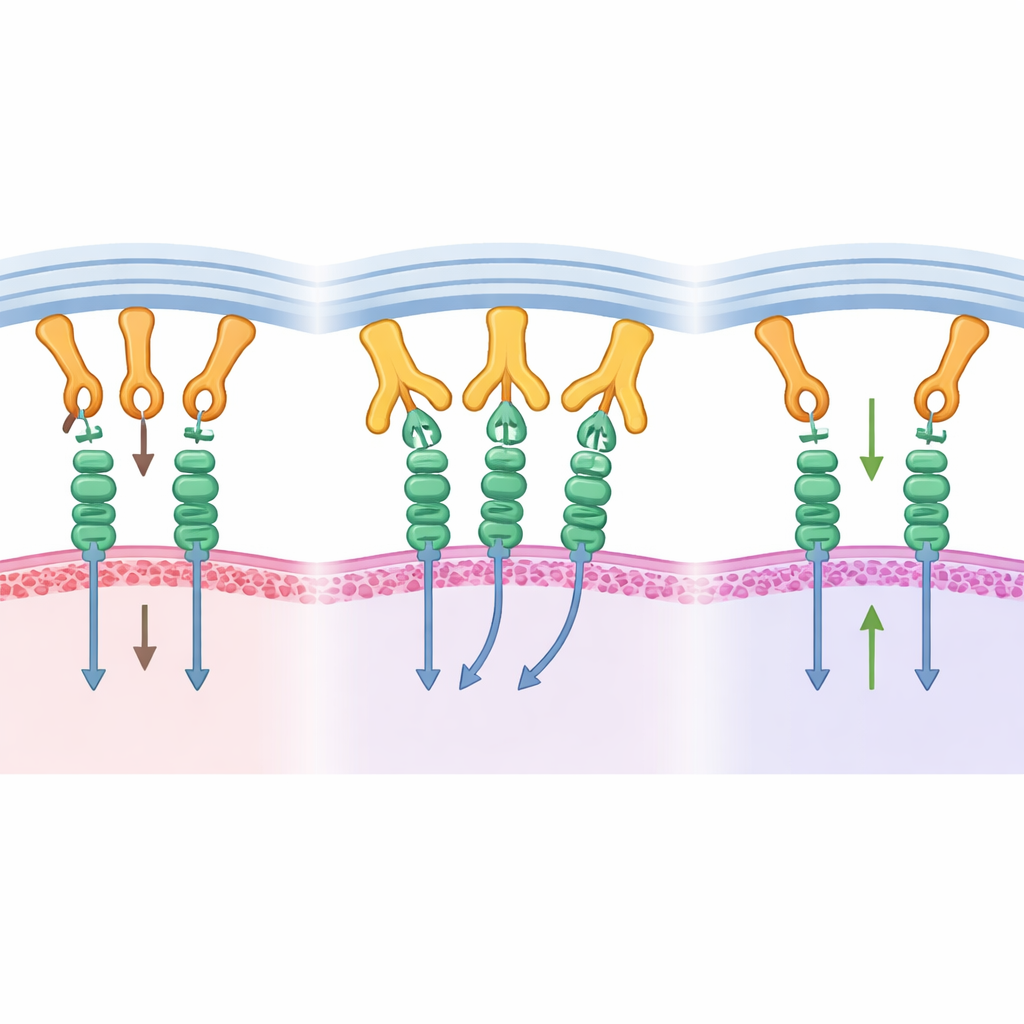
От структурного понимания к контролю над опухолью
Помогает ли это молекулярное блокирование в реальности бороться с опухолями? Чтобы проверить это, исследователи использовали олюднённую модель мыши с человеческой панкреатической опухолью. Они создали форму B1.23.2, неспособную сигнализировать через собственный Fc‑хвост, чтобы любые эффекты главным образом были следствием блокирования взаимодействия MHC–KIR. Когда мышам вводили антитело вместе с человеческими NK‑клетками, опухоли росли значительно медленнее. NK‑клетки проявляли повышенную пролиферацию, усиленную активность сигнальных и ростовых путей и большее производство воспалительных молекул, ассоциированных с убийством опухолевых клеток. Внутри опухолей NK‑клетки демонстрировали больше активирующих рецепторов — что согласуется с их освобождением от постоянного ингибирующего ввода.
Что это может значить для будущих противораковых терапий
Проще говоря, исследование показывает, как одно антитело может прокрасться между опухолевыми клетками и тормозами иммунной системы, прекращая сигнал «не атаковать», который обычно удерживает NK‑клетки в покое. Отрисовав взаимодействие с атомным разрешением и подтвердив его эффекты на животных, работа предлагает план для нового класса препаратов: антител, которые связывают «идентификационные метки» опухоли, а не сами иммунные рецепторы. Такие агенты могли бы сочетаться с существующими ингибиторами контрольных точек или клеточными терапиями, мобилизуя как NK‑клетки, так и T‑клетки и предоставляя иммунной системе дополнительное направление атаки против трудноизлечимых форм рака.
Цитирование: Jiang, J., Panda, A.K., Natarajan, K. et al. Structural mechanism of anti-MHC-I antibody blocking of inhibitory NK cell receptors in tumor immunity. Commun Biol 9, 350 (2026). https://doi.org/10.1038/s42003-026-09641-8
Ключевые слова: клетки‑естественные киллеры, МНС класс I, иммунотерапия рака, моноклональные антитела, ингибирующие рецепторы