Clear Sky Science · ru
LukS-PV, нацеленный на C5aR, ингибирует ЭМТ при гепатоцеллюлярной карциноме через ось BCL6/HDAC6/HSPD1
Преобразование бактериального оружия в средство против рака
Гепатоцеллюлярная карцинома, самая распространённая форма рака печени, часто смертельна именно из‑за способности опухоли распространяться из печени в другие органы. В этой статье рассматривается неожиданный союзник в борьбе с этим распространением: белок LukS-PV, изначально являющийся компонентом токсина бактерии Staphylococcus aureus. Исследователи показывают, как этот белок связывается с определённым рецептором на клетках рака печени и, вместо того чтобы повреждать нормальную ткань, блокирует ключевые этапы, позволяющие клеткам опухоли отрыватьcя, перемещаться и образовывать новые очаги.
Почему важно остановить изменяющиеся по форме раковые клетки
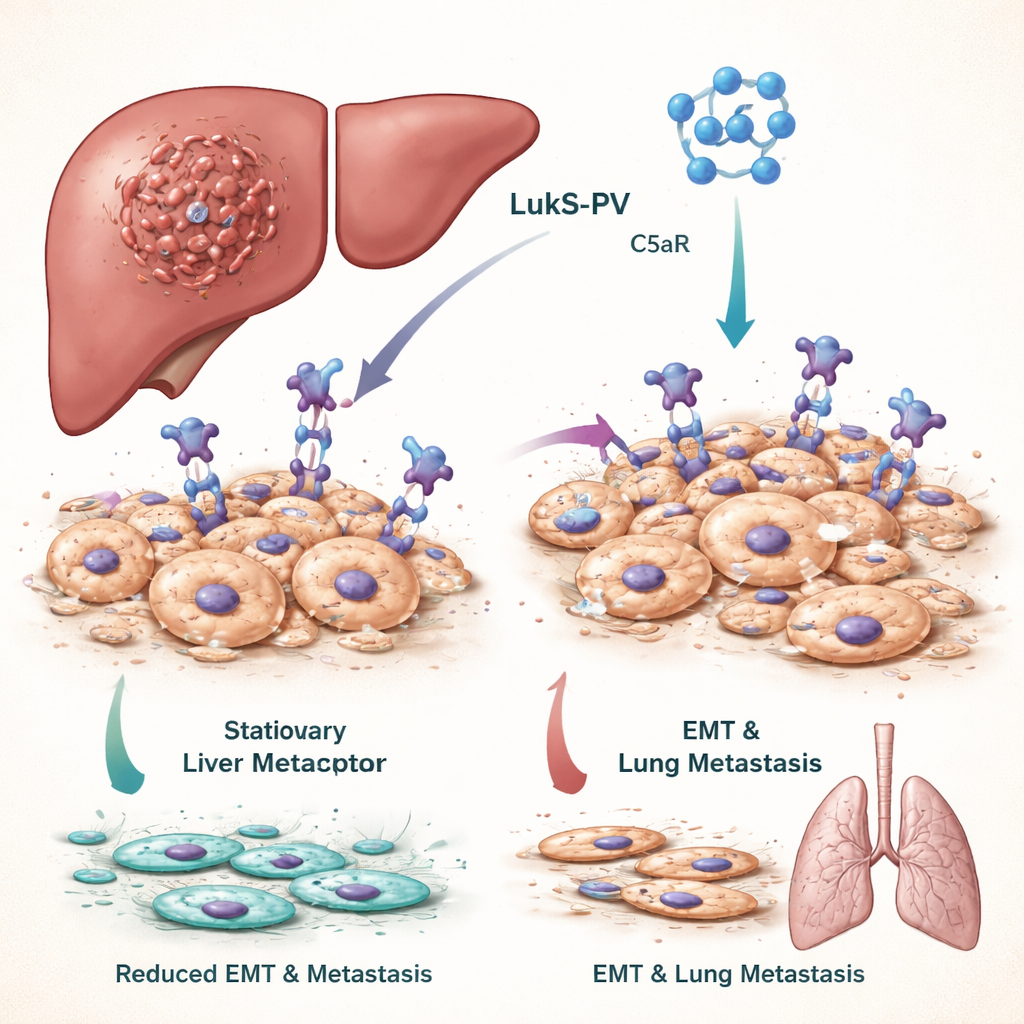
Для того чтобы рак печени дал метастазы, клетки опухоли должны пройти драматическое изменение формы и поведения, называемое эпителиально‑мезенхимальным переходом (ЭМТ). При ЭМТ тесно прилегающие клетки, которые обычно остаются на месте, становятся более гибкими, подвижными и инвазивными, что позволяет им проникать в кровеносные сосуды и засевать отдалённые органы, такие как лёгкие. У пациентов, чьи опухоли демонстрируют выраженную активность ЭМТ, прогноз обычно хуже. Команда сосредоточилась на сигнальном пути, опосредуемом молекулой C5a и её рецептором C5aR, который часто избыточно экспрессирован на многих опухолевых клетках и известен как фактор, стимулирующий ЭМТ и метастазирование.
Компонент токсина, нацеленный на опухолевый сигнал
Panton–Valentine лейкоцидин, токсин Staphylococcus aureus, содержит компонент LukS-PV, который естественным образом распознаёт и связывается с C5aR. Предыдущие работы авторов показали, что рекомбинантная, неспособная образовывать поры версия LukS-PV может подавлять рост нескольких типов рака без явно выраженной токсичности у животных. В этом исследовании линии клеток рака печени обрабатывали LukS-PV и наблюдали снижение их миграции и инвазии. Молекулярные тесты показали повышение маркёров закреплённого, «пристойного» эпителиального фенотипа и снижение маркёров агрессивных, подвижных клеток. У мышей, которым вводили клетки рака печени, лечение LukS-PV привело к значительно меньшему числу опухолевых узелков в лёгких, что указывает на снижение метастазирования.
Блокирование каскада внутри опухолевых клеток
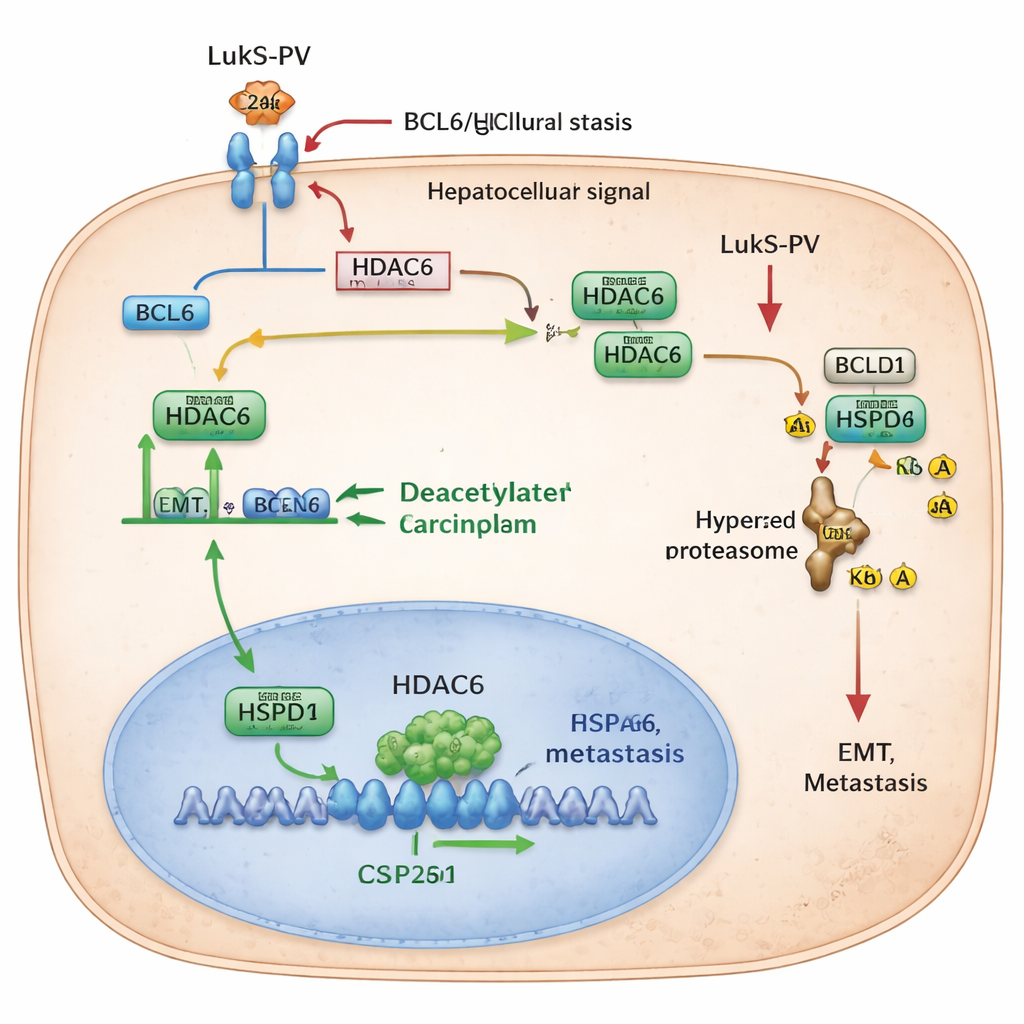
Углублённый анализ выявил цепочку регуляторных белков внутри раковых клеток, которую нарушает LukS-PV. Сначала LukS-PV связывается с C5aR на поверхности клетки и фактически блокирует прогеметастатический сигнал от C5a. Ослабление сигнального потока через C5aR понижает уровень белка BCL6, транскрипционного фактора, который обычно активирует определённые гены в ядре. Одной из мишеней BCL6 является HDAC6, фермент, удаляющий ацетильные группы с других белков. При высокой экспрессии BCL6 повышается уровень HDAC6, и клетка становится более предрасположенной к ЭМТ и миграции. Вмешательство LukS-PV в сигнализацию C5aR снижает BCL6, что, в свою очередь, уменьшает продукцию HDAC6 и замедляет эту прогеметастатическую программу.
Метка для разрушения шаперона
Далее группа выявила ключевого партнёра HDAC6 — HSPD1, также известный как HSP60, шаперонный белок, помогающий другим белкам правильно сгибаться и оставаться стабильными. В раке печени уровни HSPD1 выше, чем в окружающей нормальной ткани, и коррелируют с худшей выживаемостью пациентов. Исследователи обнаружили, что HDAC6 физически взаимодействует с HSPD1 и снимает ацетильные метки с двух специфических позиций на нём. При удалении этих ацетильных групп HSPD1 становится более стабильным и поддерживает ЭМТ и метастазирование. Когда HDAC6 уменьшают — либо генетически, либо при помощи LukS-PV — HSPD1 становится более ацетилированным. Эта гиперацетилированная форма распознаётся протеасомной системой клетки, метится убиквитином и разрушается. С понижением уровней HSPD1 у раковых клеток уменьшается способность к миграции, инвазии и колонизации лёгких.
От сложных путей к простому выводу
Для неспециалиста суть в том, что авторы проследили эффект домино внутри клеток рака печени: рецептор на поверхности (C5aR) усиливает регуляторный белок (BCL6), который повышает уровень фермента (HDAC6), защищающего шаперон (HSPD1) от разрушения. В совокупности эти компоненты помогают клеткам опухоли менять форму, перемещаться и распространяться. LukS-PV, бактериальный белок, перепрофилированный в лаборатории, прерывает эту последовательность прямо на поверхности клетки, что в конечном счёте ведёт к разрушению HSPD1 и торможению метастазирования. Хотя работа остаётся на экспериментальной стадии, она указывает на то, что препараты, смоделированные по LukS-PV, или нацеленные на BCL6, HDAC6 или HSPD1, могут предложить новые подходы к предотвращению распространения опухолей печени и улучшению прогноза пациентов.
Цитирование: Ding, P., Shi, L., Xu, X. et al. LukS-PV targeting C5aR inhibits EMT in hepatocellular carcinoma via the BCL6/HDAC6/HSPD1 axis. Commun Biol 9, 314 (2026). https://doi.org/10.1038/s42003-026-09640-9
Ключевые слова: гепатоцеллюлярная карцинома, метастазирование, эпителиально-мезенхимальный переход, HDAC6, терапия бактериальными токсинами