Clear Sky Science · ru
Негативная регуляция пути NF-κB убиквитин-лигазой Nedd4-1(NE)
Почему важно выключать воспаление
Наша иммунная система полагается на быстрые вспышки воспаления для борьбы с инфекциями и заживления ран, но те же самые механизмы могут повреждать ткани и способствовать развитию рака, если остаются включёнными слишком долго. В этой статье рассматривается, как клетки человека и других приматов избегают этой опасности с помощью недавно охарактеризованного встроенного «тормоза», который успокаивает одну из центральных сигнализационных систем организма, когда её задача выполнена.
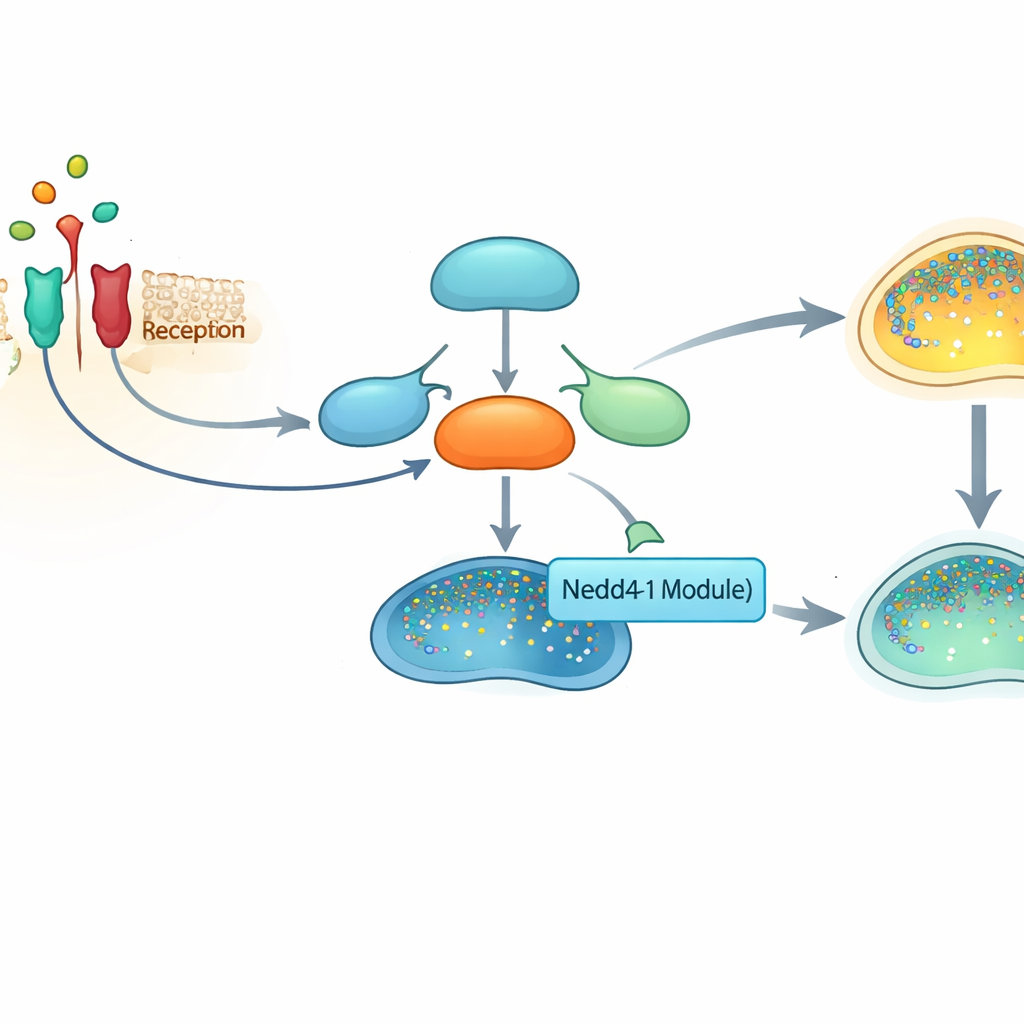
Центральный переключатель тревоги в наших клетках
В центре этой истории — NF-κB, семейство белков, действующее как главный переключатель для сотен генов, вовлечённых в воспаление, выживание клеток и иммунитет. Когда клетки ощущают стрессовые сигналы, такие как воспалительная молекула TNFα, цепочка событий освобождает NF-κB от его белковых «шаперов» в цитоплазме и позволяет ему переместиться в ядро, где он включает провоспалительные и про‑выживаемые гены. Поскольку этот путь настолько мощный, клетки должны тщательно регулировать и его активацию, и его остановку. Неспособность выключить его связана с хроническими воспалительными заболеваниями и многими видами рака.
Тормоз, встречающийся только у приматов
Исследователи сосредоточились на Nedd4-1, представителе большого семейства ферментов, которые помечают другие белки небольшой молекулой убиквитином. Эта метка часто обозначает белки для разрушения или перемещения внутри клетки, перестроивая сигнальные сети. Ранее обнаруженный сплайс‑вариант Nedd4-1, называемый Nedd4-1(NE), встречается только у приматов и несёт длинный дополнительный фрагмент на своём N‑конце, что изменяет его локализацию в клетке и спектр распознаваемых мишеней. В отличие от стандартной формы Nedd4-1, которая через других партнёров может усиливать активность NF‑κB, команда обнаружила, что Nedd4-1(NE) действует противоположно: он ослабляет сигнал NF‑κB, особенно при длительной экспозиции TNFα.
Два способа сдерживать NF-κB
Чтобы выяснить, как работает этот тормоз, авторы использовали методы проксимального меткирования и вытягивания белков, чтобы увидеть, какие молекулы физически ассоциируются с Nedd4-1(NE). Они идентифицировали ключевые компоненты пути NF‑κB, включая киназу IKKβ и прекурсорный белок NF‑κB1 (также называемый p105). Последующие эксперименты продемонстрировали, что Nedd4-1(NE) добавляет убиквитиновые метки на IKKβ, что ведёт к его деградации. При уменьшении уровня IKKβ его обычная мишень IκBα перестаёт эффективно фосфорилироваться и разрушаться. В результате IκBα остаётся более стабильным и удерживает активную субъединицу NF‑κB p50 в цитозоле, препятствуя её проникновению в ядро и включению воспалительных генов.
Передача «в тормоз» через адаптер
Nedd4-1(NE) также действует дальше по каскаду, ограничивая уровни самого NF‑κB1. Здесь фермент не работает в одиночку: он сотрудничает с другим убиквитин‑модулирующим белком под названием KPC1. KPC1 помогает обрабатывать прекурсор NF‑κB1 p105 в активную форму p50 и локализуется в органеллах, известных как поздние эндосомы, где также обнаруживается Nedd4-1(NE). Команда показала, что Nedd4-1(NE) может убиквитинировать KPC1, и что модифицированный KPC1 служит адаптером, привлекая NF‑κB1 к Nedd4-1(NE) на поздних эндосомах. Этот трёхкомпонентный комплекс способствует дестабилизации как p105, так и p50, вновь сокращая пул NF‑κB, способный достигнуть ядра.
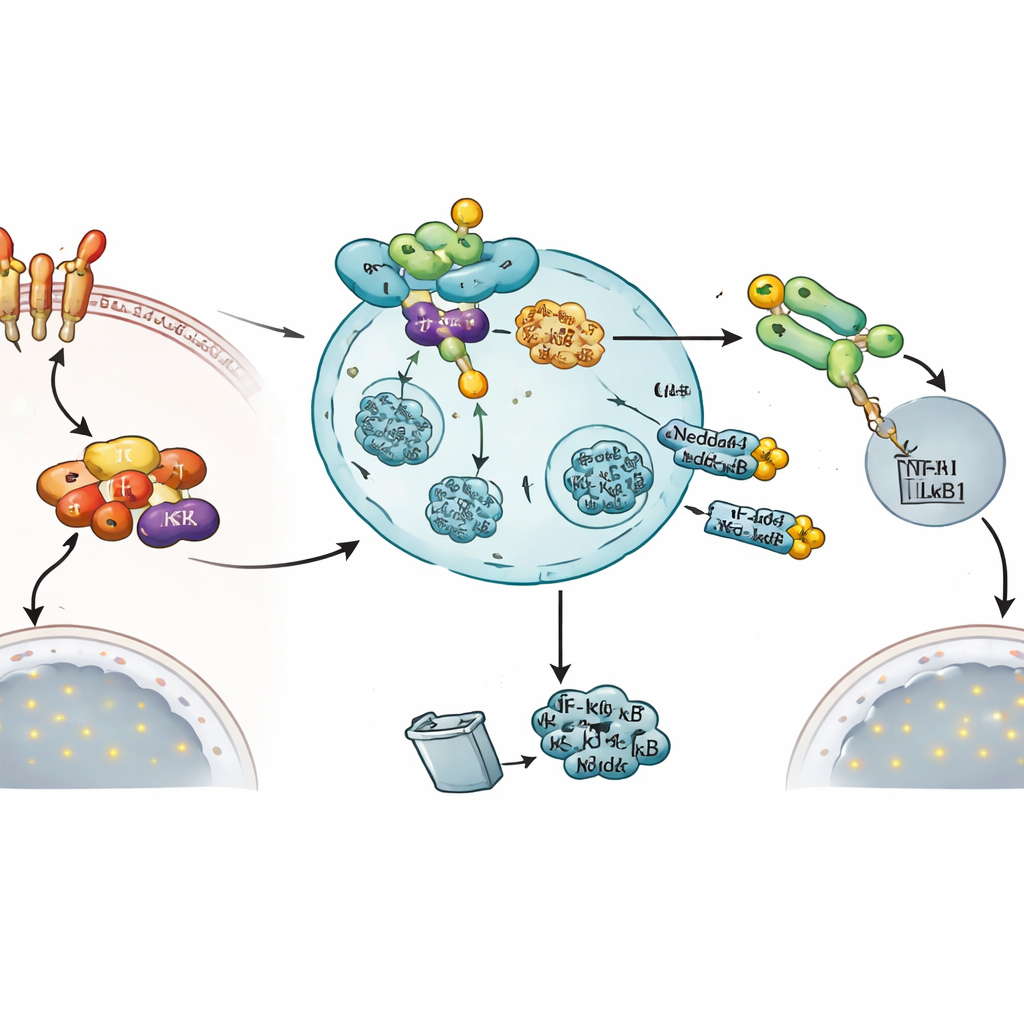
Встроенная петля обратной связи для завершения сигнала
Поразительно, что сам сигнал, активирующий NF‑κB, по-видимому, также индуцирует этот тормоз. При обработке клеток TNFα уровни мРНК Nedd4-1(NE) резко возрастали, тогда как стандартная форма Nedd4-1 не изменялась. Функциональные показатели поддерживали идею о том, что Nedd4-1(NE) выполняет роль клапана выключения: увеличение активного Nedd4-1(NE) снижало перемещение NF‑κB1 в ядро, уменьшало активность репортера, отзывчивого к NF‑κB, и снижало экспрессию регулируемого NF‑κB воспалительного гена TNFAIP3. Вместе эти данные описывают негативную петлю обратной связи, в которой активация пути NF‑κB в конечном счёте усиливает Nedd4-1(NE), который затем нацелен на два критических узла — IKKβ и NF‑κB1 — чтобы вернуть воспалительную реакцию к исходному уровню.
Что это значит для здоровья и болезней
Для широкой аудитории ключевая мысль в том, что наши клетки включают дополнительный, специфичный для приматов механизм безопасности, который не даёт воспалительным сигналам выйти из-под контроля. Селективно помечая и укорачивая ключевые компоненты системы NF‑κB, Nedd4-1(NE) помогает завершить ответ на TNFα и может способствовать долгосрочному иммунному балансу. Понимание этого встроенного тормоза может открыть новые пути для лечения заболеваний, при которых NF‑κB хронически гиперактивен, таких как аутоиммунные расстройства и некоторые виды рака, предлагая способы имитировать или усиливать этот природный процесс выключения.
Цитирование: Persaud, A., Kefalas, G., Shteiman, A. et al. Negative regulation of the NF-κB pathway by the ubiquitin ligase Nedd4-1(NE). Commun Biol 9, 374 (2026). https://doi.org/10.1038/s42003-026-09634-7
Ключевые слова: сигнализация NF-kB, воспаление, убиквитин-лигаза, Nedd4-1(NE), TNF альфа