Clear Sky Science · ru
Notch3 регулирует фенотипическую пластичность перицитов при колоректальном раке
Почему сосуды вокруг опухолей имеют значение
Колоректальный рак — один из наиболее распространённых и смертоносных видов рака в мире, однако большинство терапий нацелено непосредственно на опухолевые клетки и часто упускает из виду окружающую поддержку, которая помогает опухолям развиваться. В этой работе внимание сосредоточено на менее изученной группе поддерживающих клеток — перицитах, которые обвивают мелкие кровеносные сосуды. Раскрывая, как сигнальный переключатель Notch3 изменяет поведение перицитов, авторы показывают, как кровоснабжение опухоли может смещаться в сторону либо проницаемых, хаотичных сосудов, благоприятных для рака, либо более нормальных сосудов, способных замедлять заболевание и улучшать лечение. 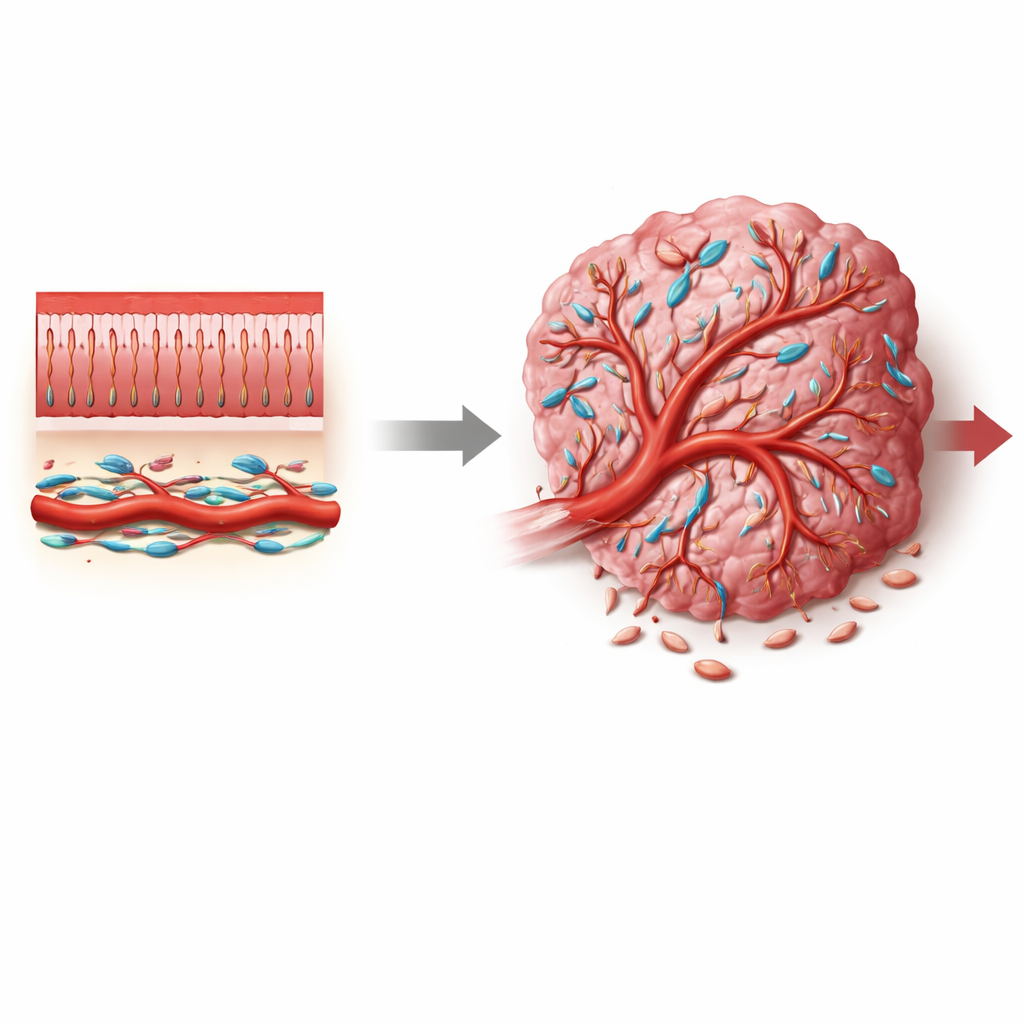
Скрытые помощники вокруг сосудов опухоли
Сосуды — это не просто полые трубки. В здоровых тканях мелкие сосуды плотно окружены перицитами — специализированными клетками, которые стабилизируют сосудистую стенку, контролируют кровоток и предотвращают утечку. В опухолях, однако, перициты часто выглядят и ведут себя иначе: они могут отрываться, размножаться или менять свою идентичность, внося вклад в аномальную, проницаемую сосудистую сеть, типичную для рака. В колоректальных опухолях, где микроокружение наполнено фибробластами, иммунными и сосудистыми клетками, оставалось неясным, откуда берутся опухоле-ассоциированные перициты, в какие состояния они переходят и какие молекулярные сигналы направляют их в пользу опухоли.
Отслеживание перицитов в процессе формирования опухоли
Чтобы проследить судьбу перицитов во времени, исследователи использовали мышиные модели колита‑ассоциированного колоректального рака, в которых можно генетически «маркировать» определённые типы клеток и наблюдать за их дальнейшей судьбой. Они показали, что перициты, обнаруженные в опухолях, в основном происходят от нормальных тканевых перицитов, которые расширяются и пролиферируют по мере развития рака, а не прибывают из отдалённых источников, таких как костный мозг. С помощью продвинутого секвенирования одиночных клеток (single-cell RNA-seq) они каталогизировали десятки тысяч стромальных клеток из мышиных опухолей и нормальной толстой кишки и обнаружили значительное обогащение перицитов в опухолевом микроокружении. Аналогичное расширение перицитов было найдено и в нескольких наборах данных по человеческому колоректальному раку, что подчёркивает, что это явление не ограничено только мышами.
Молекулярный переключатель, изменяющий поведение перицитов
Далее команда изучила, какие сигналы формируют поведение перицитов в опухолях, и обнаружила, что Notch3 — рецептор, позволяющий клеткам общаться с соседями — особенно активен в опухолевых перицитах. Вычислительный анализ клеточно‑клеточной коммуникации показал, что перициты и посылают, и воспринимают Notch‑связанные сигналы, особенно через партнёров на эндотелиальных клетках сосудов. Когда исследователи искусственно активировали Notch3 в перицитах, эти клетки больше пролиферировали, но экспрессировали меньше сократительных белков, обычно связанных со стабилизацией сосудов. Сосуды опухолей у таких мышей становились крупнее, более проницаемыми и выстланы большим числом пролиферирующих эндотелиальных клеток, что указывает на меньшую стабильность сосудистой сети. Напротив, удаление Notch3 снижало пролиферацию эндотелиальных клеток, уменьшало размер сосудов и снижало их проницаемость, что свидетельствует о сдвиге в сторону более нормализованной васкуляризации без драматического изменения раннего числа или размера опухолей. 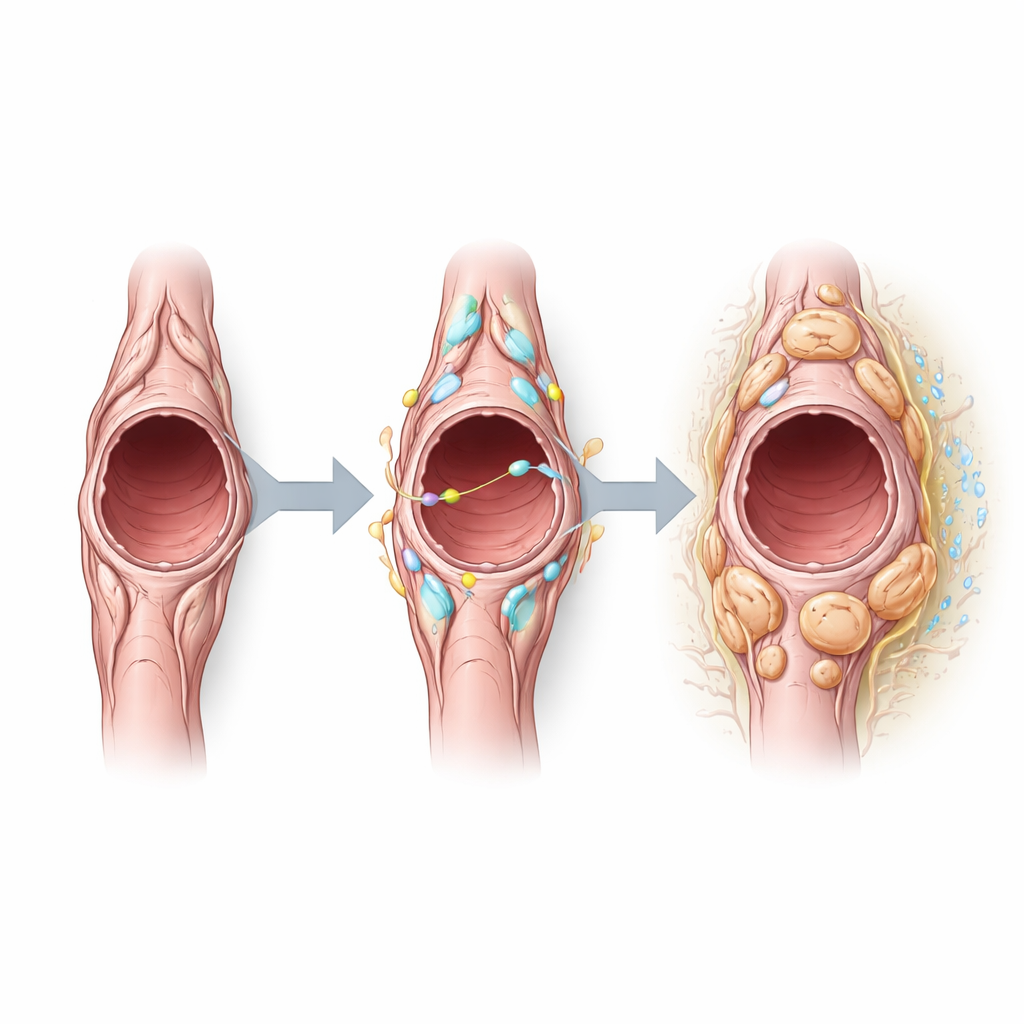
Многообразие перицитов внутри опухолей
Помимо простых включений и выключений, исследование показало, что опухолевые перициты существуют в нескольких отличительных состояниях. Некоторые подгруппы демонстрировали черты высококонтрактильных клеток, другие продуцировали большие объёмы внеклеточного матрикса, часть проявляла воспалительные свойства, а подмножество имело сигнатуры, обычно присущие эндотелиальным клеткам. Активность Notch3 была распределена неравномерно: она была обогащена в «синтетической» популяции перицитов, производящей матрикс, и низка в более контрактильном подтипе. Анализы траекторий предполагали, что перициты могут переходить из контрактильного состояния в синтетическое, пролиферирующее состояние по мере роста активности Notch3. При изучении данных по человеческому колоректальному раку исследователи обнаружили сопоставимый спектр состояний перицитов и вновь увидели повышенную активность гена‑мишени Notch3 в опухоле‑ассоциированных и пролиферирующих перицитах, что отражает результаты у мышей.
Преобразование сосудистого хаоса в терапевтическую возможность
В целом работа изображает Notch3 как ключевой регулятор, который настраивает идентичность перицитов и через них — структуру и функцию сосудов опухоли. Высокая активность Notch3 сдвигает перициты в пролиферирующее, менее контрактильное состояние, связанное с увеличенными, проницаемыми сосудами, которые способствуют прогрессированию опухоли. Низкая активность Notch3 ассоциируется с более контрактильными перицитами, спокойными эндотелиальными клетками и более нормализованной васкуляризацией, что может сдерживать рост опухоли и улучшать доставку лекарств. Прицельное вмешательство в Notch3 именно в перицитах в будущем может перенаправить сосуды опухоли из состояния хаоса в стабильное состояние, предлагая новый подход к лечению продвинутого колоректального рака в сочетании с существующими препаратами.
Цитирование: Chalkidi, N., Stavropoulou, A., Arvaniti, VZ. et al. Notch3 regulates pericyte phenotypic plasticity in colorectal cancer. Commun Biol 9, 343 (2026). https://doi.org/10.1038/s42003-026-09629-4
Ключевые слова: колоректальный рак, опухолевое микроокружение, перициты, сигнальный путь Notch3, сосуды опухоли