Clear Sky Science · ru
Эндотелиальная TRIM47 регулирует целостность гематоэнцефалического барьера и когнитивные функции через сигнальный путь KEAP1/NRF2 у мышей
Почему важно защищать мельчайшие сосуды мозга
Цереброваскулярное заболевание мелких сосудов — тихий нарушитель в мозге. Оно повреждает крошечные кровеносные сосуды, повышает риск инсульта и постепенно подтачивает память и мышление, при этом у врачей по-прежнему нет препаратов, направленных на коренные биологические причины болезни. В этом исследовании сосредоточились на одном белке — TRIM47, присутствующем в клетках, выстилающих сосуды мозга, чтобы задать простой, но важный вопрос: помогает ли он сохранять защитный гематоэнцефалический барьер и имеет ли это значение для когнитивных функций?
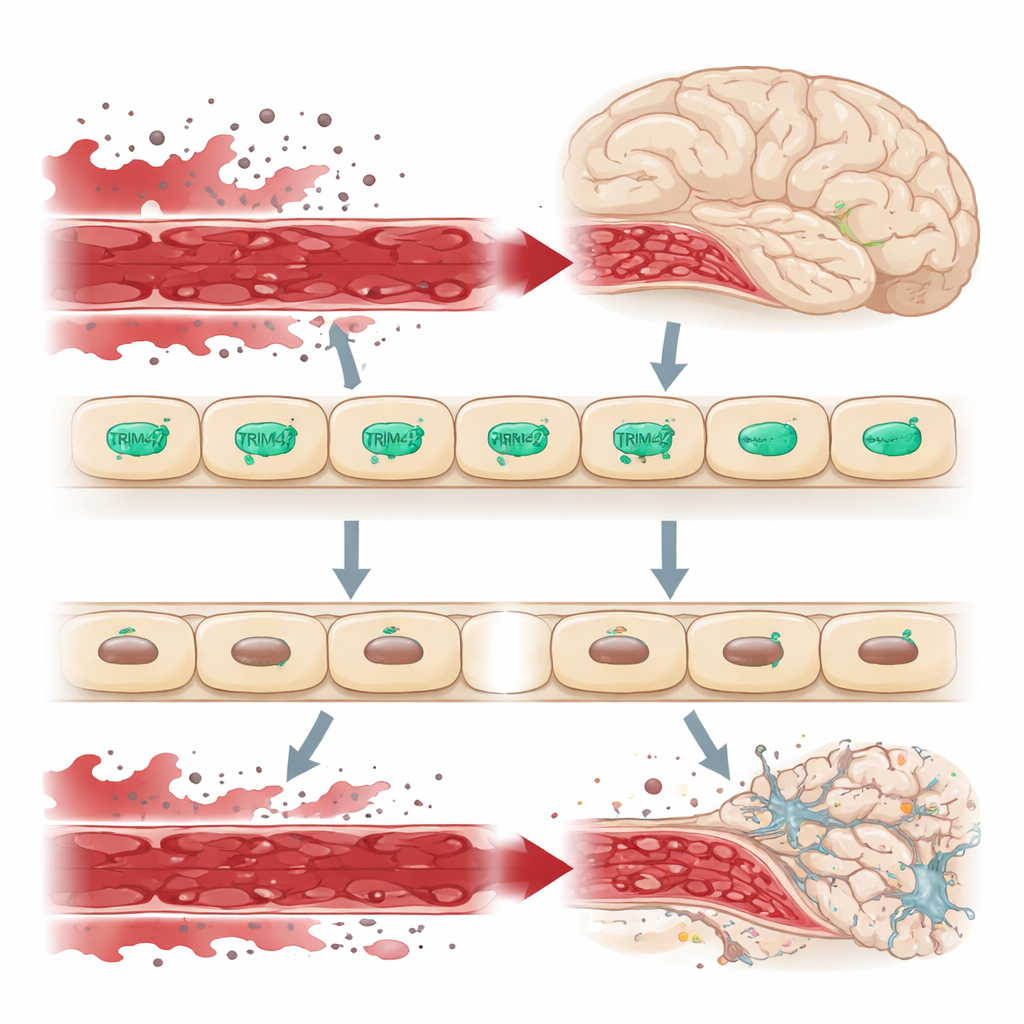
Пограничный страж у ворот мозга
Мозг защищён от остального кровообращения гематоэнцефалическим барьером — плотной оболочкой эндотелиальных клеток, которая строго контролирует, что может проникнуть в ткань мозга. Когда этот барьер становится проницаемым, вредные молекулы из крови просачиваются в мозг, нагружают нейроны и поддерживающие клетки и способствуют развитию состояний, таких как деменция. Генетические исследования больших когор людей указывали на участок ДНК с геном TRIM47 как на зону риска при заболеваниях мелких сосудов мозга. TRIM47 особенно активен в эндотелиальных клетках мозга, что наводит на мысль, что он может быть важным защитником этого барьера.
Как TRIM47 защищает клетки от окислительного стресса
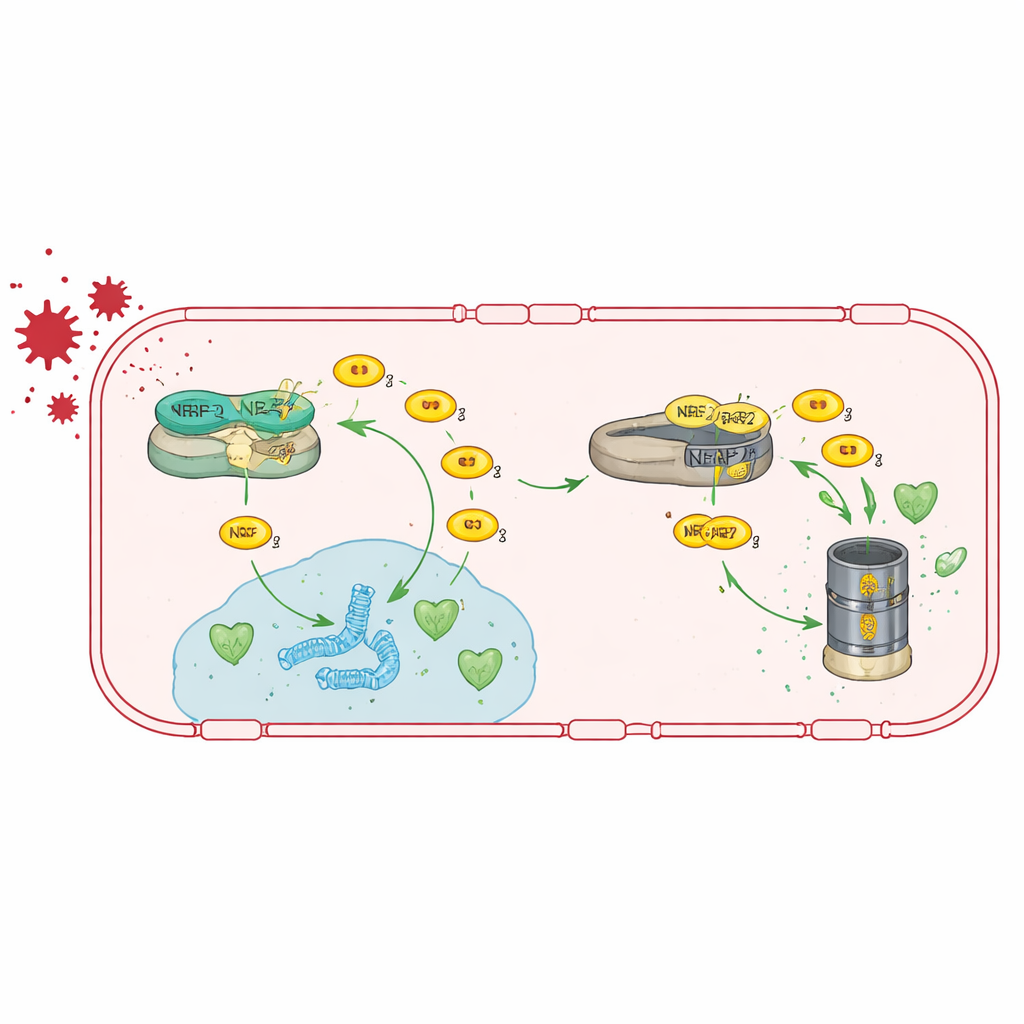
Авторы сначала изучили культивируемые человеческие эндотелиальные клетки мозга и снизили уровень TRIM47 с помощью РНК-интерференции. Это вызвало широкие изменения в активности генов, причём наиболее затронутой оказалась сеть, связанная с NRF2 — ключевым регулятором антиоксидантной защиты клетки. В норме NRF2 удерживается под контролем белка KEAP1, который направляет его на разрушение. Команда показала, что TRIM47 связывается с KEAP1 и помогает предотвратить разрушение NRF2. В присутствии TRIM47 NRF2 аккумулируется, перемещается в ядро и включает гены, детоксицирующие реактивные формы кислорода. При потере TRIM47 уровень NRF2 снижается, активность антиоксидантных генов падает, и эндотелиальные клетки становятся более уязвимыми к окислительному стрессу.
От протекающих сосудов к проблемам с памятью у мышей
Чтобы проследить этот механизм в живом мозге, исследователи создали мышей с полной потерей гена Trim47 и ещё одну линию, в которой Trim47 можно было удалять только в эндотелиальных клетках. Взрослые животные обеих моделей показали выраженные проблемы в пространственном обучении и памяти, проваливая такие тесты, как Y-лабиринт и водный лабиринт Морриса, несмотря на нормальную подвижность. При обследовании их мозга выяснилось, что гематоэнцефалический барьер стал проницаемым: небольшие флуоресцентные трассеры и кровяные белки выходили из сосудов в окружающую ткань. Ключевые «уплотняющие» белки, формирующие плотные и адгезионные контакты между эндотелиальными клетками, особенно Claudin-5 и Occludin, были снижены. Близлежащие астроциты, звёздообразные поддерживающие клетки, быстро реагирующие на повреждение, оказались активированы, хотя на этой стадии было мало признаков широкой воспалительной реакции или потери нейронов.
Включение антиоксидантного пути обратно
Поскольку TRIM47 действует главным образом через усиление активности NRF2, команда проверила, можно ли обойти его потерю, напрямую стимулируя NRF2. Они кормили мышей, лишённых Trim47, пищей, содержащей трет-бутилгидрохинон (tBHQ) — соединение, известное тем, что стабилизирует NRF2 и активирует его целевые гены. Лечение восстановило активность антиоксидантных генов в эндотелиальных клетках мозга, привело экспрессию генов плотных контактов ближе к норме и уменьшило утечку через гематоэнцефалический барьер. Поразительно, что это также нормализовало активацию астроцитов и вернуло животным результаты в тестах на память, что указывает на то, что усиление этого антиоксидантного пути может обратить как сосудистые, так и когнитивные нарушения, по крайней мере у мышей.
Подсказки из крови людей и дальнейшие шаги
Чтобы связать мышиные эксперименты с человеческой болезнью, исследователи проанализировали белки, связанные с путём NRF2, в образцах крови тысяч людей, у которых были сделаны МРТ головного мозга. Уровни нескольких белков, регулируемых NRF2, коррелировали с маркёрами малосудистых изменений на изображениях, такими как расширение периваскулярных пространств и изменения белого вещества. Это поддерживает идею о том, что нарушенная сигнализация TRIM47–NRF2 релевантна и у людей, а не только в экспериментах на животных, и что эти белки могут служить биомаркёрами тяжести или прогрессирования заболевания.
Что это значит для здоровья мозга
В совокупности работа изображает TRIM47 как молекулярного телохранителя, который помогает сосудистому эндотелию мозга выдерживать окислительное повреждение, стабилизируя антиоксидантную систему NRF2. Когда TRIM47 отсутствует или нарушен, гематоэнцефалический барьер ослабевает, накапливаются тонкие повреждения мозга, и память начинает ухудшаться. Реактивация пути NRF2 способна восстановить барьер и вернуть когнитивные функции у мышей, что выделяет эту сигнальную ось как перспективную терапевтическую цель при сосудистых формах деменции. Хотя сам tBHQ непригоден в качестве лекарства для людей, более безопасные соединения, усиливающие NRF2, или стратегии, имитирующие защитную роль TRIM47, возможно, однажды помогут сохранять здоровье мозга, укрепляя его самые мелкие и уязвимые сосуды.
Цитирование: Delobel, V., Grenier, C., Boulestreau, R. et al. Endothelial TRIM47 regulates blood-brain barrier integrity and cognition via the KEAP1/NRF2 signalling pathway in mice. Commun Biol 9, 399 (2026). https://doi.org/10.1038/s42003-026-09628-5
Ключевые слова: цереброваскулярное заболевание мелких сосудов, гематоэнцефалический барьер, TRIM47, путь NRF2, сосудистая деменция