Clear Sky Science · ru
Межсубъединичный путь необходим для энтропийно-опосредованного и отрицательного кооперативного связывания циклических нуклеотидов в канале HCN2
Как крошечный сердечный «пульсатор» улавливает химические сигналы
Каждый сердечный удар и многие ритмы мозга зависят от микроскопических каналов, которые открываются и закрываются в мембранах наших клеток. Эти каналы, называемые пейсмейкерными каналами HCN, управляются не только электрическим потенциалом, но и малыми сигнальными молекулами — циклическими нуклеотидами. В этом исследовании поставлен на вид простой на первый взгляд вопрос с далеко идущими последствиями: как эти крошечные молекулы координированно связываются с каналом HCN2 и как тонкие нарушения в этом процессе могут способствовать заболеваниям, таким как эпилепсия?
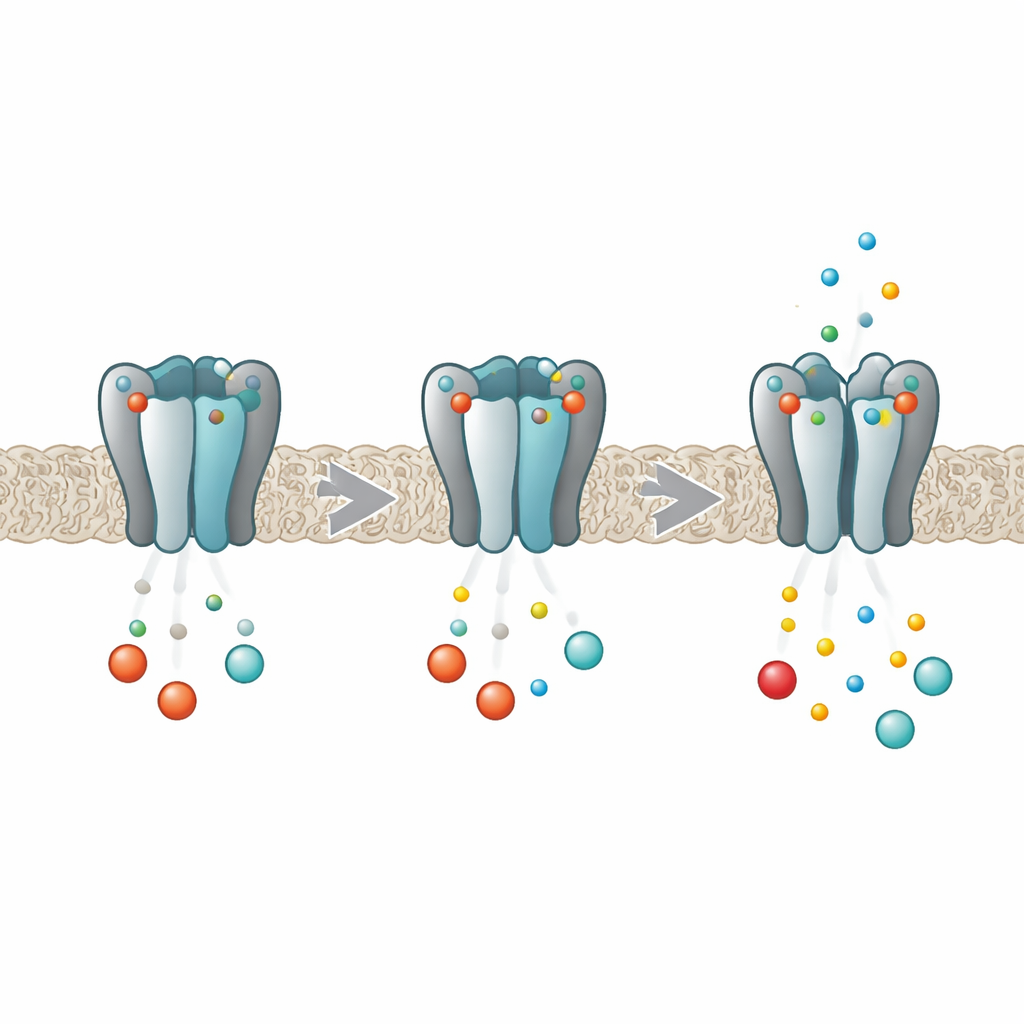
Молекулярный диммер для ритмов организма
Каналы HCN работают как регуляторы интенсивности электрической активности в клетках сердца и мозга. Каждый канал состоит из четырех одинаковых белковых субъединиц, которые вместе формируют центральный пор, через который проходят ионы. Внутри каждой субъединицы находится карман, способный захватывать циклические нуклеотиды, такие как cAMP и cGMP. Когда эти посредники связываются, им становится легче открыть пор, усиливая пейсмейкерный ток. Ранее было показано, что в варианте HCN2 связывание не происходит независимо в каждом кармане; наоборот, четыре сайта влияют друг на друга так, что первая молекула связывается легче, чем последующие — поведение, называемое отрицательной кооперативностью. Новая работа стремилась выяснить, как именно четыре субъединицы «общаются» друг с другом в этом процессе.
Субъединицы, чувствующие соседей
Исследователи сочетали компьютерное моделирование с лабораторными измерениями на изолированных фрагментах канала HCN2. С помощью длительных молекулярно-динамических симуляций они наблюдали, как хвостовая область канала — часть, содержащая карманы для циклических нуклеотидов и так называемый C-связывающий (C-linker), соединяющийся с пором — изгибается и колеблется при разном числе связанных cAMP или cGMP. Они обнаружили, что когда посредник «закреплялся» в одной субъединице, он не просто стабилизировал только эту субъединицу. Вместо этого он тонко менял стабильность соседей, иногда делая их более жесткими, иногда более гибкими, хотя общая форма белка практически не менялась. Эти соседские влияния зависели от числа занятых сайтов и их расположения по кольцу, что соответствовало ожиданиям при отрицательной кооперативности.
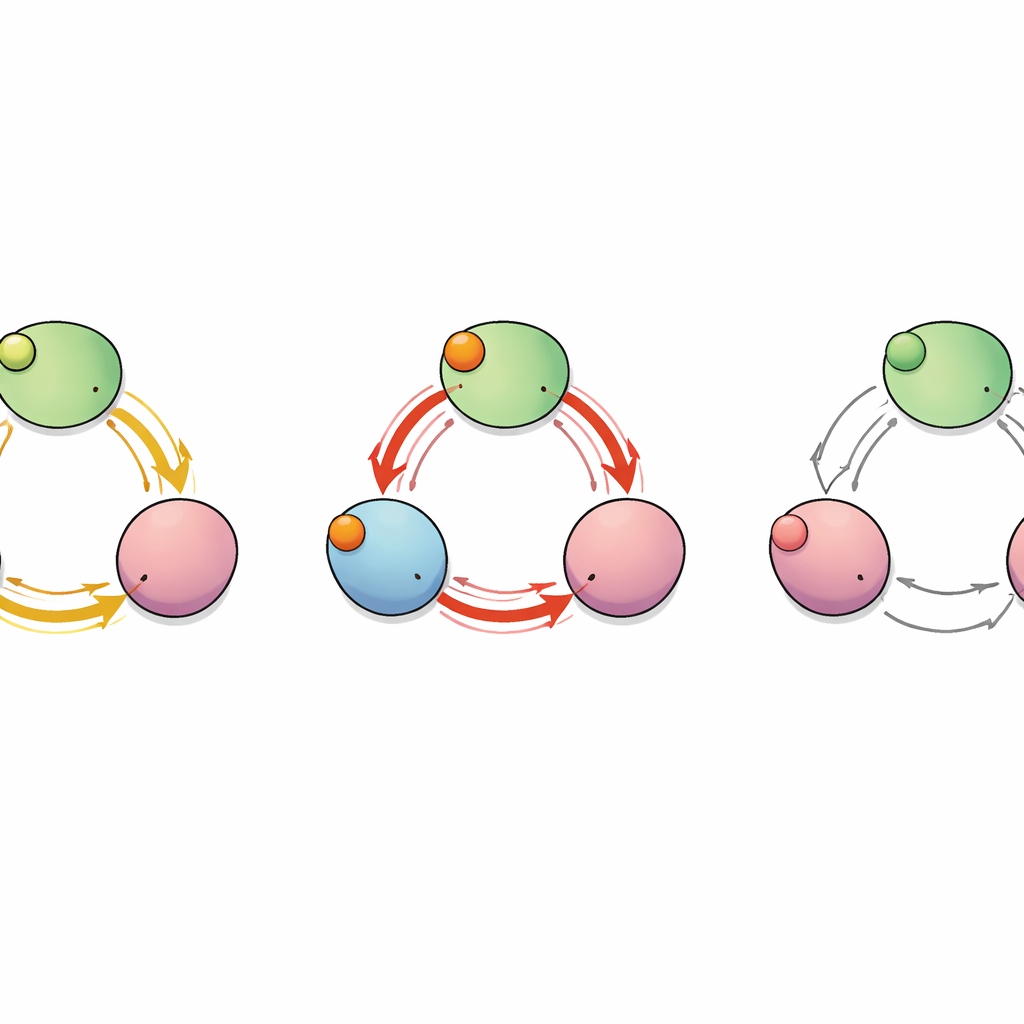
Скрытый путь между субъединицами
Чтобы сопоставить, как «сигнал» связывания проходит через белок, команда рассмотрела канал как сеть взаимодействующих аминокислот. Они вычисляли, какие остатки двигались согласованно в ходе симуляций, и использовали инструменты теории графов, чтобы определить самые короткие и наиболее эффективные пути коммуникации от карманов связывания до сегментов C-linker, контролирующих пор. Этот анализ выявил несколько возможных маршрутов, но два выделялись особенно: один оставался внутри одной субъединицы, другой перескакивал от одной субъединицы к соседней. По этому межсубъединичному маршруту одиночный остаток — глутаминовая кислота в положении 488 (E488) — выступал критическим узлом, через который проходило много кратчайших путей, что указывает на его роль ключевого ретранслятора при кооперативном связывании.
Мутации, прерывающие разговор
Авторы затем перешли к экспериментам с очищенными хвостовыми фрагментами канала, чтобы проверить важность этого пути. Они модифицировали E488 и находящийся на соседней субъединице тирозин 459 (Y459), куда этот путь приходит. С помощью динамического рассеяния света они подтвердили, что мутантные белки по-прежнему собираются в комплексы из четырех субъединиц, но перестали демонстрировать сильное вызываемое лигандом утомление/уплотнение между субъединицами, наблюдаемое в нормальном белке. Изотермическая калориметрия титрования, отслеживающая малые тепловые эффекты связывания, выявила ещё более крупное изменение: у дикого типа HCN2 наблюдались два различных события связывания — одна высокоаффинная ступень, в основном обусловленная увеличением энтропии (большей внутренней подвижностью), за которой следовали три низкоаффинных этапа. Напротив, мутанты в E488 или Y459 показали лишь один, умеренно аффинный режим связывания без благоприятного энтропийного вклада и потеряли характерную отрицательную кооперативность.
Зачем важны тонкие изменения энтропии
Собрав все эти данные воедино, исследование рисует картину канала HCN2 как динамического кольца из четырех субъединиц, связанных специфическими «путьами общения». Когда первый циклический нуклеотид связывается, он изменяет движения удаленных частей кольца через E488 и Y459, делая последующие события связывания менее благоприятными и настраивая отклик пора. Этот эффект определяется не крупными структурными перестройками, а смещениями внутренней гибкости — изменениями энтропии, невидимыми на статичных снимках, но критически важными для функции. Мутации, нарушающие ключевые остатки вдоль этого межсубъединичного пути, заглушают «разговор», устраняют отрицательную кооперативность и связаны с заболеваниями, такими как идиопатическая генерализованная эпилепсия. Для непрофессионального читателя вывод таков: жизненно важные переключатели в сердце и мозге полагаются на тонко скоординированные молекулярные «шепоты» между субъединицами белков, и понимание этих шепотов помогает объяснить как нормальные ритмы, так и то, что происходит при их нарушении.
Цитирование: Costa, F., Ng, L.C.T., Chow, S.S. et al. An inter-subunit path is required for entropically-driven and negatively cooperative binding of cyclic nucleotides in the HCN2 channel. Commun Biol 9, 362 (2026). https://doi.org/10.1038/s42003-026-09626-7
Ключевые слова: ионный канал HCN2, связывание циклических нуклеотидов, отрицательная кооперативность, аллостерическая коммуникация, мутация, связанная с эпилепсией