Clear Sky Science · ru
Малое молекула аллостерически активирует секрецию, зависящую от SecA
Перевод портового терминала бактерии в режим повышенной мощности
Бактерии выживают, постоянно экспортируя белки через крошечные шлюзы в своих мембранах. Эти экспорты помогают им строить клеточную стенку, выделять токсины и адаптироваться к стрессу — процессы, лежащие в основе многих инфекций. В этом исследовании описана малое соединение, названное HSI#6, которое ведёт себя необычно: вместо блокировки машинерии экспорта оно переключает её в гиперактивный, менее избирательный режим. Понимание механизма этого переключения может как открыть новые антимикробные стратегии, так и дать инструмент для биотехнологий, позволяющий по требованию усиливать секрецию белков.
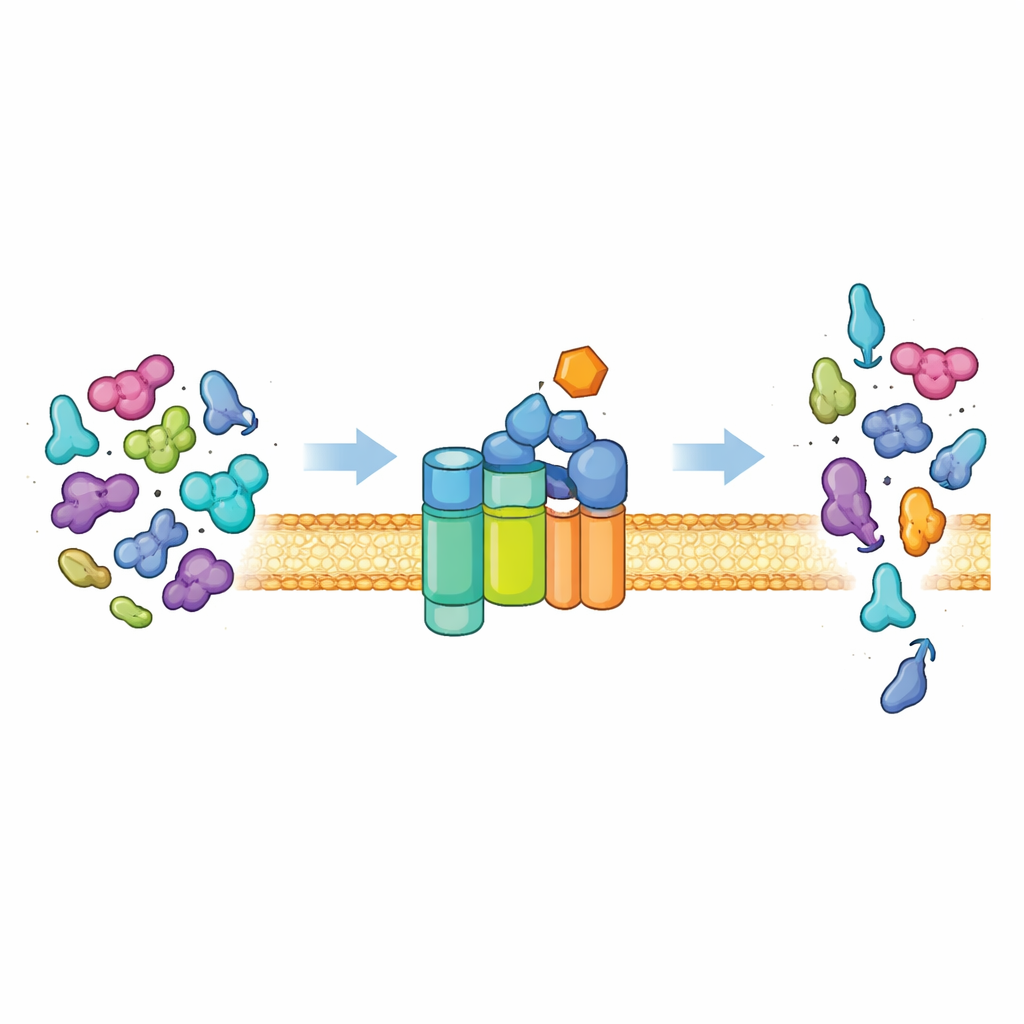
Выходные ворота клетки для белков
Большинство бактерий выводят белки из клетки с помощью универсального пути, известного как система Sec. В её основе лежит мембранный канал (SecYEG) и моторный белок (SecA), который расходует клеточное топливо (АТФ), проталкивая развернутые цепи белков через канал. В нормальных условиях эта система разборчива. Она преимущественно экспортирует «предбелки», несущие специальные адресные метки — сигнальные пептиды, а также дополнительные элементы в основной части молекулы. Эти признаки необходимы, чтобы переключить SecA из спокойного, низкоактивного состояния в мощный мотор. Только белки с правильной комбинацией сигналов могут разблокировать полную активность, обеспечивая экспорт нужного груза и удержание обычных цитоплазматических белков внутри.
Малое молекула, пробуждающая мотор
Исследователи обнаружили HSI#6 в скрининге соединений, нарушающих бактериальную секрецию белков и рост. Биохимические тесты показали, что HSI#6 непосредственно связывается с SecA с микромолярной аффинностью и меняет его эффективность использования АТФ. В растворе он заставляет SecA сильнее удерживать АТФ; когда SecA прикреплён к каналу, HSI#6 как улучшает связывание АТФ, так и ускоряет его гидролиз. Эта картина характерна для аллостерического активатора: молекулы, связывающейся в одной части белка и меняющей активность в другой, отдалённой области. В отличие от естественных белковых субстратов, HSI#6 не должен выступать в роли груза, чтобы стимулировать мотор — он просто настраивает внутреннюю динамику SecA так, что вся транслоказа становится каталитически подготовленной.
От избирательного фильтра к промискуитетной наномашине
После связывания HSI#6 система Sec уже не настаивает на обычных экспортных метках. В тестах в пробирке соединение примерно удваивало секрецию стандартной предбелковой мишени и делало комплекс более устойчивым к азиду натрия, известному ингибитору SecA. Более показательно то, что HSI#6 позволял штатной, «дикой» системе перемещать белки, полностью лишённые сигнальных пептидов, а также белки, которые обычно находятся в цитоплазме. В живых бактериальных клетках тот же эффект наблюдали с помощью репортеров на основе щелочной фосфатазы: когда цитоплазматические белки были слиты с секретируемым ферментом, присутствие HSI#6 вызывало резкий рост секрецированной активности без изменения уровня синтеза белка. Иными словами, HSI#6 фактически разъединяет экспорт от обычной проверки идентичности субстрата, превращая систему Sec в универсальную насосную машину для любого достаточно развернутого белка.
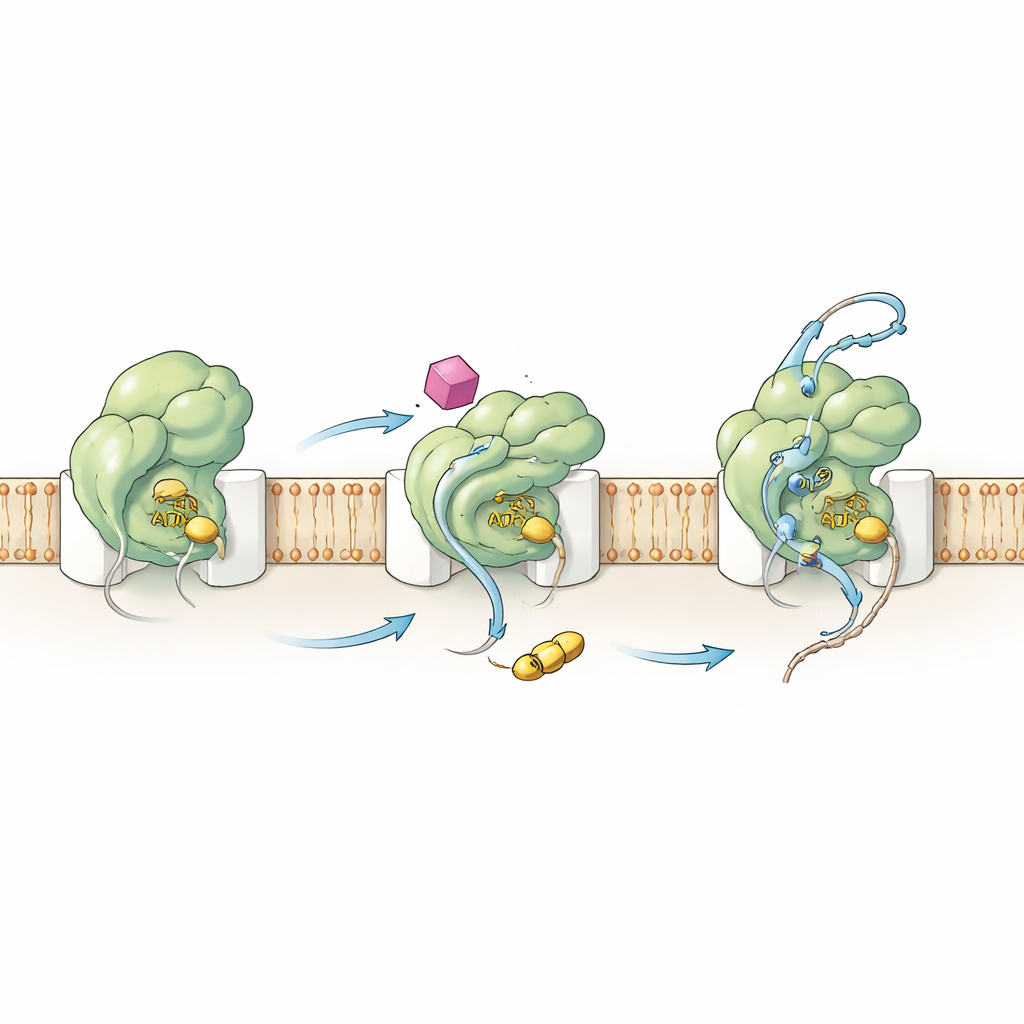
Перенастройка мотора изнутри
Чтобы понять, как HSI#6 вызывает такое поведение, команда изучила как химию, так и движения SecA. Кинетические измерения показали, что соединение смещает ключевой шаг активации вверх по потоку: комплекс SecA–канал становится каталитически активным ещё до того, как связывается белковый субстрат. HSI#6 также облегчает SecA отдать истраченный «топливный» ADP — обычно медленный, лимитирующий по скорости шаг — и тем самым поддерживает более быстрый цикл АТФ. С помощью масс-спектрометрии обмена водород/дейтрий авторы картировали, как HSI#6 меняет гибкость различных участков SecA. Соединение выборочно ослабляет части белка, которые распознают субстраты и соединяются с каналом, при этом упрочняя каркасный регион, который, вероятно, служит местом связывания. Полученная картина движений напоминает уже задействованное, «включённое» состояние транслоказы, что позволяет предположить, что HSI#6 стабилизирует активированную форму — возможно, даже предпочитая мономерный SecA, связанный с каналом — без присутствия субстрата.
Почему это важно для медицины и биотехнологий
Показав, что малая молекула может аллостерически активировать SecA и лишить систему обычной селективности по клиентам, эта работа выявляет новый способ контролировать центральную бактериальную машину. Для борьбы с инфекциями форсированная, неконтролируемая секреция может ослаблять патогены, истощая энергию и нарушая их тонко настроенные программы экспорта, делая активаторы наподобие HSI#6 привлекательными отправными точками для разработки антибиотиков — или ориентирами при создании будущих ингибиторов, блокирующих те же регуляторные элементы. Для биотехнологий тот же принцип можно переиспользовать для усиления секреции полезных рекомбинантных белков без необходимости в проектированных сигнальных пептидах или сложных генетических вмешательствах. По существу, исследование демонстрирует, что бактериальный «порт» для белков можно перепрограммировать химически, открывая новые пути как в борьбе с микроорганизмами, так и в использовании их в роли микрофабрик.
Цитирование: Sedky, H., Hamed, M.B., Krishnamurthy, S. et al. A small molecule allosterically activates SecA dependent secretion. Commun Biol 9, 368 (2026). https://doi.org/10.1038/s42003-026-09623-w
Ключевые слова: секреция белков у бактерий, транслоказа SecA, аллостерическая активация, регуляторы малых молекул, поиск антибактериальных препаратов