Clear Sky Science · ru
LncRNA P4HA2-AS1 способствует интерстициальному фиброзу почек через K63-убиквитинирование ULK1, опосредованное TRIM32, и дисрегуляцию аутофагии
Почему рубцевание почек важно
Хроническое заболевание почек поражает сотни миллионов людей во всем мире и часто прогрессирует бессимптомно до тех пор, пока диализ или трансплантация не станут единственным способом выжить. В основе этого ухудшения лежит процесс, называемый рубцеванием, при котором нормальная почечная ткань постепенно замещается плотным, нефункциональным материалом. В этом исследовании поставлен простой, но ключевой вопрос: какие молекулярные переключатели внутри клеток почек толкают их в сторону вредного рубцевания и возможно ли повернуть эти переключатели обратно?
Скрытый РНК‑переключатель в клетках почек
Наши почки фильтруют кровь с помощью сложных сетей крошечных канальцев. При повреждении этих канальцев — из‑за обструкции оттока мочи, высокого уровня сахара в крови или внезапного нарушения кровоснабжения — они могут реагировать откладыванием рубцовой ткани между клетками. Исследователи изучали почки мышей с разными типами повреждения и сравнивали их со здоровыми почками с помощью РНК‑секвенирования — метода, который показывает, какие гены включены. Они обнаружили малоизвестную молекулу P4HA2-AS1, длинную некодирующую РНК, не кодирующую белок, которая последовательно была повышена в повреждённых почках, формирующих рубцы, и в культуре человеческих почечных клеток, находившихся в стрессе. Эта РНК преимущественно локализовалась в везикулярной/жидкостной части клетки, что указывает на то, что она может регулировать белки в этой среде. 
Понижение уровня РНК для защиты почки
Чтобы проверить, является ли P4HA2-AS1 просто свидетелем повреждения или активным его драйвером, команда снизила её уровни у мышей и в культивируемых человеческих почечных клетках. В классической модели длительной обструкции, где перевязывают один мочеточник, уменьшение этой РНК с помощью таргетной вирусной доставки смягчало многие признаки рубцевания: канальцы оставались более целыми, между клетками было меньше коллагена и других белков рубца, а маркеры функции почек в крови улучшались. В культурах человеческих почечных клеток снижение P4HA2-AS1 также ослабляло ответ на сильный профибротический сигнал TGF‑β, приводя к меньшему образованию фибронектина, коллагена и других провоспалительных/профибротических факторов. Эти эксперименты показали, что эта РНК не просто маркер повреждения, а активно питает процесс рубцевания.
Аутофагия: от домохозяйства к вреду
Затем исследователи задали вопрос, как именно эта РНК причиняет вред. Их данные по экспрессии генов и визуализации указали на аутофагию — встроенную в клетку систему утилизации, разрушающую изношенные белки и органеллы. При нормальных условиях аутофагия — полезный процесс поддержания гомеостаза, но при чрезмерной и продолжительной активации она может сдвинуть повреждённые почки в сторону неадаптивного восстановления и рубцевания. В стрессированных почечных клетках P4HA2-AS1 усиливала поток субстратов через аутофагический путь, приводя к накоплению везикул переработки. При блокировании РНК эта гиперактивация снижается до более нормальных уровней как в клетках, так и в почках мышей с обструкцией. Мыши с дефицитом ULK1, ключевого фермента запуска аутофагии, также были защищены от рубцевания, и в этих животных сверхэкспрессия P4HA2-AS1 уже не усугубляла повреждение, что прочно связывает эффекты РНК с этим путём.
Трёхзвенная молекулярная цепочка
Углубляясь, команда использовала биохимические методы «ловли» для идентификации белков, физически связывающихся с P4HA2-AS1. Выделялся один белок: TRIM32, фермент, помечающий другие белки небольшими молекулярными «флажками» — убиквитином. РНК связывается с TRIM32 и защищает его от разрушения, повышая его уровни в почечных клетках. Стабилизированный TRIM32, в свою очередь, прикрепляет специфическую цепочку убиквитина типа K63 к ULK1. Вместо направления ULK1 на разрушение, такая метка действует как усилитель, повышая способность ULK1 запускать аутофагию. Когда учёные удаляли TRIM32 у мышей или заглушали его в почечных клетках, и рубцевание, и чрезмерная аутофагия уменьшались. Повторное введение TRIM32 в клетки, где P4HA2-AS1 был блокирован, частично восстановило профибротический ответ, показывая, что этот фермент является ключевым промежуточным звеном в цепи. 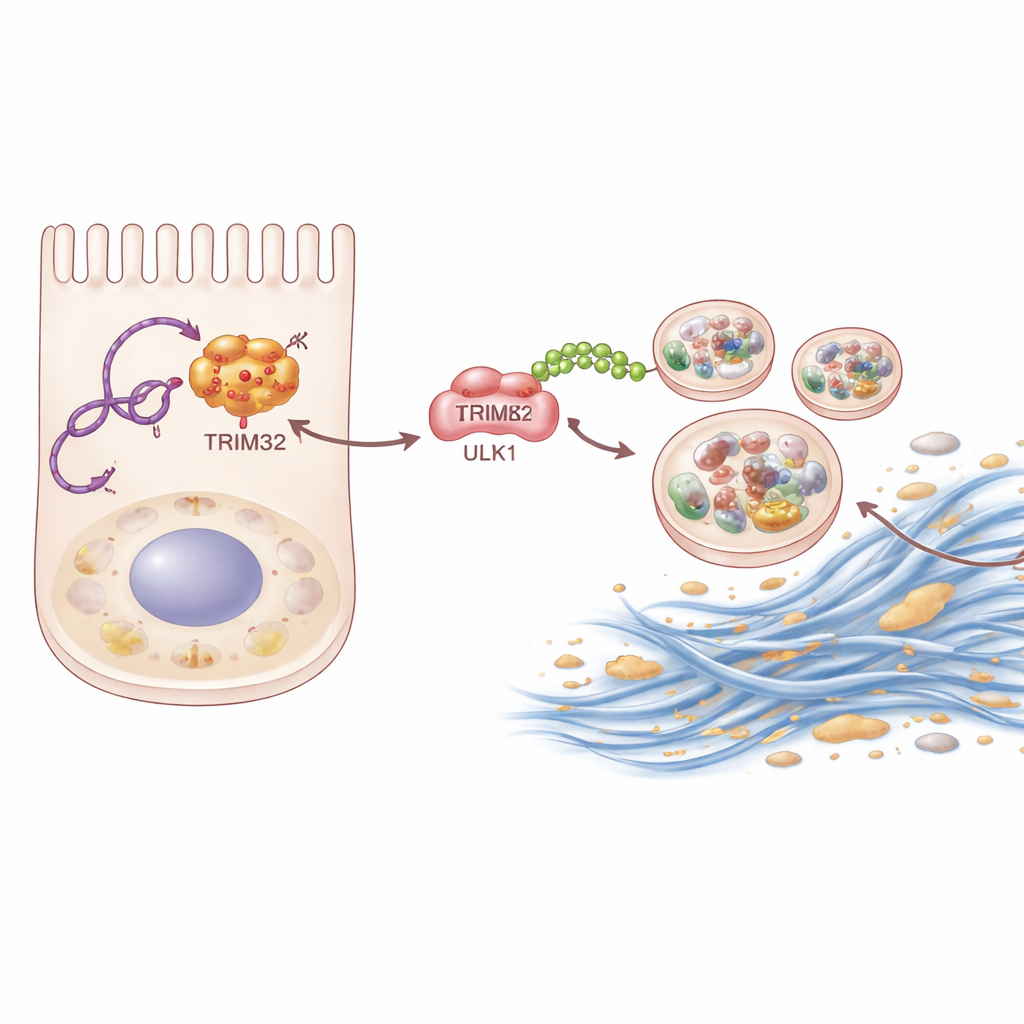
Новые пути к более «мягким» почкам
В совокупности работа выявляет ранее неизвестный молекулярный маршрут, связывающий длинную некодирующую РНК, метки белков и клеточную утилизацию с накоплением рубцовой ткани в почках. При повреждении почек P4HA2-AS1 повышается, стабилизирует TRIM32, усиливает ULK1 и доводит аутофагию за пределы её полезной роли, в конечном итоге способствуя накоплению фибротических белков и потере функции. Для неспециалистов ключевая мысль такова: рубцевание почек не является неизбежной «чёрной ящиком» — им управляют определяемые переключатели, которые потенциально можно лечить. Таргетирование оси P4HA2-AS1–TRIM32–ULK1 — путем снижения уровней «вредной» РНК, усмирения TRIM32 или тонкой настройки активности ULK1 — может в будущем предложить новые подходы для замедления или предотвращения прогрессирования хронического заболевания почек.
Цитирование: Pan, Z., Xiao, F., Hu, W. et al. LncRNA P4HA2-AS1 drives renal interstitial fibrosis via trim32-mediated k63 ubiquitination of ULK1 and autophagic dysregulation. Commun Biol 9, 339 (2026). https://doi.org/10.1038/s42003-026-09618-7
Ключевые слова: хроническое заболевание почек, почечный фиброз, аутофагия, длинная некодирующая РНК, почечные канальцы