Clear Sky Science · ru
Ожирение нарушает сперматогенез через ферроптоз клеток Лейдига, вызванный печёночными экзосомами с miR-122-5p
Почему вес и фертильность связаны
Ожирение обычно обсуждают в контексте сердечно‑сосудистых заболеваний и диабета, но оно также может незаметно подрывать мужскую фертильность. В этом исследовании на мышах обнаружен неожиданный механизм, через который жирная диета снижает уровень тестостерона и повреждает сперматогенез: печень посылает в кровь крошечные «посылки‑мессенджеры», которые запускают особую форму гибели клеток в гормонопродуцирующих клетках яичек. Понимание этой скрытой коммуникации печень→яички может помочь объяснить, почему у людей с избыточным весом часто встречаются низкий тестостерон и бесплодие, а также указать на новые терапевтические мишени.
Скрытая почта между органами
Наши органы постоянно общаются между собой с помощью гормонов и других химических сигналов. Одна из форм такой связи — экзосомы: нанометровые пузырьки, выделяемые клетками и несущие липиды, белки и генетический материал. Исследователи начали с мышей, которых кормили либо обычным рационом, либо высокожировой диетой, вызывающей ожирение, инсулинорезистентность и плохой контроль гликемии. У ожиревших мышей яички были меньших размеров и менее активны: у них снижались количество сперматозоидов, уровень тестостерона, а также размер и число сперматогенетических канальцев. При изучении ключевых маркеров клеток в яичках обнаружилось меньше клеток Лейдига, производящих тестостерон, а также снижение числа ранних и поздних форм сперматозоидов, что подтверждает нарушение всей «конвейерной» линии производства спермы. 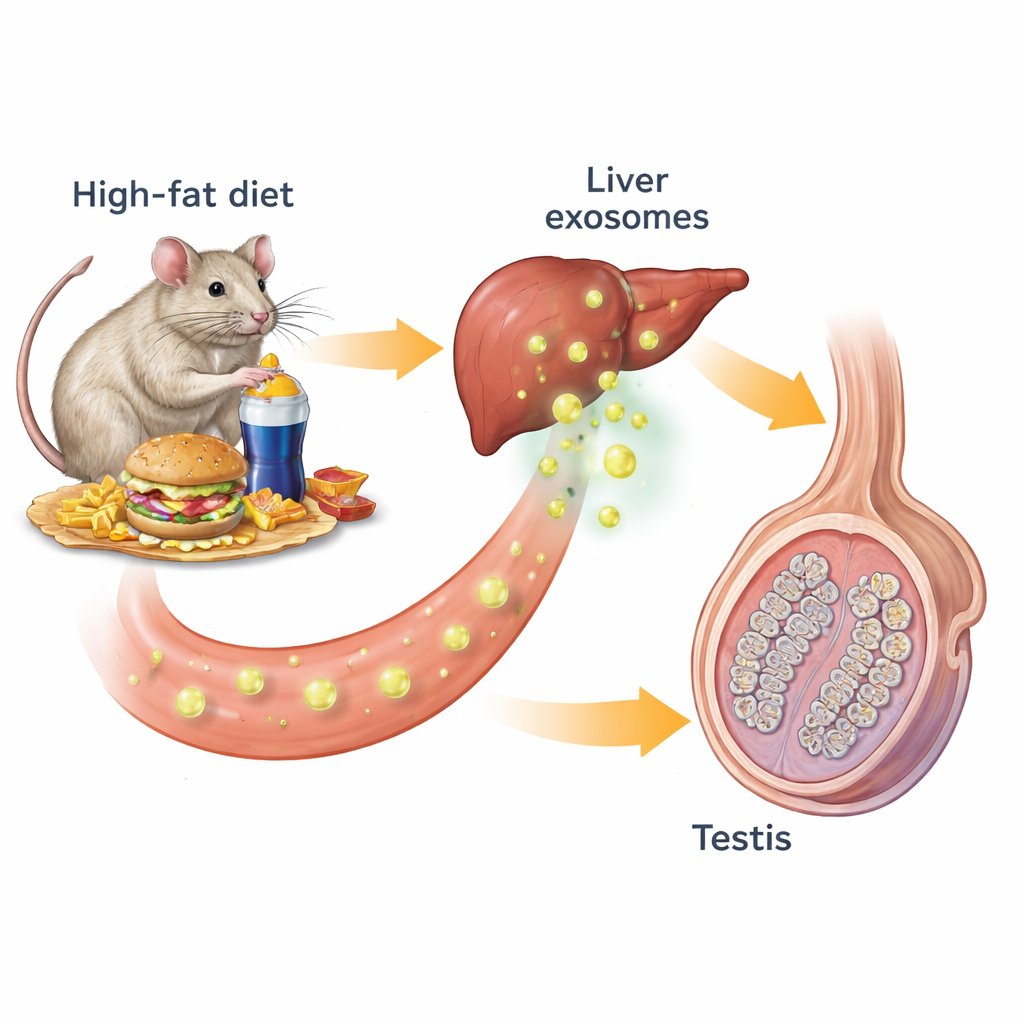
Экзосомы распространяют повреждение
Чтобы проверить, способствуют ли циркулирующие экзосомы этому вреду, учёные очистили экзосомы из крови ожиревших и худых мышей. Инъекции экзосом от ожиревших мышей здоровым худым животным были достаточны, чтобы воспроизвести многие проблемы: у реципиентов появились признаки метаболических нарушений, упал уровень тестостерона, а количество сперматозоидов и структура яичек ухудшились. Блокирование выделения экзосом у ожиревших мышей с помощью препарата GW4869 в значительной мере обратило эти изменения, восстановив число сперматозоидов, уровень тестостерона и нормальную архитектуру яичек. Эти результаты показывают, что экзосомы в кровотоке — не просто наблюдатели; они активно переносят вредные сигналы от ожирения к репродуктивной системе.
Токсичная форма гибели клеток
Далее команда изучала, что именно экзосомы делают с клетками Лейдига. Они сосредоточились на ферроптозе — форме гибели клеток, зависящей от железа и характеризующейся накоплением железа, окислительным повреждением липидов и нарушением митохондрий — энергетических станций клетки. У ожиревших мышей и у здоровых животных, получивших экзосомы от ожиревших доноров, в яичках отмечались повышенные уровни железа и малонового альдегида (продукта повреждения липидов), а также явные повреждения митохондрий при электронно‑микроскопическом исследовании. Лечение ожиревших мышей ингибитором ферроптоза Ferrostatin‑1 сохраняло клетки Лейдига, повышало уровни тестостерона и количество сперматозоидов и улучшало состояние митохондрий. В культуре клеток тот же препарат защищал изолированные клетки Лейдига от гибели и окислительного стресса, вызванного экзосомами от ожиревших животных. В совокупности эти эксперименты выявляют ферроптоз как ключевое звено между ожирением и сниженной продукцией тестостерона.
Послание печени и переключатель SCD2
Чтобы отследить сообщение внутри экзосом, исследователи секвенировали их мелкий РНК‑груз и обнаружили, что определённый микроРНК, miR‑122‑5p, сильно увеличен в экзосомах от ожиревших мышей. Эта микроРНК была особенно обильна в печени и в экзосомах печёночного происхождения, и такие печёночные экзосомы можно было проследить до яичек. Когда уровни miR‑122‑5p экспериментально снижали в экзосомах, клетки Лейдига становились менее восприимчивыми к ферроптозу, а продукция тестостерона улучшалась, несмотря на то что животные оставались метаболически нездоровыми. Дополнительные тесты показали, что miR‑122‑5p прямо подавляет ген Scd2, который участвует в преобразовании определённых жиров в формы, защищающие клетки от окислительного повреждения. Снижение Scd2 в клетках Лейдига делало их более уязвимыми к ферроптозу и снижало тестостерон, тогда как усиление выражения Scd2 у ожиревших мышей частично восстановливало уровни гормона, производство спермы и структуру митохондрий. 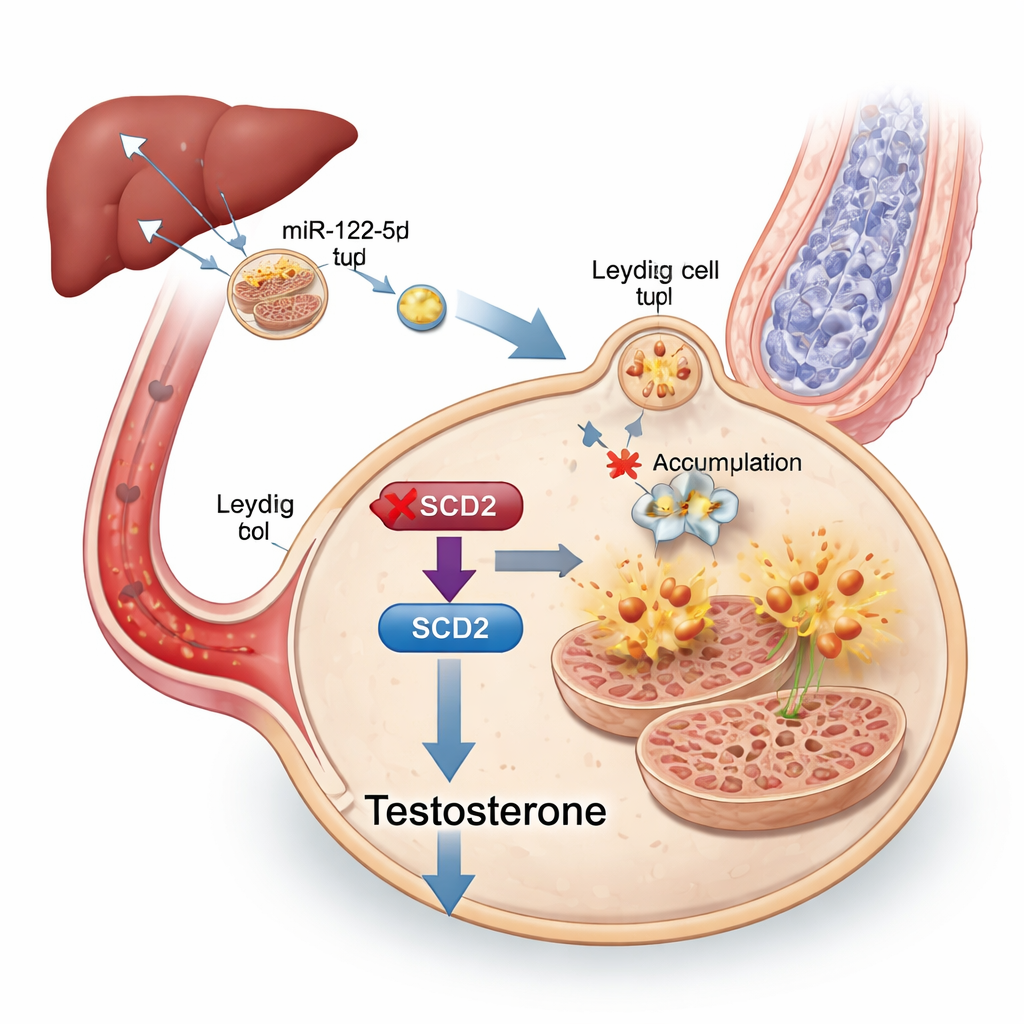
Что это значит для здоровья людей
Проще говоря, эта работа показывает, что высокожировая диета может заставить печень загружать экзосомы избытком miR‑122‑5p. Эти экзосомы путешествуют по крови к яичкам, где микроРНК выключает «жировой» переключатель Scd2 в клетках Лейдига. Без Scd2 клетки накапливают железозависимое окислительное повреждение, проходят ферроптоз, вырабатывают меньше тестостерона и в итоге обеспечивают меньше здоровых сперматозоидов. Хотя исследования проводились на мышах и требуют подтверждения у людей, они выделяют печёночные экзосомы, miR‑122‑5p, ферроптоз и Scd2 как перспективные биомаркеры и потенциальные мишени для лекарств против бесплодия, связанного с ожирением — и подчёркивают ещё одну причину, почему длительные высокожировые диеты могут незаметно подрывать репродуктивное здоровье.
Цитирование: Wang, N., Zhang, B., Chen, T. et al. Obesity impairs spermatogenesis via Leydig cell ferroptosis induced by liver-derived exosomal miR-122-5p. Commun Biol 9, 318 (2026). https://doi.org/10.1038/s42003-026-09612-z
Ключевые слова: ожирение и мужская фертильность, тестостерон, экзосомы, клетки Лейдига, ферроптоз