Clear Sky Science · ru
Распознавание и связывание гликолипидов сиглеком-6 зависит от взаимодействий с клеточной мембраной
Как наши клетки отличают своих от чужих
Иммунная система постоянно сканирует собственные клетки, решая, когда сохранять спокойствие, а когда атаковать. Важную роль в этой слежке играет распознавание сахарных структур на поверхности клеток. В этом исследовании показано, что один человеческий иммунный рецептор, называемый сиглеком-6, опирается не только на сами сахара, но и на окружающую клеточную мембрану, чтобы принимать особенно точные решения о том, к чему прикрепляться. Такая необычная стратегия может помочь объяснить, как организм точно настраивает иммунные сигналы, и открыть новые возможности для прицельной терапии.
Сахаро-чувствительный страж на иммунных клетках
Сиглеки — это семейство рецепторов на иммунных клетках, распознающих сахара, содержащие сиаловую кислоту, что помогает иммунной системе отличать «свое» от «чужого». Большинство сиглеков опираются на один высоко консервативный аминокислотный остаток — аргинин — для захвата этих сахаров. Если этот аргинин убрать, связывание обычно теряется. Сиглек-6, однако, выделяется: предыдущие работы показали, что он всё ещё может связываться с некоторыми липидами, несущими сахара, даже когда этот ключевой аргинин мутирован. Новое исследование поставило цель выяснить, как сиглек-6 может нарушать это, казалось бы, правило и что это значит для его роли в тучных клетках, В-клетках памяти и клетках плаценты человека.
Особые липиды, которые ищет сиглек-6
На поверхности клеток релевантные сахара могут быть представлены как на белках, так и на липидах. В этой работе внимание сконцентрировано на группе сахаросодержащих липидов, называемых ганглиозидами, особенно на трёх близких по структуре — GM1, GM2 и GM3. Все три выдвигают из мембраны одиночную «головку», заканчивающуюся сиаловой кислотой. Ранее показывали, что сиглек-6 сильно связывается с GM1 в составе мембраны, но почти не связывается с GM2 или GM3, несмотря на схожесть их сахарных головок. С помощью подробных компьютерных симуляций реалистичных мембран авторы подтвердили, что сиаловая кислота в GM1 и GM3 одинаково открыта и доступна. Иначе говоря, простая физическая доступность не объясняет особый статус GM1. Вместо этого дополнительный сахар на конце GM1 — терминальная галактоза — оказался критическим элементом, помогающим правильно позиционировать сиглек-6 относительно мембраны.
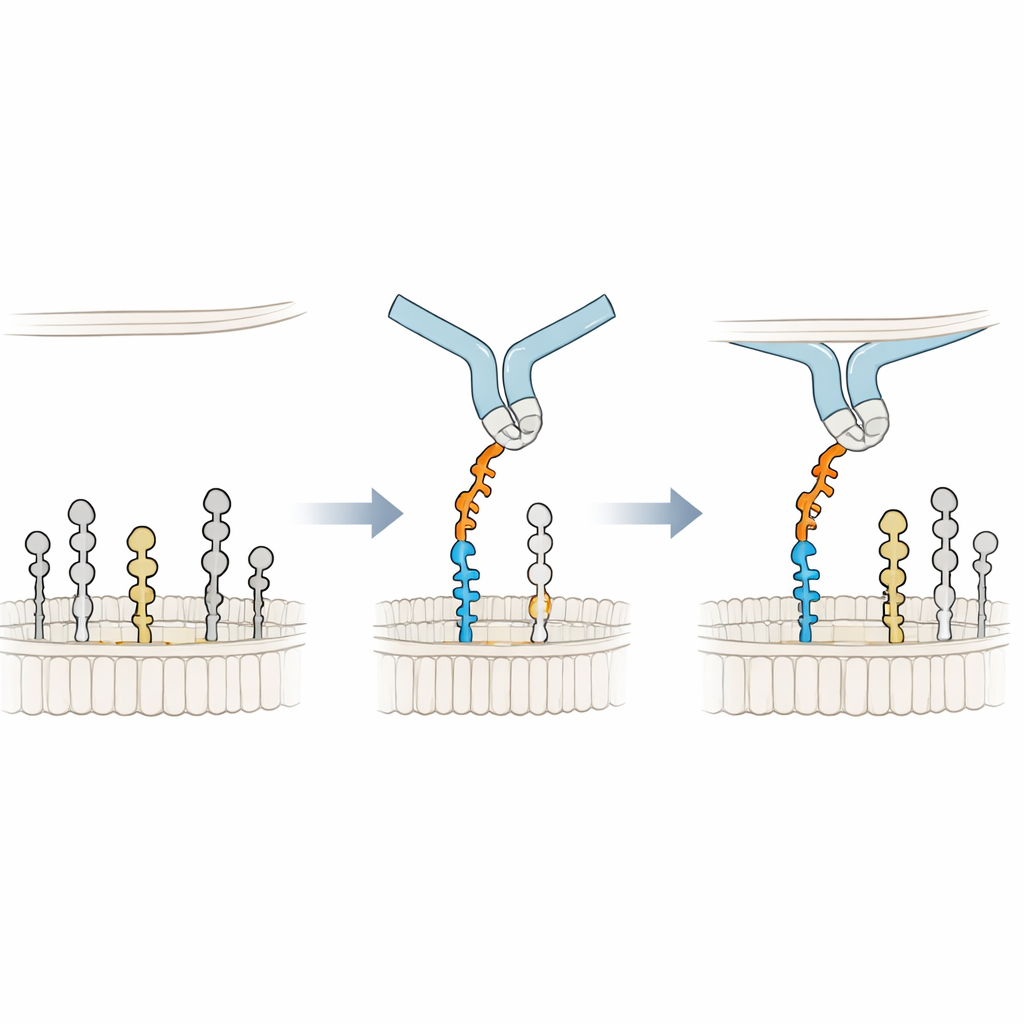
Опора на мембрану ради более прочного захвата
Чтобы понять механизм связывания на атомарном уровне, исследователи построили 3D‑модели сиглек-6, взаимодействующего с GM1 в мембране, и провели длительные молекулярно‑динамические симуляции. Они обнаружили, что сиглек-6 всё ещё использует свой канонический аргинин (Arg122) для контакта с сиаловой кислотой, но этот контакт прерывист: он появляется и исчезает во времени. Стабильность комплекса обеспечивает нечто новое: соседний триптофан (Trp127) вдвигается в жировую часть мембраны, а прилегающий лизин (Lys126) взаимодействует с заряженными головками окружающих липидов. Эта «клинья» в мембране дополняет обычное сахар—аргининное взаимодействие, фактически позаимствовав энергию связывания у липидного окружения. Когда терминальную галактозу GM1 удаляют, имитируя GM2, гибкая петля в сиглек-6 занимает освободившееся пространство, оттягивает рецептор от мембраны и нарушает такую мембрано‑ассистированную опору, что объясняет потерю стабильного связывания.
Эксперименты, проверяющие механизм
Команда затем проверила эти вычислительные гипотезы в живых клетках и в биохимических тестах. Они модифицировали клетки так, чтобы те экспрессировали нормальный или мутантный сиглек-6, и измеряли, насколько хорошо клетки связываются с флуоресцентными липосомами и маленькими липидными дисками с GM1. Мутация канонического аргинина лишь умеренно снижала связывание, когда GM1 находился в мембране, подтверждая, что сиглек-6 в этом контексте не полагается исключительно на этот остаток. Напротив, мутация Trp127 почти полностью устраняла связывание с липосомами, содержащими GM1, а мутация сразу Trp127 и Lys126 практически полностью уничтожала связывание. Те же мутанты нормально связывались с подобными GM1 сахарами, представленными вне мембраны, что показывает сохранность базовой структуры сиглек-6. Эксперименты с нативной масс‑спектрометрией дополнительно выявили, что сиглек-6 может связываться не только с GM1, но и с обычными фосфолипидами, причём это липидное взаимодействие исчезает при удалении Trp127. Удивительно, но сиглек-6 даже прилипал к «голым» липосомам без GM1 — снова в зависимости от Trp127 — что указывает на возможность первичного «пробного» контакта с мембраной с последующей фиксацией при обнаружении GM1.
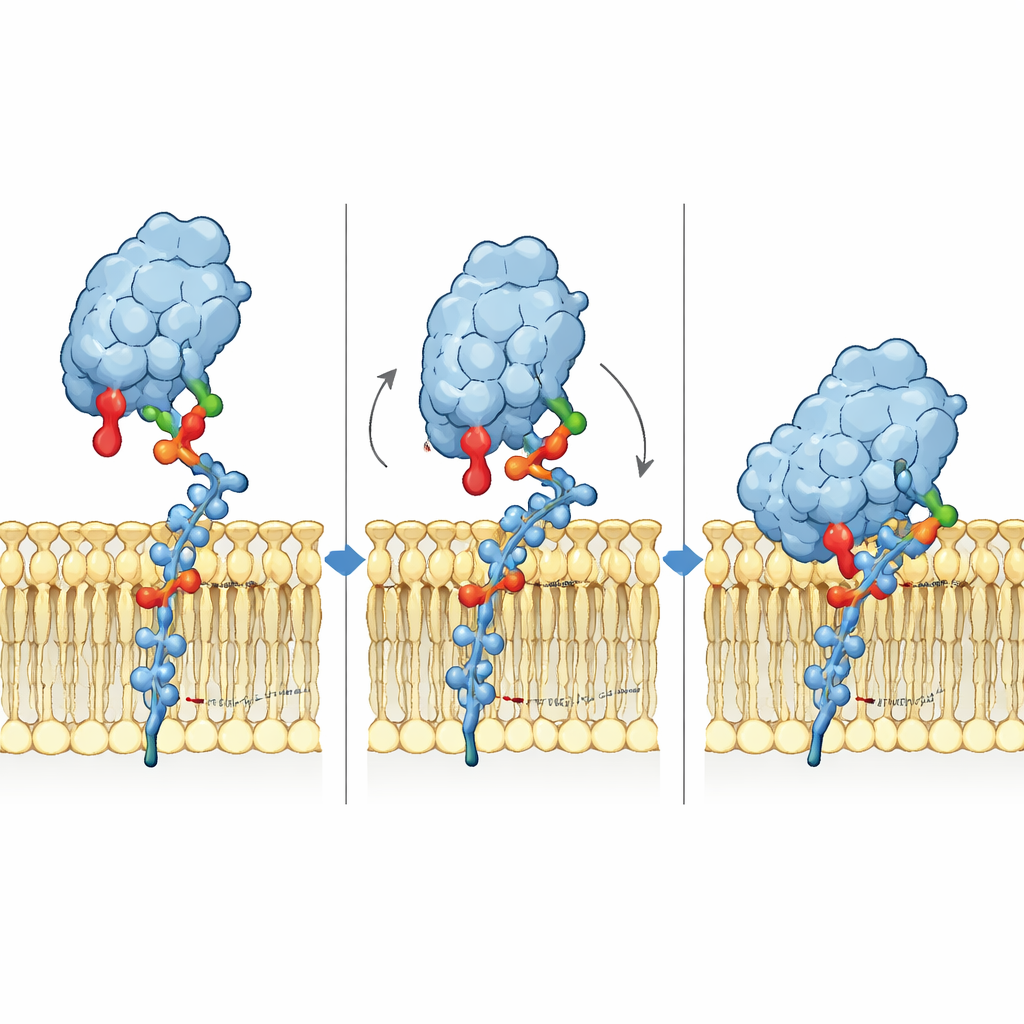
Свободные сахара рассказывают иную историю
Когда те же три ганглиозида тестировали в виде свободно плавающих сахарных фрагментов, а не в составе мембраны, сиглек-6 вёл себя скорее как его родственники. В растворе он связывался с GM1, GM2 и GM3 с примерно одинаковой слабой аффинностью, и теперь канонический аргинин был необходим: мутация Arg122 резко снижала связывание, тогда как мутация Trp127 почти не влияла. Это различие показывает, что сиглек-6 фактически переключает механизм в зависимости от того, встречает ли он сахара в мембране или в свободной форме. В мембране он полагается на кооперацию между сахарной головкой, терминальной галактозой GM1 и прямым контактом с мембраной; в растворе он возвращается к классическому аргинин-центрированному механизму распознавания.
Почему это важно для иммунного контроля
В совокупности исследование выявляет сиглек-6 как тонко настроенный датчик, который использует физический контекст мембраны для повышения своей специфичности. Частично закрепляясь в окружающих липидах, он способен селективно распознавать GM1 среди очень похожих ганглиозидов, превращая общий «считыватель сиаловой кислоты» в высокоточный детектор конкретного поверхностного рисунка. Эта мембрано‑ассистированная стратегия выглядит уникальной среди изученных сиглеков и может помочь сиглек-6 сканировать поверхности клеток в поисках специфических гликолипидных сигнатур, регулирующих иммунные ответы или отмечающих определённые ткани, например плаценту человека. Понимание этого двойного режима распознавания может способствовать разработке терапий и диагностических инструментов, использующих необычное сочетание сиглек-6 чувствительности к сахарам и мембране.
Цитирование: D’Andrea, S., Schmidt, E.N., Bui, D. et al. Glycolipid recognition and binding by Siglec-6 hinges on interactions with the cell membrane. Commun Biol 9, 333 (2026). https://doi.org/10.1038/s42003-026-09609-8
Ключевые слова: Сиглек-6, ганглиозиды, клеточная мембрана, распознавание гликолипидов, регуляция иммунитета