Clear Sky Science · ru
Ингибирование ATM повышает эффективность встраивания за счёт подавления AAV-индуцированной активации апоптотических путей
Повышение эффективности генного редактирования
CRISPR-редактирование обещает терапии генетических заболеваний, более устойчивые культуры и мощные исследовательские инструменты. Но одна из его наиболее ценных возможностей — точная вставка новой ДНК в заданное место генома, известная как «встраивание» (knock-in) — по‑прежнему работает неэффективно. Это исследование изучает, почему одни клетки принимают новую ДНК охотнее других, и показывает способ побудить клетки выполнять точные правки чаще, особенно при использовании адено‑ассоциированного вируса (AAV), одного из ведущих векторов для генной терапии.
Наблюдение за ремонтом ДНК в реальном времени
Чтобы понять, что помогает или мешает точной вставке, исследователи создали сложную «панель мониторинга» внутри эмбриональных стволовых клеток мыши. Эта система с тремя репортерами использует три флуоресцентных маркера, чтобы в одних и тех же клетках отслеживать: был ли разрезан геном CRISPR, произошла ли точная встраиваемая замена и была ли вставка донорской ДНК выполнена более грубым методом восстановления. Считывая различные цветовые комбинации с помощью проточной цитометрии, они могли отделить чистые шаблонно‑зависимые правки от ошибочных вставок и неизменённых клеток. Такое параллельное отслеживание позволило им с гораздо большим разрешением, чем старые ПЦР‑методы, проследить вклад разных путей восстановления ДНК в каждое из исходов.
Два типа доноров, два разных ответа
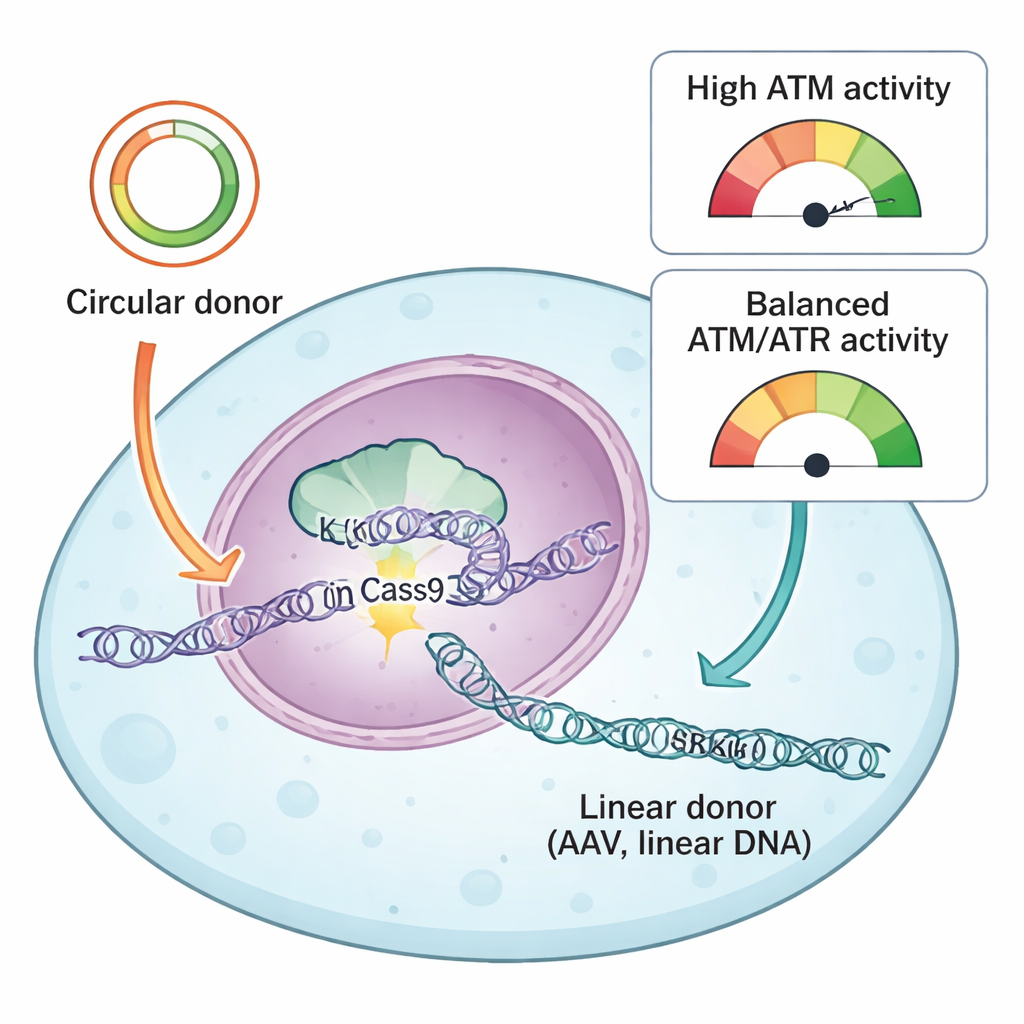
Команда сравнила два распространённых типа донорной ДНК, используемых для направляемого восстановления CRISPR: кольцевые плазмиды и линейную ДНК, полученную из AAV. Оба содержат совпадающие «гомологичные плечи», которые подсказывают клетке, куда вставить новую последовательность, но они попадают в клетку в разной физической форме. Кольцевые плазмиды представляют собой замкнутые двойные спирали, тогда как доноры AAV обычно поступают как одиночные линейные молекулы. Используя свою систему репортеров и библиотеку препаратов, нацеленных на белки ответа на повреждение ДНК, авторы обнаружили, что один ключевой белок, ATR, был одинаково необходим для успешных встраиваний с обоими типами доноров. Ингибирование ATR резко снижало точную вставку, тогда как мягкое усиление активности ATR через путь KEAP1–NRF2 делало встраивания более эффективными, особенно с донорами AAV.
Когда защита ДНК даёт обратный эффект
Другой датчик повреждения ДНК, ATM, проявил себя поразительно зависимо от типа донора. При использовании кольцевых плазмид блокирование ATM снижало и точные встраивания, и вставки, выполненные путём лигирования концов, что соответствует его классической роли в помощи клеткам при восстановлении двухцепочечных разрывов. Но при линейной ДНК — будь то от AAV, самокомплементарного AAV или плазмид, разрезанных в прямые фрагменты — ингибирование ATM действовало наоборот: оно увеличивало эффективность встраивания. Исследователи проследили этот эффект до того, как клетки интерпретируют всплески линейной ДНК. Высокие дозы AAV сильно активировали ATM, что, в свою очередь, включало p53 и каспазу‑3, ключевых исполнителей программируемой гибели клеток. Клетки, поглотившие много копий донорной ДНК и потому имевшие наибольший шанс на успешное встраивание, одновременно оказывались наиболее уязвимы к гибели из‑за этой системы сигнализации.
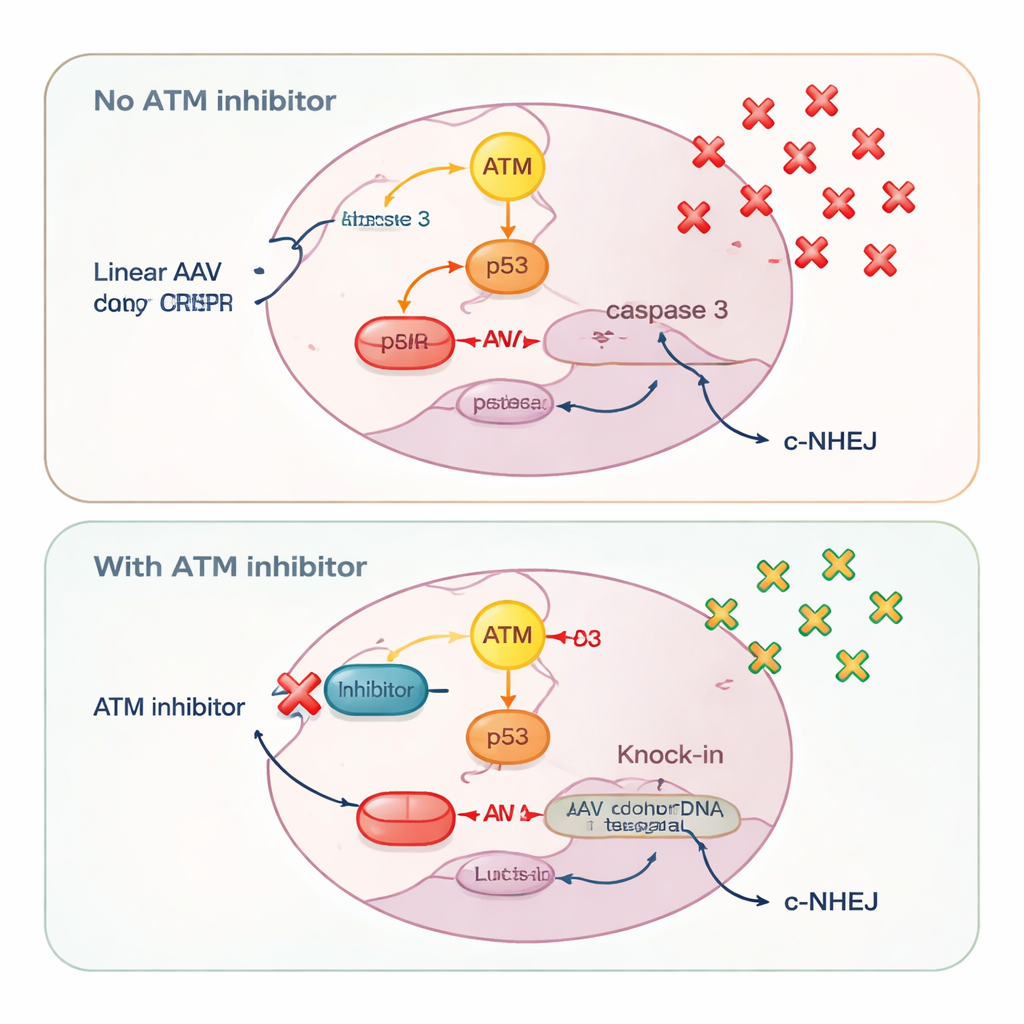
Сохранение наиболее подготовленных клеток
Добавляя ингибиторы ATM, учёные подавляли путь смерти ATM–p53–каспаза‑3. Это сохранило клетки с высоким содержанием донорной ДНК, позволив большему числу из них выжить достаточно долго для завершения точного встраивания. Измерения числа копий вирусного генома подтвердили, что ингибирование ATM увеличивало количество молекул AAV, сохраняющихся в клетках. Одновременно блокада ATM слегка ослабляла быстрый грубый путь ремонта, называемый классическим негомологичным лигированием концов (c-NHEJ), что проявлялось в сниженной активации DNA‑PK, ключевого фермента этого пути. Ослабление этой конкурирующей опции восстановления смещало больше разрезов CRISPR в сторону гомологичного встраивания, а не быстрых латаний, игнорирующих донорный шаблон.
Что это значит для будущих генетических терапий
Для неспециалистов смысл в том, что те же клеточные механизмы защиты, которые уберегают нас от повреждений ДНК, могут непреднамеренно саботировать точное генное редактирование, особенно при использовании больших количеств вирусной донорной ДНК. Работа показывает, что аккуратная настройка этих механизмов — поддержание активности ATR при одновременном временном подавлении ATM в присутствии линейных доноров, таких как AAV — может сделать CRISPR‑встраивания более надёжными и эффективными. Такая стратегия может улучшить генные терапии, клеточную инженерию и модели заболеваний, помогая большему числу клеток принять требуемое изменение и избегая ненужной гибели клеток.
Цитирование: Natsagdorj, ME., Hara, H., Uosaki, H. et al. ATM Inhibition Enhances Knock-in Efficiency by Suppressing AAV-Induced Activation of Apoptotic Pathways. Commun Biol 9, 177 (2026). https://doi.org/10.1038/s42003-026-09604-z
Ключевые слова: CRISPR встраивание, редактирование генов AAV, ответ на повреждение ДНК, ингибирование ATM, геномная инженерия