Clear Sky Science · ru
STING контролирует гликолиз и лактилцию гистонов, вызывая метаболическую перенастройку макрофагов при послеоперационной илеусе
Когда операция заставляет кишечник «поставить на паузу»
После абдоминальных операций у многих пациентов кишечник словно отказывается «просыпаться». Это замедление, называемое послеоперационной илеусой, может означать дни тошноты, вздутия и затянувшегося восстановления. В этом обзоре исследователи задают на первый взгляд простый вопрос: почему определённые иммунные клетки в кишечнике удерживают работу кишечника в состоянии приостановки и не могла бы модуляция одного молекулярного переключателя помочь двигательной активности возобновиться?
Как рутинная операция запускает воспаление кишечника
Абдоминальная операция неизбежно нарушает работу кишечника. У мышей деликатное обращение с кишкой вызывало отёк, накопление жидкости и закупорку содержимого в тонкой кишке. Когда учёные отслеживали, насколько далеко безопасный флуоресцентный краситель прошёл через кишечник, они увидели резкое замедление его продвижения — признак снижения моторики. Микроскопическое исследование стенки кишечника показало, что мышечный слой — ткань, которая собственно сокращается, продвигая содержимое — стал воспалённым и заполнился поступающими иммунными клетками, особенно макрофагами и нейтрофилами. Эти наблюдения указывают, что мышечная оболочка кишечника превращается в очаг воспаления после операции, и это местное воспаление тесно связано с параличом кишечника.
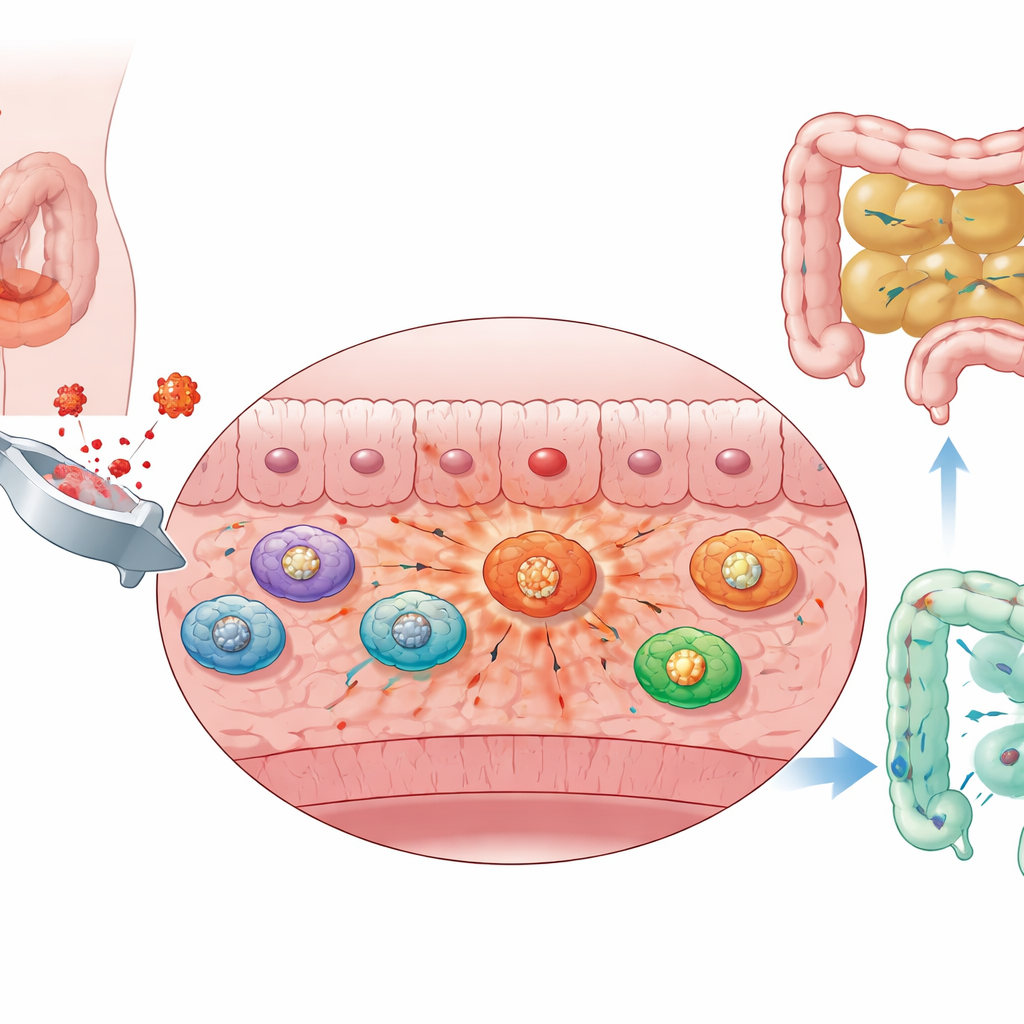
Макрофаги переключают топливо и подливают масла в огонь
Чтобы понять, чем занимаются эти инфильтрирующие макрофаги, команда проанализировала крупномасштабные данные РНК-секвенирования и одноклеточные профили из мышечного слоя кишечника. Они обнаружили, что макрофаги у животных после операции значительно усиливали быстрый путь сжигания сахара, известный как гликолиз. По сравнению с другими иммунными клетками в той же ткани инфильтрирующие макрофаги показали самые высокие показатели гликолиза и повышенную экспрессию ключевых гликолитических ферментов. Отдельный подтип этих клеток в значительной степени зависел от гликолиза, имел выраженные воспалительные подписи и активно реагировал на бактериальные компоненты, такие как липополисахарид. По сути, макрофаги переключились в режим высокого потребления сахара и высокой воспалительной активности, что, по-видимому, усугубляет воспаление мышечного слоя и поддерживает остановку моторики кишечника.
Молекулярный переключатель, связывающий распознавание угрозы и сжигание сахара
Далее исследователи сосредоточились на STING — белке, известном прежде всего как сигнал тревоги при наличии чужеродной ДНК, но всё чаще рассматриваемом как регулятор метаболизма. В воспалённом мышечном слое кишечника подмножество макрофагов с высоким гликолизом демонстрировало заметно повышенные уровни STING, что подтвердили и окрашивания тканей. В культуре клеток воздействие бактериальным липополисахаридом повышало как активность STING, так и уровни гликолитических ферментов, превращающих глюкозу в энергию и лактат. При нокауте гена STING этот всплеск сжигания сахара исчез: снизились уровни гликолитических промежуточных метаболитов, уменьшилась закислённость среды культуры и сократилось производство реактивных форм кислорода. Эти клетки с дефицитом STING также продукировали меньше лактата, что указывает на тесную связь между путём распознавания угрозы и метаболическим механизмом.
От сахара-отхода к эпигенетической памяти
Лактат часто рассматривают как метаболический отход, но здесь он выполняет более тонкую функцию. Команда показала, что у нормальных макрофагов поток лактата используется для химической модификации гистонов — белков, упаковывающих ДНК — в процессе, называемом лактиляцией. Эта модификация была особенно выражена на сайте H4K8 гистонов рядом с геном HK2, ключевого регулятора гликолиза. В клетках с дефицитом STING уровни лактилирования гистонов и доступность хроматина у промотора HK2 были снижены, а специализированные методы секвенирования подтвердили, что эти изменения ограничивали активацию HK2. Одновременно транскрипционный фактор IRF3 оказался способным непосредственно связываться с промотором HK2 более охотно при наличии метки лактилрования гистонов. Вместе эти шаги формируют самоподдерживающуюся петлю: STING стабилизирует факторы, усиливающие гликолиз; гликолиз производит лактат; лактат модифицирует гистоны, открывая ген HK2; а IRF3 усиливает экспрессию HK2, дополнительно подпитывая гликолиз и воспаление.
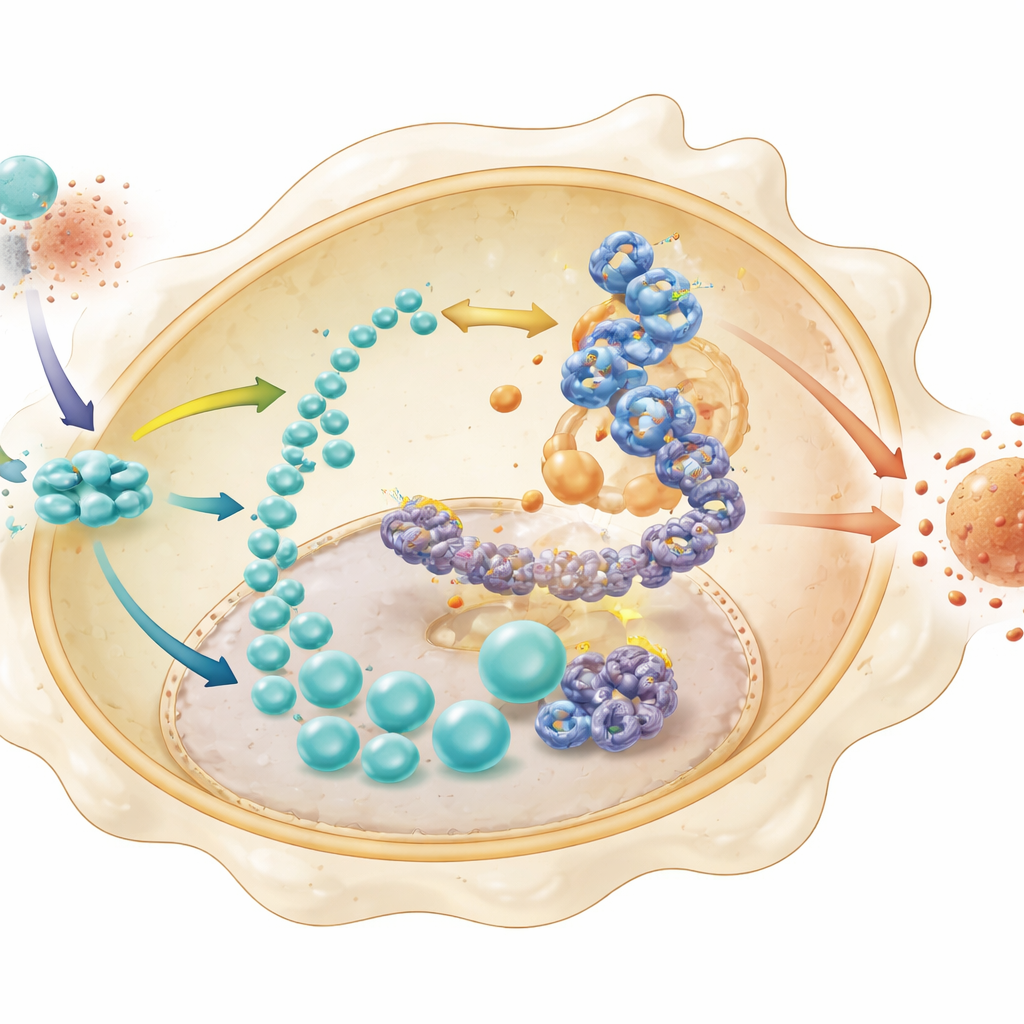
Разрыв петли позволяет кишечнику восстановиться
Наконец, команда проверила, может ли разрыв этой петли реально помочь животным восстановиться после послеоперационной илеуса. У мышей с дефицитом STING мышечная ткань кишечника выражала меньше гликолитических ферментов, содержала меньше воспалительных макрофагов и демонстрировала смещение от агрессивного провоспалительного состояния макрофагов в сторону более разрешающего профиля. Инфильтрация нейтрофилов была ниже, и гастроинтестинальный транзит улучшился. Фармакологическая блокада STING у нормальных мышей давала схожие преимущества, в то время как повторная активация фермента HK2 у животных без STING частично восстанавливала воспаление и проблемы моторики. Для непрофессионального читателя вывод ясен: один опаснический переключатель в макрофагах кишечника способен перепрограммировать их метаболизм так, что кишечник остаётся в затянувшейся паузе после операции. Нацеливание на STING — или на контрольную обратную связь гликолиза и лактилрования гистонов, которой он управляет — открывает перспективный путь для ускорения восстановления и облегчения одного из наиболее упрямых осложнений абдоминальных операций.
Цитирование: Chen, K., Li, G., Cheng, Y. et al. STING controls glycolysis and histone lactylation to drive macrophage metabolic reprogramming in postoperative ileus. Commun Biol 9, 358 (2026). https://doi.org/10.1038/s42003-026-09602-1
Ключевые слова: послеоперационная илеус, метаболизм макрофагов, путь STING, гликолиз, воспаление кишечника