Clear Sky Science · ru
Характеризация пригодности нанотел для разработки терапевтических препаратов с помощью Therapeutic Nanobody Profiler
Почему крошечные «родственники» антител важны для будущих лекарств
Многие из нынешних блокбастеров — это антитела: белки, которые с высокой точностью связываются с мишенями болезни. Новый класс ещё меньших связывающих молекул, называемых нанотелами, способен проникать в труднодоступные впадины на вирусах, опухолях и других мишенях. Но способность связываться недостаточна: кандидат в лекарственные препараты также должен легко производиться, оставаться стабильным в флаконе и быть безопасным в организме. В этой статье представлен Therapeutic Nanobody Profiler — вычислительный инструмент, помогающий учёным уже на раннем этапе и по последовательности предсказывать, какие нанотела с наибольшей вероятностью станут практичными лекарствами.
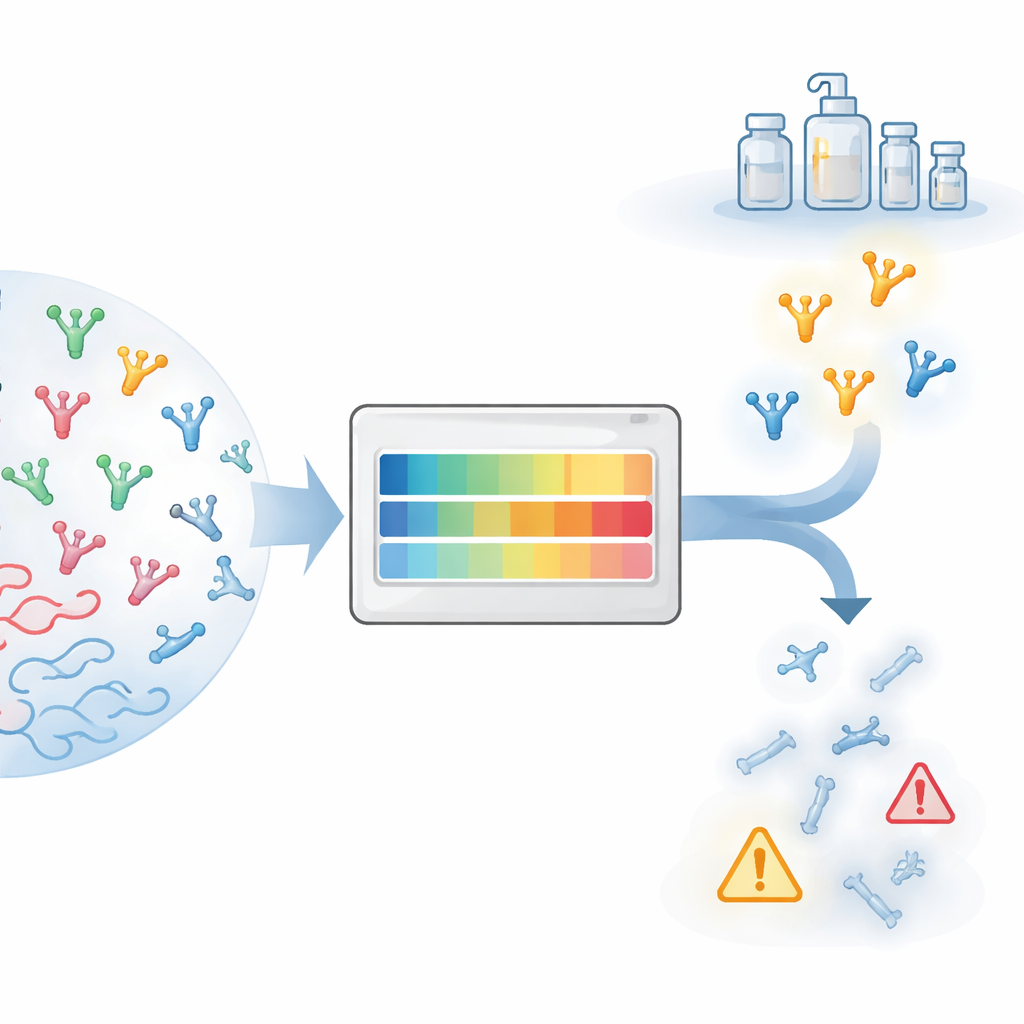
От перспективной идеи к реальному препарату
Преобразование белка в реальную терапию связано с рядом практических препятствий, объединённых термином «пригодность к разработке» (developability). Белки должны производиться в больших объёмах, оставаться растворимыми, не образовывать агрегаты и сохранять стабильность при транспортировании и хранении. За последнее десятилетие исследователи научились предсказывать многие из этих свойств для полноразмерных моноклональных антител, опираясь на обширные клинические данные и специальные лабораторные тесты. Нанотела, однако, структурно отличаются: они состоят из одного домена вместо пары цепей, часто имеют более длинные петли связывания и демонстрируют поверхности, скрытые в обычных антителах. Поэтому методы, настроенные под стандартные антитела, при применении к нанотелам могут давать вводящие в заблуждение результаты.
Профайлер, созданный с учётом особенностей нанотел
Чтобы устранить это несоответствие, авторы разработали Therapeutic Nanobody Profiler (TNP), вдохновлённый прежним инструментом для стандартных антител, но перестроенный с учётом биологии нанотел. Они собрали последовательности нанотел из множества источников: клинических испытаний, естественных иммунных репертуаров, патентов, научных публикаций и известных кристаллических структур. С помощью методов глубокого обучения, адаптированных к однодоменных антителам, они сгенерировали трёхмерные модели для этих последовательностей. Из каждой модели измеряли длину петель связывания, насколько далеко одна ключевая петля выступает от тела белка, а также как на поверхности расположены кластеры гидрофобных и заряженных остатков — признаки, сильно влияющие на растворимость, агрегацию и неселективное прилипание.
Два структурных варианта — оба рабочие
Одно из самых заметных наблюдений касается основной петли связывания, известной как CDR3. Когда команда количественно оценивала, насколько «компактна» эта петля — сравнивая её длину и степень выступания от белка — они обнаружили чёткое разделение на два структурных стиля. В одном подтипе петля длиннее и загибается назад по боковой части белка, образуя множество стабилизирующих контактов с набором характерных остатков. В другом подтипе петля выступает сильнее, как в традиционном фрагменте антитела. Клинические нанотела встречаются в обоих подтипах, и при сравнении десятков практических лабораторных измерений — таких как агрегация, самосоединение и термальная стабильность — не было обнаружено систематического преимущества одного стиля над другим. Это означает, что разработчикам лекарств не нужно предпочитать одну форму петли в целом, если остальные свойства приемлемы.
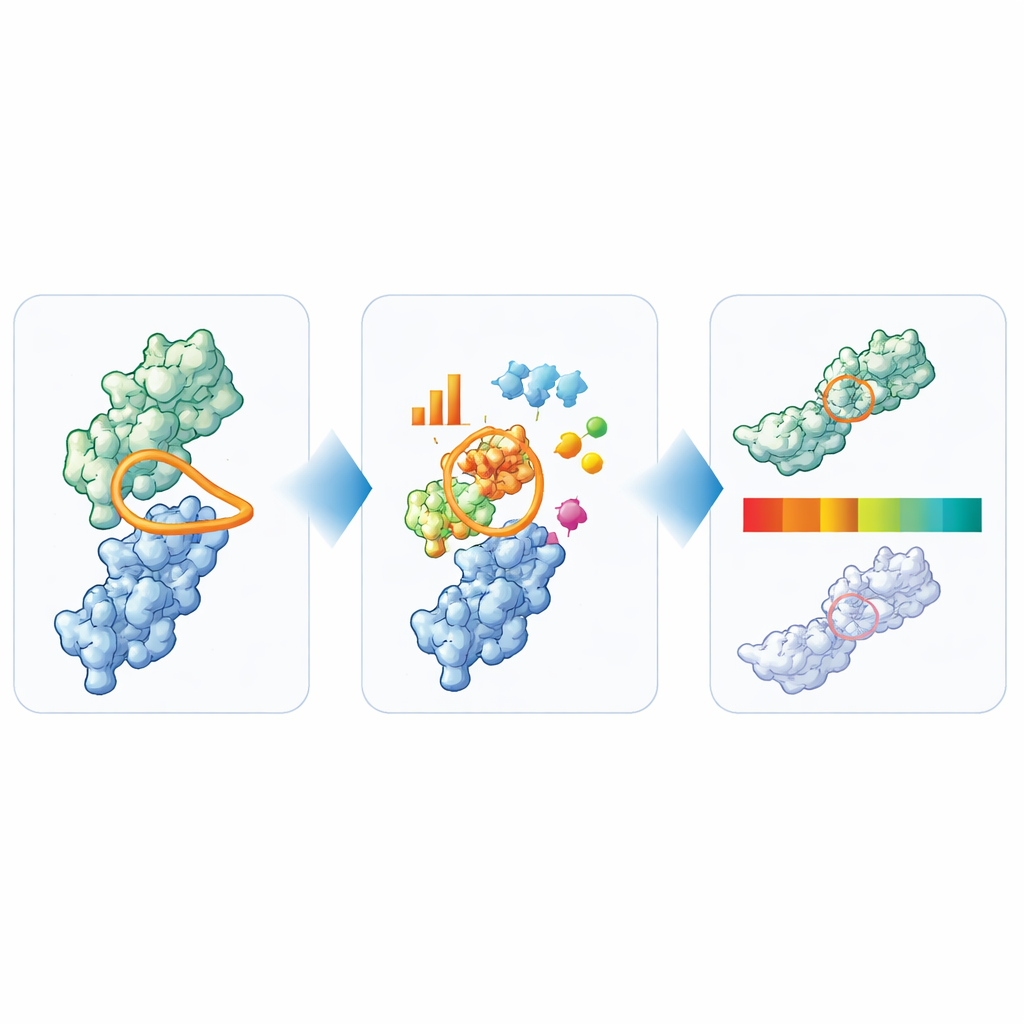
Превращение структуры в простые сигналы «светофора»
Исходя из широкого анализа, авторы выделили шесть ключевых признаков, которые в совокупности отражают основные проблемы пригодности нанотел: суммарная длина петель, специфическая длина и компактность CDR3, а также размеры гидрофобных, положительно заряженных и отрицательно заряженных поверхностных участков вокруг сайта связывания. Затем они использовали 36 нанотел, дошедших до клинических испытаний, чтобы задать практические границы для каждой меры. Значения в центральной, часто встречающейся области помечены «зелёным», пограничные значения — «оранжевым», а явные отклонения — «красным». Чтобы проверить информативность этих сигналов, они применили TNP к 72 дополнительным частным нанотелам и сравнили флаги с обширной панелью лабораторных тестов. Нанотела, которые TNP отмечал как явные выбросы, обычно также демонстрировали несколько экспериментальных предупреждающих признаков, тогда как те, что выглядели чистыми в вычислениях, чаще вели себя хорошо в лаборатории.
Что это значит для будущих терапий
Для неспециалистов основной вывод в том, что форму и рисунок поверхности нанотела теперь можно превратить в простой профиль пригодности до проведения дорогостоящих лабораторных работ. Therapeutic Nanobody Profiler не заменяет эксперименты, и несоответствия между предсказаниями и тестами по‑прежнему встречаются, особенно потому, что лабораторные исследования проводились на нанотелах, соединённых с большими фрагментами антител. Но благодаря быстрому выявлению кандидатов с необычно длинными или сильно сложенными петлями либо с проблемными поверхностными участками, TNP помогает сосредоточить внимание на нанотелах, которые с большей вероятностью станут надёжными препаратами. По мере поступления в клинику большего числа нанотел и расширения эталонного набора инструмент должен становиться ещё точнее, что ускорит разработку небольших, устойчивых антитеподобных лекарств для широкого спектра заболеваний.
Цитирование: Gordon, G.L., Gervasio, J., Souders, C. et al. Characterising nanobody developability to improve therapeutic design using the Therapeutic Nanobody Profiler. Commun Biol 9, 344 (2026). https://doi.org/10.1038/s42003-026-09594-y
Ключевые слова: нанотела, пригодность биологических препаратов, компьютерное профилирование, инжиниринг антител, стабильность белков