Clear Sky Science · ru
DTX1-опосредованное разрушение TUBB3 в клетках Купфера смягчает прогрессирование гепатоцеллюлярной карциномы через регуляцию поляризации M1/M2
Почему имеют значение «соседи» опухоли в печени
Большинство людей воспринимают рак как болезнь из-за разрастания ненормальных клеток. Но опухоли существуют в оживлённом окружении иммунных клеток, кровеносных сосудов и поддерживающей ткани, которые могут либо сражаться с раком, либо незаметно ему помогать. В этом исследовании рассмотрена печёночная карцинома — конкретно гепатоцеллюлярная карцинома — и показано, как белок внутри специализированных печёночных иммунных клеток может смещать баланс между противораковой реакцией и средой, благоприятной для опухоли. Понимание этого скрытого регуляторного переключателя может открыть новые подходы к улучшению существующих иммунотерапий.
Рак печени, управляемый окружающей средой
Печень богата иммунными клетками, включая популяцию резидентных макрофагов — клетки Купфера, которые обычно поддерживают здоровье органа. При раке печени многие из этих клеток преобразуются в макрофаги, ассоциированные с опухолью, которые могут либо атаковать рак (состояние, напоминающее M1), либо защищать его (состояние, похожее на M2). Пациенты, у которых опухоль насыщена макрофагами типа M2, как правило, имеют худший прогноз и часто хуже отвечают на препараты, снимающие иммунные тормоза, такие как ингибиторы PD‑1. Авторы начали с анализа публичных геномных баз и образцов пациентов в поисках молекул, связанных одновременно с раком печени и этими макрофагами, и сосредоточились на структурном белке TUBB3, который оказался неожиданно обильно представлен в опухолевой ткани.
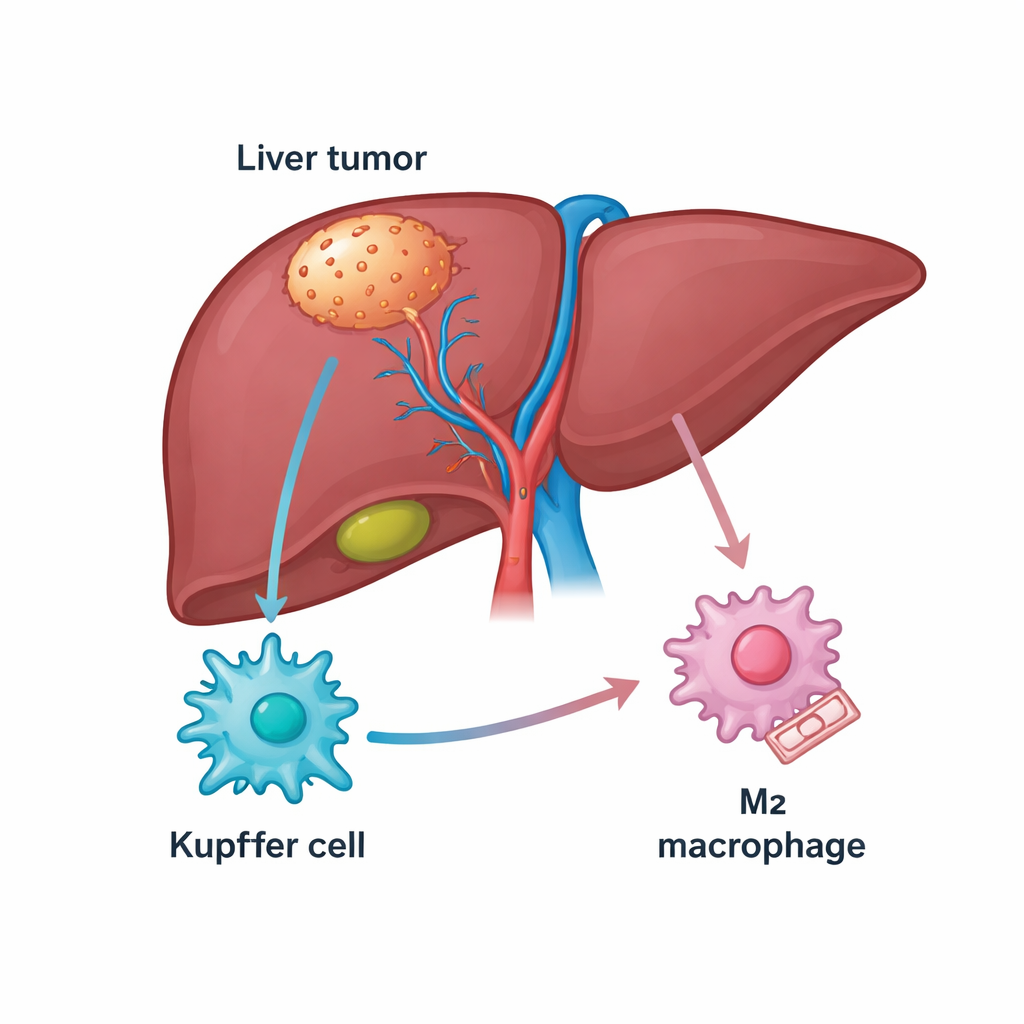
Неожиданный белок, подталкивающий иммунные клетки к поддержке опухоли
TUBB3 прежде всего известен как строительный компонент мельчайших «рельсов» внутри клеток, однако его также связывали с агрессивным поведением и лекарственной устойчивостью при нескольких видах рака. В этой работе исследователи обнаружили, что уровни TUBB3 значительно выше в опухолях печени по сравнению с прилежащей здоровой тканью, и что у пациентов с большим количеством TUBB3 выживаемость была ниже. С помощью методов окрашивания они показали, что TUBB3 особенно накоплен в клетках Купфера внутри опухолей, и его присутствие тесно коррелировало с маркерами опухоль-помогающего состояния M2. Иными словами, клетки Купфера с высоким содержанием TUBB3 чаще вели себя так, что притупляло иммунную атаку и поддерживало рост опухоли.
Перепрограммирование макрофагов для сдерживания опухолей печени
Чтобы проверить причинно-следственную связь, команда снизила уровни TUBB3 в клетках Купфера в лабораторных экспериментах. При подавлении TUBB3 эти клетки производили меньше сигналов типа M2, больше — типа M1, и секретировали меньше молекул, которые обычно подавляют иммунную активность. Раковые клетки печени, подвергшиеся воздействию таких перепрограммированных макрофагов, росли медленнее, делились реже и хуже мигрировали и проникают в ткань. У мышей смешивание раковых клеток печени с клетками Купфера, лишёнными TUBB3, приводило к меньшим опухолям, большему числу погибающих раковых клеток и повышенному притоку киллерных CD8 T-клеток, оснащённых цитотоксическими белками. Если макрофаги полностью удаляли у животных, эффект от блокирования TUBB3 в значительной степени исчезал, что подчёркивает, что действие проходит через эти иммунные клетки, а не только через раковые клетки.
Выявление внутреннего «тормоза» на ключевом сигнальном пути
Исследование также изучало, как именно TUBB3 оказывает такое влияние. Авторы сосредоточились на известном пути роста и выживания, контролируемом белками PTEN и AKT, который также определяет, примут ли макрофаги идентичность M1 или M2. Они обнаружили, что снижение TUBB3 повышает PTEN, что, в свою очередь, снижает фосфорилирование (активирующие «фосфатные метки») AKT, подталкивая макрофаги к антиопухолевому состоянию. Когда AKT искусственно повторно активировали, макрофаги снова принимали паттерн M2, а раковые клетки восстанавливали агрессивное поведение, даже при отсутствии TUBB3. Это помещает TUBB3 выше по иерархии относительно PTEN и AKT, как своего рода внутренний регулятор поведения макрофагов.
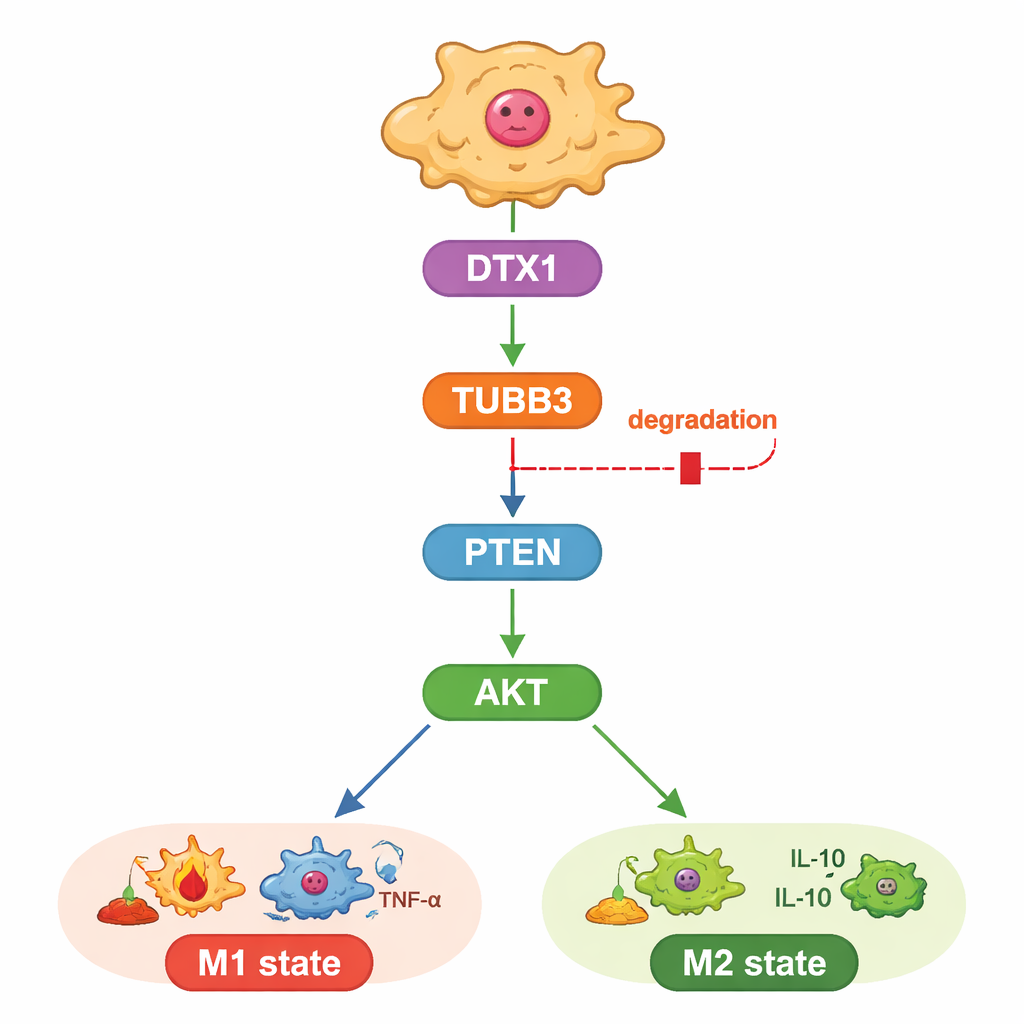
Встроенный «тег для мусора», который можно вновь включить
Наконец, исследователи задали вопрос, почему TUBB3 так много в опухолях печени. Сочетая биоинформатические прогнозы с данными об экспрессии, они выделили фермент DTX1, принадлежащий к семейству белков, помечающих молекулы для утилизации, как вероятного регулятора. Уровни DTX1 были ниже в опухолях печени по сравнению со здоровой тканью и связаны с лучшими исходами у пациентов и с большим присутствием макрофагов типа M1. В клетках повышение DTX1 ускоряло распад TUBB3, ослабляло активность AKT и сдвигало макрофагов в антиопухолевое состояние, сдерживая рост раковых клеток. Восстановление эффекта за счёт повторного введения лишнего TUBB3 стирало преимущества DTX1 как в культурах, так и в опухолях у мышей. В совокупности результаты проводят чёткую линию от DTX1 через TUBB3 и PTEN/AKT к иммунному тону опухоли.
Что это значит для будущего лечения рака печени
Для неспециалистов ключевое послание таково: работа выявляет ранее скрытую систему контроля внутри резидентных печёночных иммунных клеток, которая решает, помогают ли они или препятствуют раку. Когда фермент, помечающий для утилизации DTX1, снижен, TUBB3 накапливается, включается путь роста, и клетки Купфера смещаются в режим поддержки опухоли, ослабляя эффект иммунотерапии. Восстановление этой цепочки — за счёт снижения TUBB3, повышения DTX1 или точной коррекции сигнала PTEN/AKT — может пробудить локальные иммунные механизмы и повысить эффективность таких препаратов, как ингибиторы PD‑1. Хотя такие стратегии пока находятся на экспериментальной стадии, они подчёркивают перспективу лечения не только самих раковых клеток, но и окружающих их иммунных «соседей», которые существенно влияют на поведение рака печени.
Цитирование: Sun, J., Sun, T., Zhang, Y. et al. DTX1-mediated degradation of TUBB3 in Kupffer cells mitigates hepatocellular carcinoma progression by regulating M1/M2 polarization. Commun Biol 9, 311 (2026). https://doi.org/10.1038/s42003-026-09593-z
Ключевые слова: гепатоцеллюлярная карцинома, макрофаги, ассоциированные с опухолью, клетки Купфера, иммунотерапия, сигналинг AKT