Clear Sky Science · ru
Разрежение и декаорреляция активности гранулярных клеток в зубчатой извилине под действием норадреналина
Почему вспышка возбуждения может сделать воспоминания яснее
Моменты, которые внезапно будят нас — едва избежанная авария, неожиданный комментарий, неожиданный поворот сюжета в фильме — часто запоминаются лучше, чем обычный день. Это исследование объясняет одну ключевую причину: химическое вещество мозга, связанное с возбуждением, норадреналин незаметно меняет способ, которым важный «фильтр» памяти в гиппокампе отбирает и разделяет впечатления, помогая легче отличать похожие события позже.
Воротник мозга для похожих впечатлений
Внутри гиппокампа расположена зубчатая извилина, область, выступающая в роли воротника для новых воспоминаний. Она получает обширную информацию от энторинальной коры — сигналы о том, где мы находимся и что вокруг происходит — и преобразует их в паттерны активности в гранулярных клетках, своих основных нейронах. Теория и эксперименты показывают, что эти паттерны должны быть «разреженными» (активны только немногие клетки одновременно) и «декоррелированными» (разные переживания активируют разные наборы клеток), чтобы воспоминания не сливались. Тем не менее, как именно это преобразование выполняется на уровне отдельных клеток и схем было неясно.
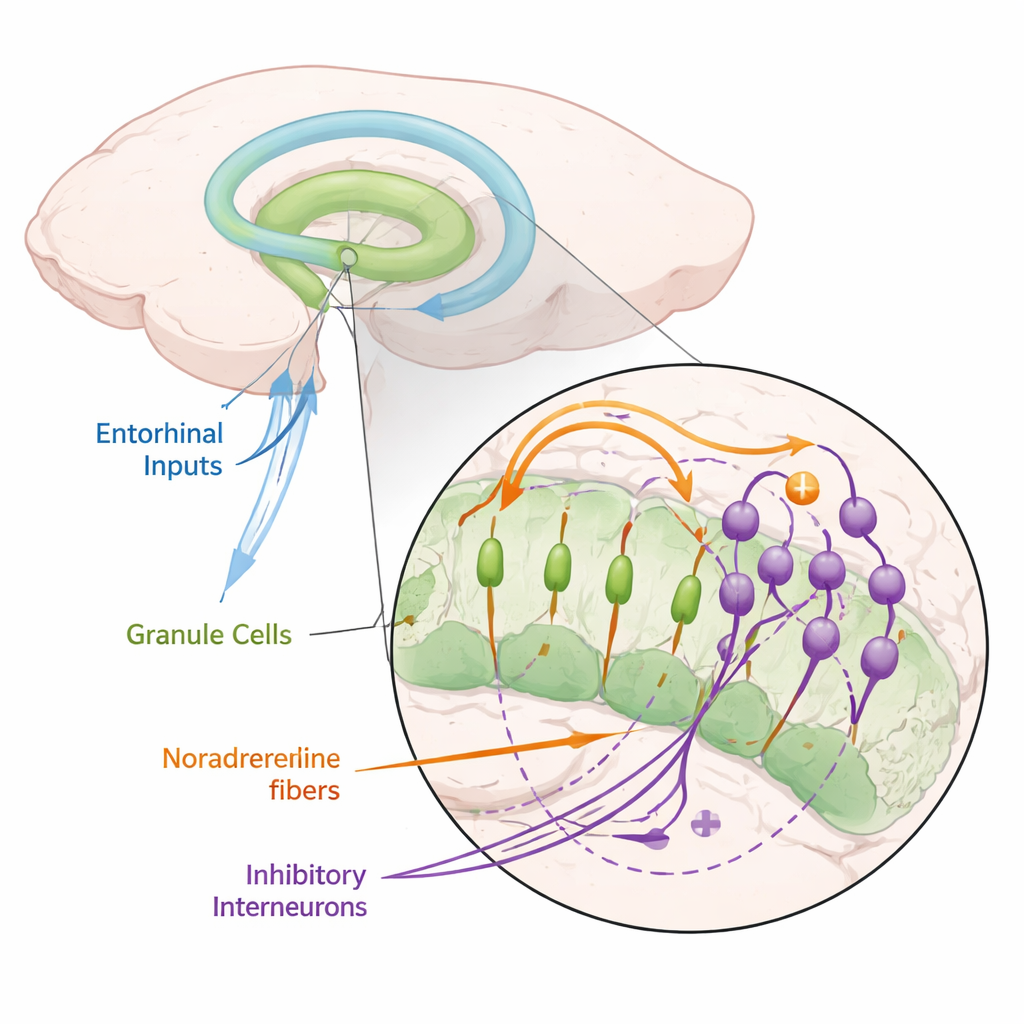
Химический фактор возбуждения, который притормаживает ключевые клетки памяти
Авторы сосредоточились на норадреналине — нейромодуляторе, выделяемом нейронами небольшой стволовой области, называемой голубым пятном (locus coeruleus), который активируется при внимании, новизне и стрессе. На мышах они экспрессировали светочувствительные белки в этих норадренергических нейронах, что позволяло высвобождать норадреналин по команде вспышками света. Стимулируя главный входной путь к зубчатой извилине и записывая активность гранулярных клеток, исследователи обнаружили, что высвобождение норадреналина сильно снижало склонность этих клеток к спайкингу. Это подавление проявлялось как на уровне отдельных нейронов, так и в популяционных сигналах, и воспроизводилось при простом добавлении норадреналина в раствор срезов. Блокировка рецепторов норадреналина устраняла эффект, что показало, что он действительно зависел от этого химического посредника.
Не слабее возбуждение, а сильнее тормоза
Чтобы понять, как норадреналин «заглушал» гранулярные клетки, команда проверила очевидные варианты. Он существенно не изменял потенциал покоя или входное сопротивление гранулярных клеток, то есть их базовая возбудимость оставалась примерно прежней. Также он не ослаблял возбуждающие токи, которые эти клетки получают от энторинальной коры. Вместо этого при блокаде GABAA-рецепторов, через которые опосредовано торможение, норадреналин уже не мог подавлять спайкинг гранулярных клеток. Детальные измерения токов показали, что норадреналин селективно усиливал быстрый, прямой (feedforward) тип торможения: входящие возбуждающие сигналы сначала активировали набор интернейронов, которые затем быстро подавляли гранулярные клетки до того, как те успевали выдать спайк. Анализ временных соотношений показал, что этот чувствительный к норадреналину тормозной ток приходил сразу после прямого возбуждения, но до того, как основная популяция гранулярных клеток выстреливала, что является признаком именно прямого (feedforward) тормоза.
Специализированные тормозные клетки, которые задают точность по времени
Какие же интернейроны обеспечивали это решающее торможение? Вопреки ожиданиям, клетки, экспрессирующие парвальбумин, которые долгое время считались доминирующими в быстром feedforward-контроле, не были виновниками — норадреналин фактически делал их менее активными. Вместо них ключевыми игроками оказались интернейроны, экспрессирующие холецистокинин (CCK-клетки). Эти клетки получают прямой вход от тех же корковых волокон, которые возбуждают гранулярные клетки, и активируются чуть раньше гранулярных клеток, указывая на feedforward-роль. Норадреналин деполяризовал CCK-клетки, делая их легче наборными, и увеличивал частоту, с которой входные сигналы их вызывали, не меняя при этом силы каждой отдельной тормозной связи. Когда исследователи фармакологически блокировали выход CCK-клеток, норадреналин уже не мог подавлять активность гранулярных клеток. По сути, норадреналин включает схему CCK-интернейронов, которая накладывает очень узкое временное окно, в течение которого входящие возбуждающие спайки могут успешно вызвать ответ гранулярных клеток.
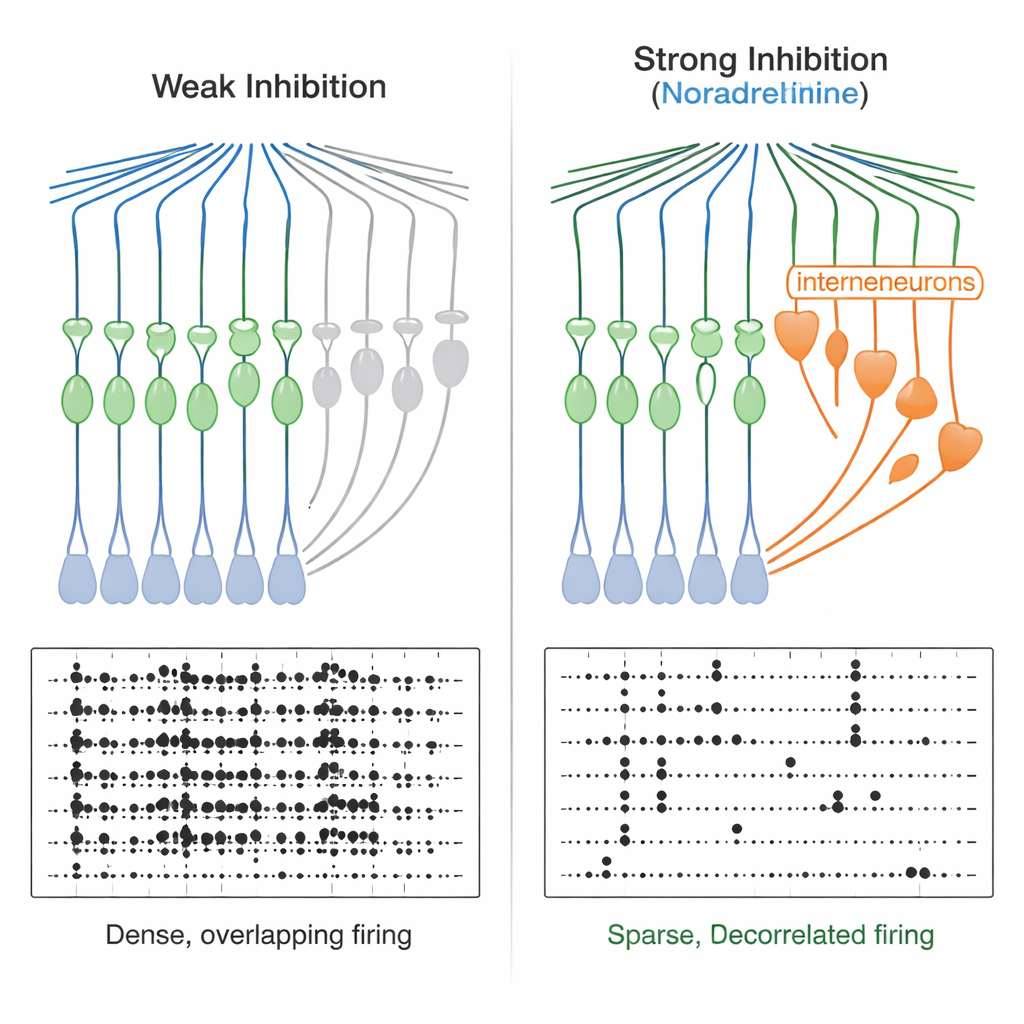
От узких окон к чище кодам памяти
Это сузившееся по времени окно имеет мощные последствия. Когда команда подавала пары кратких возбуждающих входов, они заметили, что в нормальных условиях гранулярные клетки могли интегрировать входы, разнесённые на десятки миллисекунд, в единичный спайк. В присутствии норадреналина окно сжалось до всего нескольких миллисекунд — гранулярные клетки стали реагировать почти исключительно на высоко синхронизированные входы. Вычислительные сетевые модели подтвердили, что усиление и ускорение feedforward-торможения даёт более разреженный выход и уменьшает перекрытия между паттернами активности, улучшая «декорреляцию». Экспериментально, когда исследователи подавали в зубчатую извилину два похожих, но не идентичных входных паттерна, гранулярные клетки отвечали более различимыми схемами спайкинга в присутствии норадреналина, как в записях одиночных клеток, так и в кальциевой визуализации по многим клеткам. Одновременно общая активность гранулярных клеток становилась более разреженной.
Как возбуждение помогает разделять похожие воспоминания
Для неспециалиста главный вывод таков: норадреналин, выделяемый, когда мы настороже или эмоционально вовлечены, делает ключевой фильтр памяти в гиппокампе более разборчивым. Активируя специфический класс тормозных нейронов, он сужает временное окно, в течение которого входы могут вызвать гранулярные клетки, так что проходят лишь тесно синхронизированные, значимые сигналы. Это снижает общую частоту спайкинга, уменьшает перекрытие паттернов активности и помогает мозгу сохранять похожие впечатления — например, две аудитории или два разговора — как отдельные воспоминания, а не как неясную мешанину. Работа выявляет конкретный схемный механизм, связывающий кратковременное возбуждение с более точными, менее путаемыми воспоминаниями.
Цитирование: Glovaci, I., Mihály, A., Vervaeke, K. et al. Sparsification and decorrelation of granule cell activity in the dentate gyrus by noradrenaline. Commun Biol 9, 323 (2026). https://doi.org/10.1038/s42003-026-09592-0
Ключевые слова: норадреналин, зубчатая извилина, тормозные интернейроны, разделение шаблонов, эпизодическая память