Clear Sky Science · ru
Структурные данные о хеликазе WRN показывают конформационные состояния и открывают возможности для разработки лекарств против MSI‑H рака
Почему это важно для лечения рака
Некоторые виды рака имеют встроенную уязвимость: им трудно исправлять ошибки в ДНК. Белок WRN‑хеликаза действует как молекулярный инструмент ремонта, поддерживая жизнь этих хрупких опухолей. В этом исследовании на атомном уровне показано, как WRN перемещается по ДНК и как экспериментальные препараты могут блокировать его движение — что дает дорожную карту для создания новых препаратов, направленных на избирательное уничтожение уязвимых раковых клеток при минимальном вреде для здоровых тканей.
Мастер по работе с ДНК под микроскопом
Хеликаза WRN — часть «обслуживающей бригады» клетки, помогающая развернуть ДНК, чтобы повреждения можно было обнаружить и исправить. Люди, рожденные без функционирующего WRN, развивают синдром Вернера — редкое заболевание с преждевременным старением, что подчеркивает ключевую роль этого белка в поддержании генома. Опухоли с высокой микросателлитной нестабильностью (MSI‑H) — частая проблема при колоректальном и некоторых других раках — особенно зависят от WRN. При подавлении WRN в этих клетках их и без того нестабильная ДНК быстро распадается, и раковые клетки гибнут. Это делает WRN привлекательной мишенью для лекарств, но до сих пор ученым не хватало ясного представления о том, как белок меняет форму при захвате ДНК, расходовании химической энергии и движении вдоль генетического материала.
Наблюдая, как WRN сгибается и «дышит»
Авторы использовали рентгеновскую кристаллографию, чтобы зафиксировать несколько высокоразрешающих «снимков» ядра человеческой хеликазы WRN. Они определили структуры WRN в свободном состоянии и в комплексе с однонитевой ДНК и нерасщепляемым аналогом топлива ATP. Эти изображения показали, что белок собран из двух основных лопастей, соединенных гибким шарниром, который действует как «дышащий» сустав. В состоянии покоя без топлива WRN принимает компактную «закрытую» форму, в которой лопасти расположены близко друг к другу. При наличии аналогов ATP и ДНК лопасти раздвигаются в более «открытую» конфигурацию, способную удерживать ДНК в положительно заряженной борозде. Небольшая ароматическая петля внутри WRN перестраивается в короткую спираль и поджимается между основаниями ДНК, действуя как храповик — она помогает белку делать шаг вперед, не соскальзывая назад.
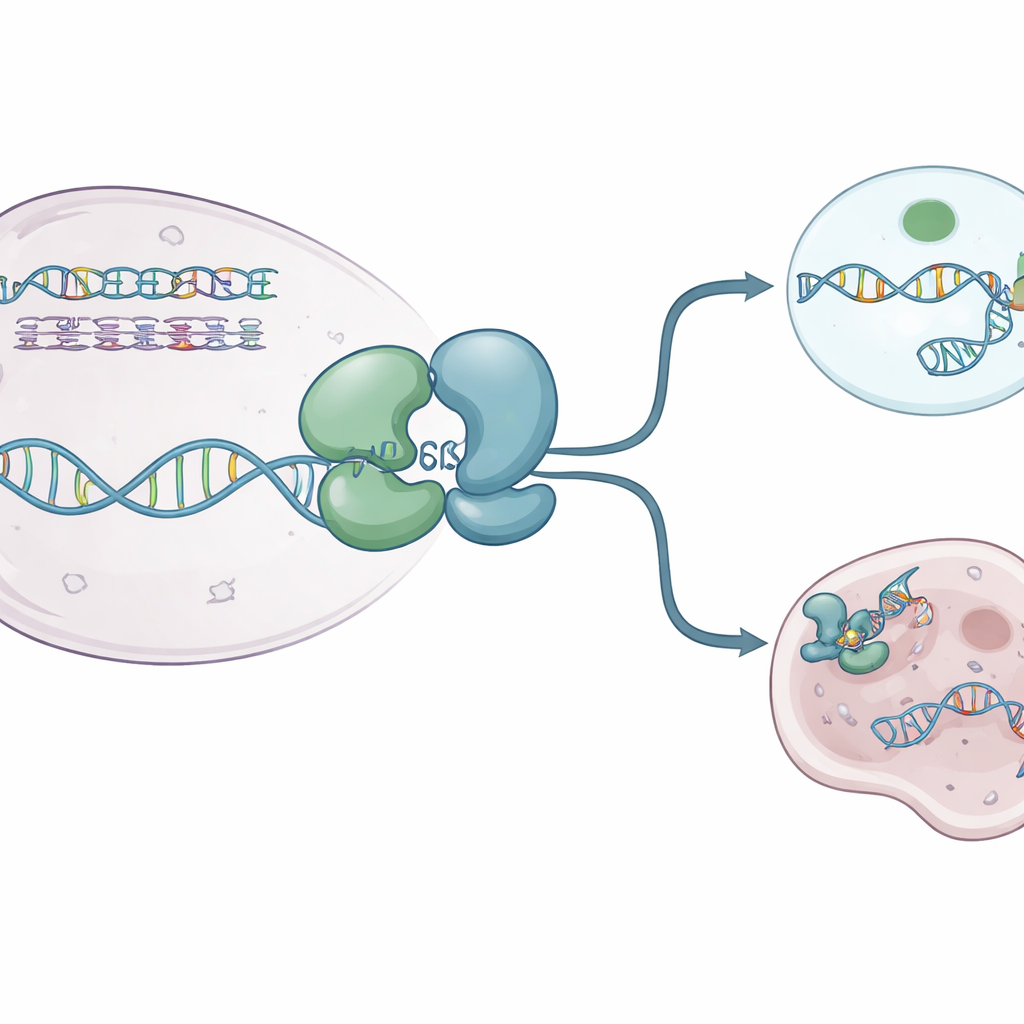
Как современные препараты выключают WRN
Несколько соединений, блокирующих WRN, недавно вошли в клинические испытания. Они не забивают активную борозду белка напрямую. Вместо этого они действуют издалека, захватывая область шарнира и фиксируя WRN в формах, неспособных правильно взаимодействовать с ДНК. Некоторые молекулы, такие как HRO761 и связанный клинический кандидат от GSK, поворачивают одну лопасть примерно на 180 градусов относительно другой, создавая впечатляющую «скрученную» форму, находящуюся вне ДНК. Другие, включая VVD‑133214 и близкое к нему соединение, изученное здесь, фиксируют WRN в туго «закрытом» состоянии, которое не обнажает ключевые поверхности для удержания ДНК. Биофизические эксперименты подтвердили, что в связанном состоянии WRN больше не способен образовывать стабильный комплекс с однонитевой ДНК, эффективно разрывая связь между расходом ATP и расплетением ДНК.
Как раковые клетки учатся уходить от действия препаратов
Чтобы понять, как опухоли могут избежать действия этих препаратов, команда выращивала MSI‑H колоректальные раковые клетки в присутствии ингибиторов WRN в течение недель и месяцев. Быстро возникли популяции, устойчивые к препаратам. Генетический анализ показал, что в каждом случае клетки приобрели одну точную замену в гене WRN рядом с участком связывания препарата у шарнира. Одна мутация ослабляла эффект ингибитора «скрученого» состояния HRO761, тогда как другая мутация снижала чувствительность к VVD‑133214, который стабилизирует закрытую форму. Кроме того, многие устойчивые клетки усиливали производство WRN, обеспечивая себе больше копий мишени и частично разводя эффект препарата. Эти наблюдения перекликаются с шаблонами резистентности, известными для других таргетных противораковых препаратов, где небольшие структурные изменения в белке‑мишени или сверхэкспрессия могут ослаблять терапию.
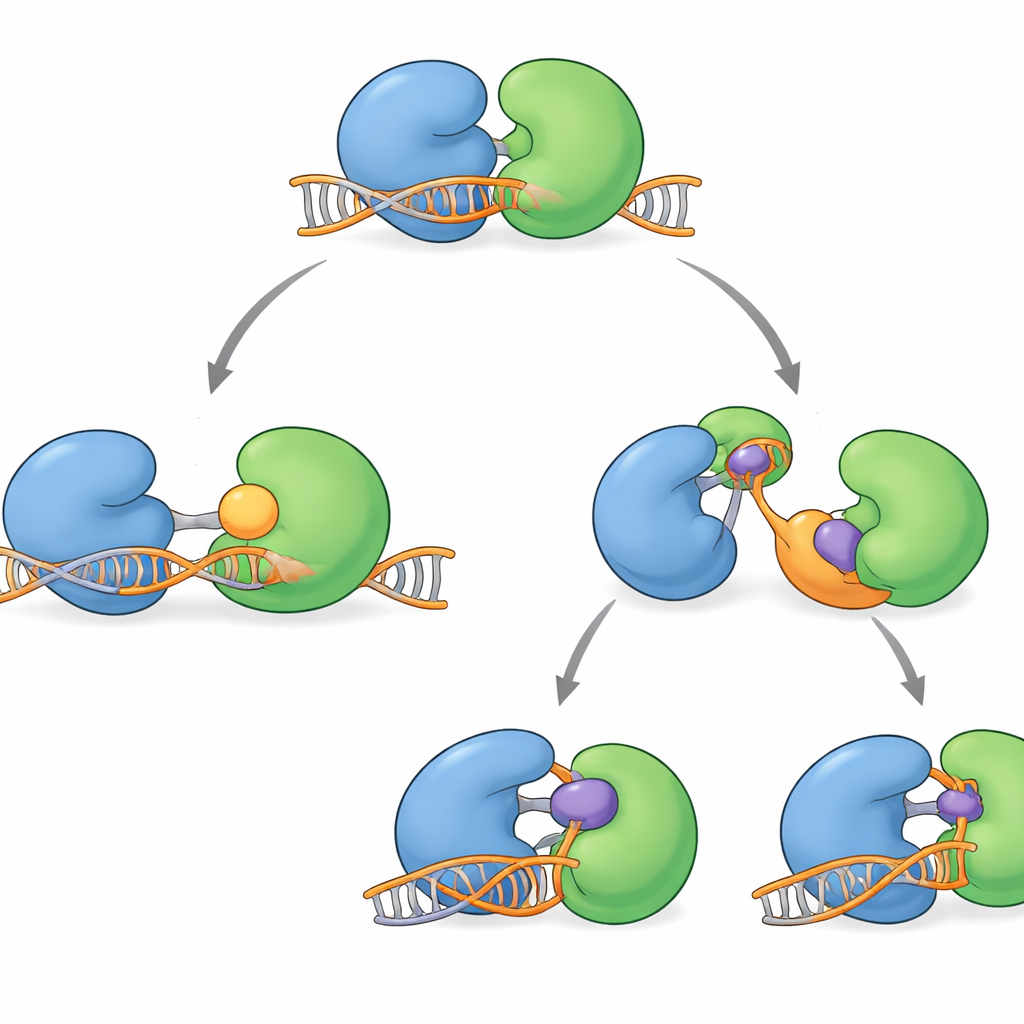
Взгляд в будущее: более умные блокаторы WRN
В совокупности новые структуры отображают полный рабочий цикл WRN: как он захватывает ДНК, делает шаги и затем сбрасывается. Они также показывают, что современные клинические соединения в основном стабилизируют «вне‑ДНК» формы белка. Главное для широкой аудитории — теперь мы понимаем, где WRN уязвим и как опухоли могут адаптироваться. Это указывает на следующий виток разработки ингибиторов, которые связывают WRN в тот момент, когда он зафиксирован на ДНК, потенциально «запирая» его в токсическом состоянии — подобно успешным препаратам, которые захватывают другие ферменты репарации ДНК. Такие «on‑DNA» ингибиторы WRN, применяемые отдельно или в сочетании с существующими средствами, могут предложить более устойчивые способы использования скрытой слабости MSI‑H опухолей.
Цитирование: Fletcher, C.T., Mornement, A.A., Barrett, C. et al. Structural insights into WRN helicase reveal conformational states and opportunities for MSI-H cancer drug discovery. Commun Biol 9, 334 (2026). https://doi.org/10.1038/s42003-026-09584-0
Ключевые слова: хеликаза WRN, микросателлитная нестабильность, репарация ДНК, аллостерические ингибиторы, лекарственная резистентность