Clear Sky Science · ru
PiR48444 ингибирует остеогенную дифференцировку МСК и регенерацию кости через нацеливание на METTL7A/eIF4E-зависимую m6A-метилирование BMP2
Почему крошечные молекулы важны для заживления переломов
Переломы и возрастная потеря костной ткани — распространённые проблемы, и врачи стремятся использовать стволовые клетки, чтобы помочь организму восстановить повреждённый скелет. Однако эти клетки не всегда столь эффективно формируют новую кость, как хотелось бы, особенно у пожилых людей или при воспалении тканей. В этом исследовании обнаружена небольшая РНК-молекула, названная piR48444, которая действует как молекулярный тормоз для костеобразующих стволовых клеток. Сняв этот тормоз, учёные показывают, что можно повысить способность к восстановлению кости и защитить от её потери.
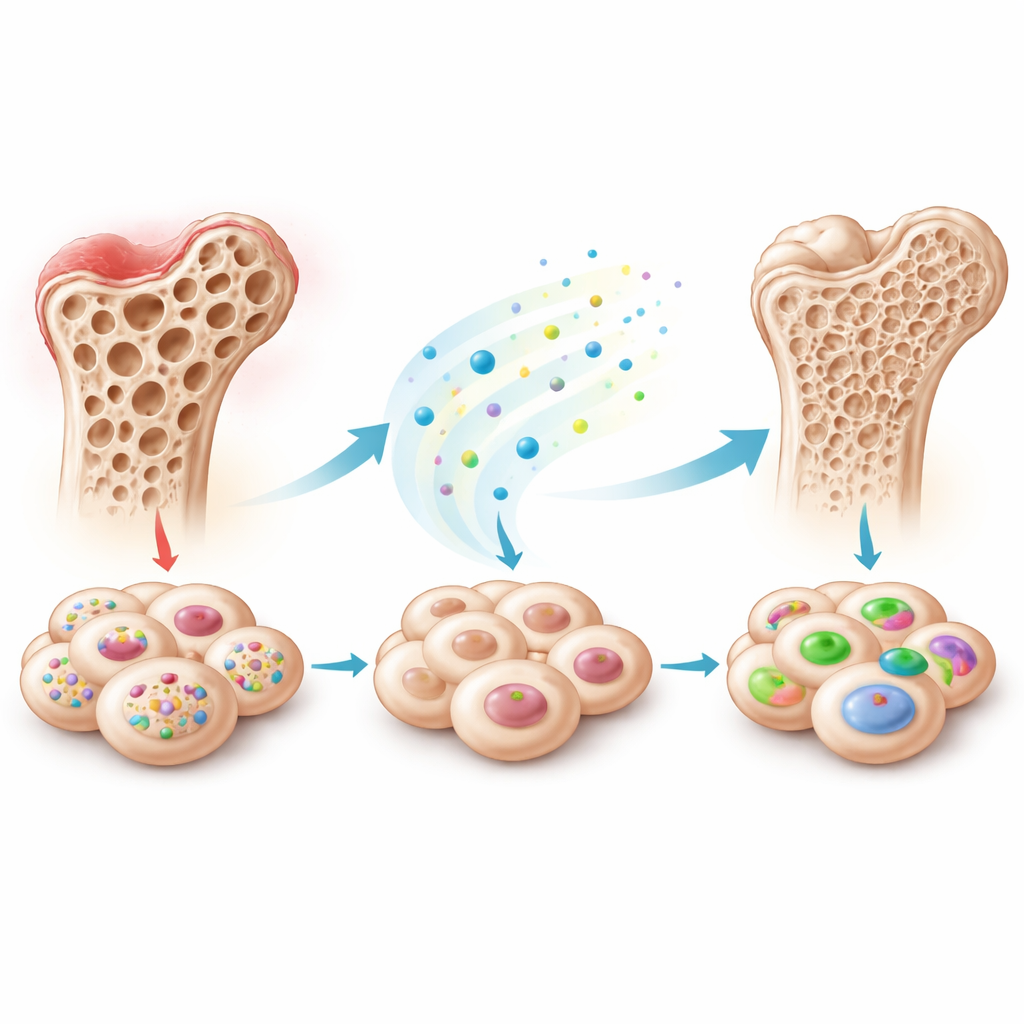
Скрытый тормоз в разных типах стволовых клеток
Команда сосредоточилась на мезенхимальных стволовых клетках — универсальных клетках, которые могут превращаться в кость, хрящ, жировую ткань и другие типы, и которые выделяются из различных тканей, таких как костный мозг, молочные зубы и жир. При индукции остеогенеза в лаборатории активность тысяч генов и малых РНК изменяется. Секвенируя эти молекулы в стволовых клетках из эксфолированных молочных зубов, исследователи обнаружили, что одна малая РНК, piR48444, стабильно снижалась по мере перехода клеток к костной траектории. Затем они проверили другие типы стволовых клеток и увидели ту же закономерность: в клетках с повышенным остеогенезом было меньше piR48444, что наводит на мысль, что эта молекула обычно сдерживает их способность образовывать кость.
От чашек Петри до живых костей
Чтобы проверить эту идею, учёные изменили уровень piR48444 в нескольких типах стволовых клеток. При снижении piR48444 клетки откладывали больше кальция, включали гены, связанные с образованием кости, и под микроскопом напоминали незрелую костную ткань. При вынужденной экс-прессии piR48444 наблюдалось обратное: активность, связанная с костеобразованием, уменьшалась. Дальше команда перешла к моделям на животных. Стволовые клетки с выключенной piR48444 использовали для заполняния небольших дефектов черепа у мышей. Эти модифицированные клетки давали значительно больше новой кости по сравнению с контрольными, что демонстрировалось 3D-рентгеном и окрашиванием тканей, что свидетельствует о том, что блокирование piR48444 реально улучшает заживление костей в живом организме.
Защита хрупкой кости при заболеваниях и старении
Потеря костной ткани обусловлена не только травмами, но и воспалением и старением. В стволовых клетках костного мозга, подвергнутых действию бактериальных токсинов, а также в клетках от старых животных уровни piR48444 были аномально высоки, тогда как маркеры костеобразования снижены. Исследователи создали «антагомир» — короткую молекулу, предназначенную для нейтрализации piR48444 в крови, — и вводили её мышам с воспалением, вызывающим потерю кости, или естественно старым мышам. В обоих моделях лечёные животные сохраняли намного больше губчатой внутренней кости с более плотными и многочисленными тонкими костными балками, тогда как плотная наружная оболочка кости оставалась без изменений. Это указывает на то, что блокирование piR48444 может избирательно защитить хрупкую, метаболически активную часть скелета, наиболее уязвимую при старении и хроническом воспалении.
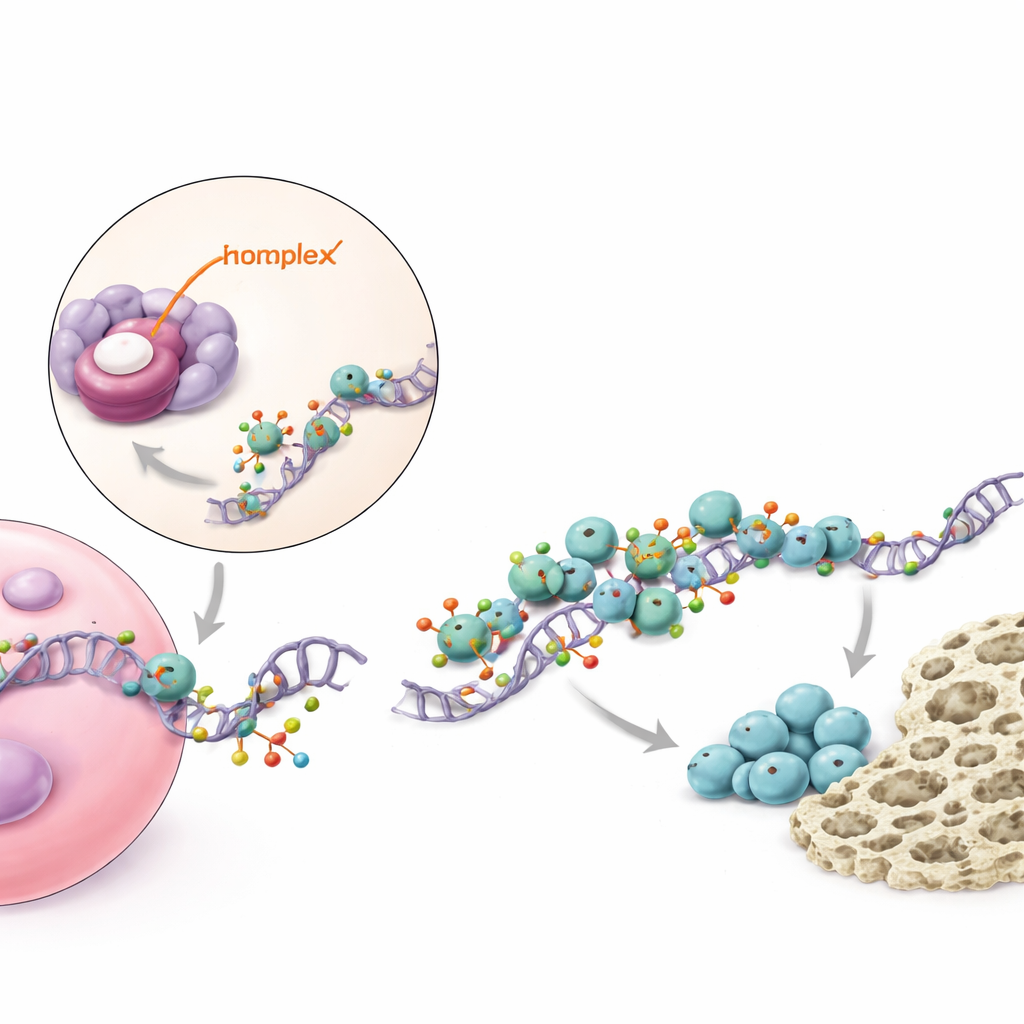
Молекулярная передача, усиливающая ключевой костный сигнал
Углубившись, исследование картировало, как piR48444 реализует свои эффекты внутри клеток. Малая РНК связывается и подавляет белок METTL7A, который функционирует как фермент, модифицирующий матричные РНК, несущие шаблон для BMP2 — хорошо известного фактора роста, который сильно стимулирует образование кости. METTL7A добавляет небольшие химические метки к сообщениям BMP2, делая их более стабильными и легче читаемыми белковых машин клетки. METTL7A также взаимодействует с другим белком, eIF4E, который помогает инициировать синтез белка. Когда piR48444 в избытке, METTL7A подавлен, меньше сообщений BMP2 модифицировано и транслируется, и производится меньше белка BMP2, поэтому стволовые клетки реже превращаются в кость. Когда piR48444 блокируется, уровни METTL7A и BMP2 увеличиваются, сдвигая клетки в сторону остеогенеза.
Что это значит для будущего восстановления кости
Проще говоря, авторы показывают цепочку регуляции, где малая РНК (piR48444) ослабляет вспомогательный фермент (METTL7A), который, в свою очередь, ограничивает мощный сигнал костеобразования (BMP2). Перерывая эту цепь на уровне piR48444, можно повысить способность различных стволовых клеток формировать кость и уменьшить потерю кости у мышей. Хотя безопасность, эффекты вне цели и долгосрочные последствия требуют тщательной проверки, работа указывает на piR48444 как на потенциальный маркер в крови для оценки риска остеопороза и как перспективную мишень для препаратов, направленных на усиление регенерации кости с помощью стволовых клеток в клинике.
Цитирование: Zheng, Z., Li, X., Qin, W. et al. PiR48444 inhibits MSC osteogenic differentiation and bone regeneration via targeting METTL7A/eIF4E-mediated BMP2 m6A methylation. Commun Biol 9, 337 (2026). https://doi.org/10.1038/s42003-026-09583-1
Ключевые слова: регенерация кости, мезенхимальные стволовые клетки, остеопороз, некодирующая РНК, сигнализация BMP2