Clear Sky Science · ru
Локальная фиксация катионов искажает и размягчает дуплекс РНК
Почему этот крохотный поворот в РНК важен
Внутри каждой клетки ДНК и РНК постоянно сгибаются, растягиваются и закручиваются, когда хранят и используют генетическую информацию. Эти движения — не просто механические детали: они контролируют, как считываются гены, как вирусы копируют себя и как будут работать новые лекарства и наноустройства на основе РНК. В этом исследовании показано, что простые соли из положительно и отрицательно заряженных ионов могут драматически менять жесткость или гибкость РНК, и что РНК реагирует на это совершенно иначе, чем ДНК. Понимание этой тонкой «песни размягчения и упрочнения» может помочь учёным лучше проектировать РНК‑лекарства, вакцины и молекулярные инструменты.
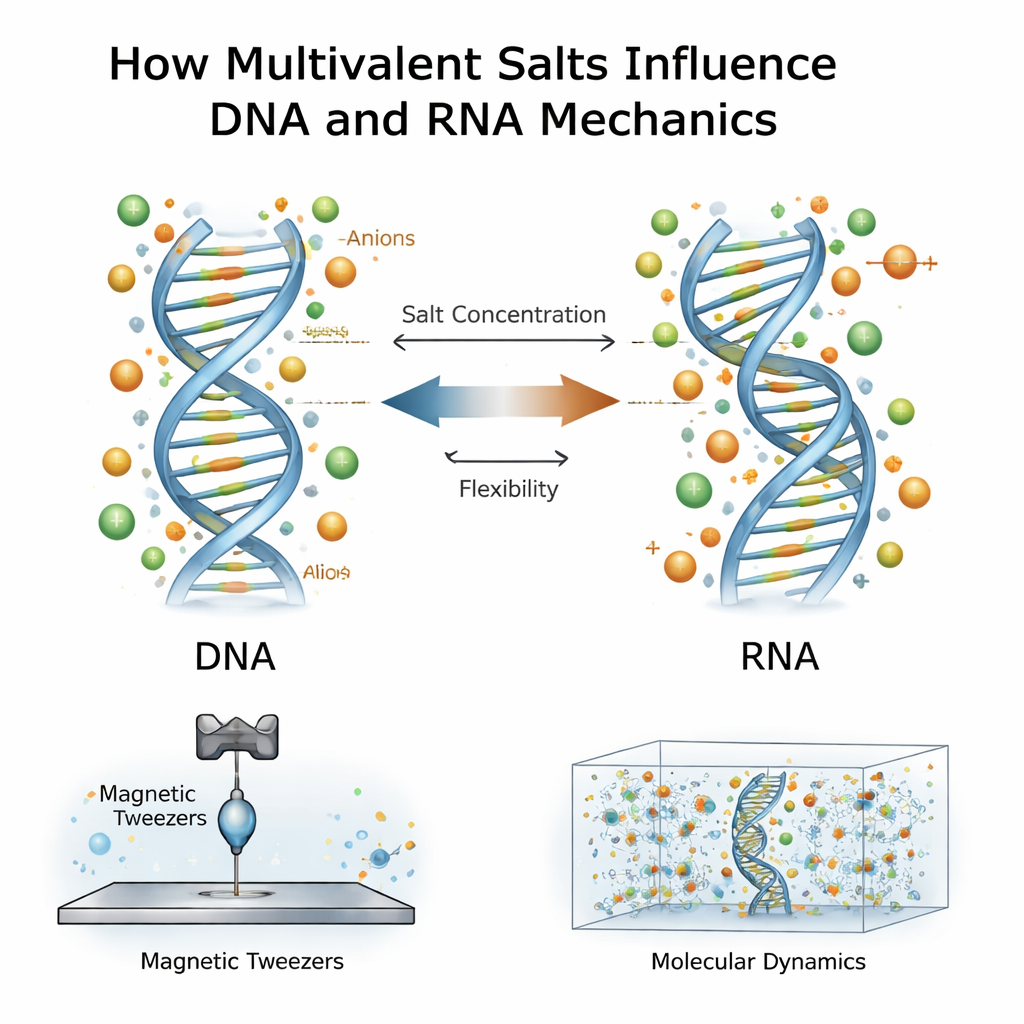
Солёное окружение и генетические молекулы
ДНК и РНК несут сильный отрицательный электрический заряд, поэтому в воде вокруг них формируются облака противоположно заряженных ионов. Большая часть предыдущих работ сосредотачивалась на положительных ионах, особенно на мультивалентных, которые несут два или три положительных заряда, таких как магний или спермин. Известно, что эти ионы удерживают нити ДНК вместе, конденсируют их или меняют их лёгкость изгиба. РНК, хотя и химически похожа на ДНК, ведёт себя иначе: её обычно труднее согнуть, но легче растянуть. Новая работа задаёт более глубокий вопрос: что происходит, когда и положительные ионы, и их сопровождающие отрицательные партнёры — анионы — взаимодействуют с ДНК и РНК при очень высоких уровнях соли, значительно выше тех, что встречаются в типичной клетке?
Тянем за одиночные молекулы, чтобы измерить жёсткость
Исследователи использовали метод, называемый магнитными пинцетами, чтобы растягивать отдельные двойные спирали ДНК или РНК по одной. Каждая молекула была закреплена на стеклянной подложке с одного конца и на крошечной магнитной бусине с другого. Перемещая магниты над образцом, они могли прикладывать контролируемые силы и записывать, насколько удлинялась каждая молекула и как она закручивалась под натяжением. По этим кривым «сила — удлинение» они извлекли четыре ключевых механических характеристики: насколько трудно изгибать молекулу, насколько трудно её растянуть, эффективная длина на пару оснований и как скручивание меняет её длину. Эти измерения повторяли при широком диапазоне концентраций мультивалентных солей для нескольких различных солей, включая спермин и хлорид кальция.
ДНК снова уплотняется, а РНК вдруг размягчается
Для ДНК поведение в целом соответствовало ожиданиям. По мере увеличения концентрации мультивалентных положительных ионов ДНК сначала становилась легче для изгиба — её жёсткость падала — потому что ионы нейтрализовали её отрицательный заряд. При ещё более высоких уровнях избыток положительных ионов перекрывал заряд, фактически меняя знак суммарного заряда ДНК. Эта «инверсия заряда» делала ДНК снова более жёсткой, поэтому её жёсткость росла. Удивительно, что РНК показала противоположную и более драматичную картину. При низких и умеренных концентрациях её жёсткость при изгибе увеличивалась: дуплекс РНК выпрямлялся и становился более жёстким. Но при очень высоких концентрациях жёсткость изгиба РНК падала более чем вдвое, а другие свойства, такие как растяжимость и взаимосвязь скручивания и удлинения, менялись неожиданным образом.
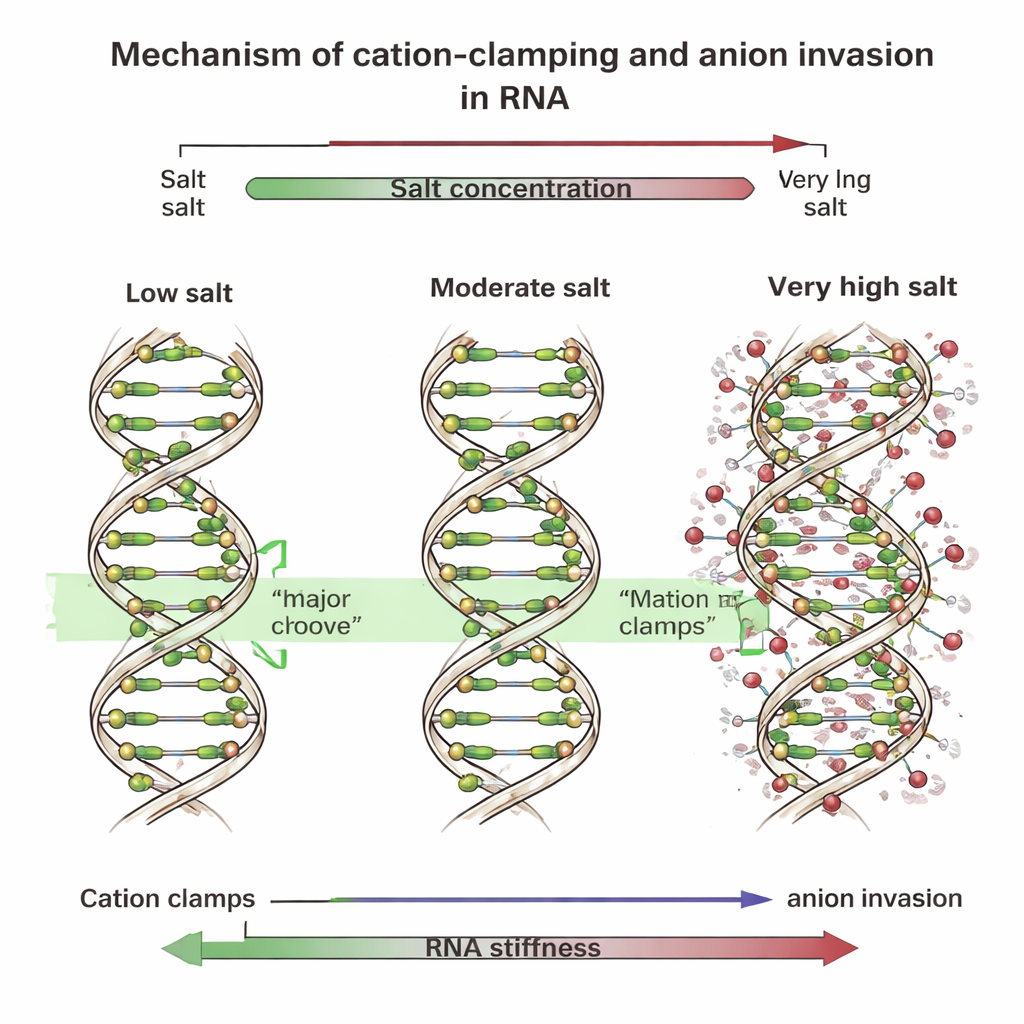
Зажимы, борозды и вторгающиеся ионы
Чтобы выяснить причину, команда провела подробные компьютерные симуляции, отслеживающие каждый атом коротких фрагментов ДНК и РНК в солёной воде. Эти симуляции показали, что при низких и умеренных концентрациях мультивалентные положительные ионы оседают в широкой поверхности РНК, называемой большой бороздой. Там они образуют «катионные зажимы», которые перепрыгивают через борозду, притягивая её стороны, выпрямляя спираль и делая её жёстче. ДНК, у которой борозды имеют другую форму, в основном связывает эти ионы вдоль внешнего остова. Однако при очень высоких уровнях соли многие отрицательные ионы — например, хлорид — проникают близко к остову РНК и даже в большую борозду. Их присутствие нарушает упорядоченные зажимы, превращая их в неправильные, пятнистые «локальные зажимы», которые искажают спираль. Когда исследователи имитировали этот эффект, добавляя искусственные пружины или фиксируя дополнительные отрицательные ионы рядом с РНК в симуляциях, остов РНК сильнее сгибался и её общая жёсткость резко падала, как и наблюдалось в экспериментах.
Что это значит для будущих РНК‑технологий
Если упростить, исследование показывает, что РНК можно сделать либо более прямой и жёсткой, либо более изломанной и гибкой просто изменением типа и концентрации окружающих солей. При умеренных уровнях мультивалентных ионов положительные заряды аккуратно «запирают» внешнюю поверхность РНК и её подпиирают; при экстремальных уровнях вторгающиеся отрицательные ионы разрушают эту равномерную опору и создают искривлённые, более мягкие участки. ДНК не демонстрирует такого резкого размягчения, потому что связывает ионы иначе и в итоге претерпевает инверсию заряда. Эти выводы подчёркивают, что важны не только положительные ионы, но и их отрицательные партнёры для контроля формы РНК. Это знание поможет исследователям целенаправленно настраивать механику РНК в лаборатории — например, для стабилизации РНК‑лекарств, контроля сворачивания РНК в биосенсорах или проектирования более надёжных наноструктур на основе РНК.
Цитирование: Zhang, C., Dong, HL., Zhang, JH. et al. Local cation-clamping distorts and softens RNA duplex. Commun Biol 9, 308 (2026). https://doi.org/10.1038/s42003-026-09580-4
Ключевые слова: механика РНК, мультивалентные ионы, фиксация катионов, ДНК против РНК, эффекты соли