Clear Sky Science · ru
CISH — ключевая внутриклеточная «тормозная» молекула: сравнение и сочетание с существующими и новыми иммунными контрольными точками при раке
Освобождение «тормозов» у клеток, борющихся с раком
Иммунотерапии рака изменили прогноз для многих пациентов, но значительная часть людей по‑прежнему получает мало пользы или совсем не реагирует на лечение. В этом исследовании изучается новый подход к усилению собственных T‑клеток организма — «киллеров» иммунной системы — посредством отключения внутреннего «тормоза» под названием CISH. В отличие от текущих препаратов, действующих на молекулярные переключатели на поверхности клетки, эта стратегия нацелена на систему регулирования внутри клетки, с целью сделать генетически модифицированные T‑клетки значительно лучше в поиске и уничтожении опухолей, даже когда те пытаются скрыться.
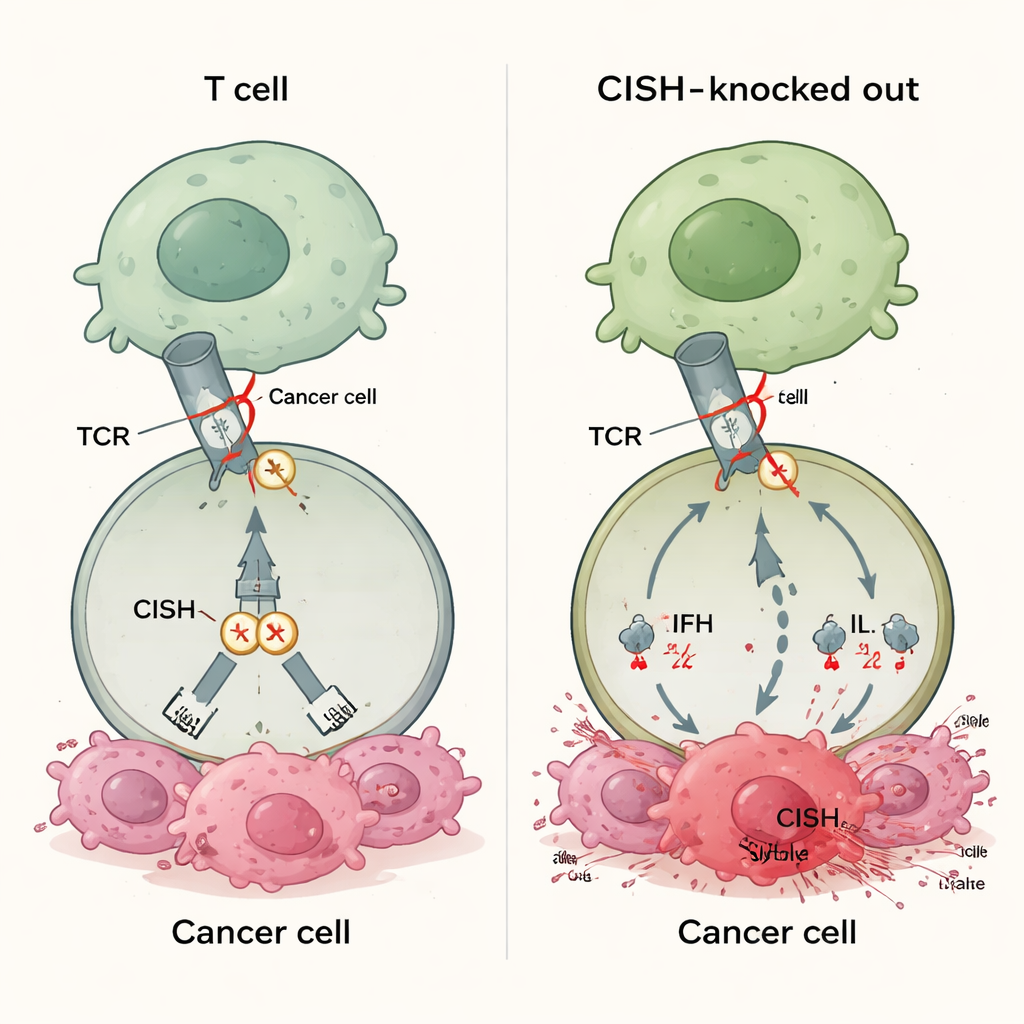
Новый тип иммунного «тормоза»
Большинство одобренных препаратов иммунотерапии блокируют белки, такие как PD‑1, на поверхности T‑клеток. Эти лекарства работают только когда опухоли экспрессируют соответствующие молекулы‑лиганд, например PD‑L1, а многие раки либо никогда не вырабатывают их в достаточном количестве, либо теряют их со временем. Это помогает объяснить, почему 30–60% пациентов не отвечают на современные терапии, нацеленные на контрольные точки. CISH принадлежит к другой категории «тормозов», располагающихся внутри T‑клетки. Он включается при активации Т‑клеточного рецептора и затем ослабляет сигнал, способствуя разрушению ключевого сигнального белка. Поскольку это действие не зависит от лигандов, экспрессируемых опухолью, выключение CISH, по идее, могло бы усилить ответ T‑клеток при многих типах рака, независимо от статуса PD‑L1 или других биомаркеров.
Лоб в лоб с существующими контрольными точками
Исследователи применили редактирование генома CRISPR для удаления CISH и сравнили полученные T‑клетки с клетками, лишёнными PD‑1 или нескольких других внутриклеточных «тормозов». При слабой стимуляции — моделирующей опухоли с низкой плотностью антигена — клетки с удалённым CISH вырабатывали гораздо больше ключевых иммунных медиаторов, включая интерферон‑гамма, TNF‑альфа и IL‑2. Эти клетки также были более «полифункциональными», то есть отдельные T‑клетки могли выполнять несколько функций одновременно, что является признаком высокой противоопухолевой активности. Напротив, простое удаление PD‑1 не помогало в условиях низкого уровня сигнала. В ряде тестов потеря CISH сильнее усиливала активацию, способность к уничтожению и формирование долговременных «памятных» T‑клеток по сравнению с выбитием других внутренних кандидатов, таких как RASA2, CBLB, SOCS1, REGNASE1, HPK1 или PTPN1/2.
Сотрудничество с другими внутриклеточными переключателями
Поскольку сигнальная сеть T‑клеток контролируется множеством пересекающихся путей, команда проверила, не даст ли комбинирование удаления CISH с удалением других «тормозов» суммарного эффекта. С помощью мультиплексного редактирования CRISPR они обнаружили, что удаление CISH совместно с SOCS1, HPK1 или RASA2 дополнительно повышало выработку полезных цитокинов при слабой стимуляции. В опухолевой модели, основанной на распространённой мутации KRAS, T‑клетки, сконструированные с рецептором, специфичным к KRAS, лучше уничтожали раковые клетки при удалении CISH, и этот эффект усиливался при сочетании с удалением SOCS1 или RASA2. Эти результаты свидетельствуют о том, что CISH контролирует нереплицируемый узел в биологии T‑клеток и может взаимодействовать с избранными партнёрами для повышения специфического противоопухолевого эффекта.
Укрепление CAR‑T клеток против хитрых опухолей
Авторы затем обратились к клинически важной модели: CAR‑T клеткам, нацеленным на маркер B‑клеток CD19. Они создали лейкозные клетки с различным уровнем экспрессии CD19, чтобы имитировать опухоли, теряющие или уменьшающие свои цели, чтобы уйти от терапии. CAR‑T клетки без CISH значительно эффективнее уничтожали раковые клетки, даже при низком уровне CD19, и секретировали больше сигналов активации и привлечения. Одновременно они выделяли меньше веществ, известных ослабляющими T‑клетки или способствующих росту опухоли, таких как галектин‑1, галектин‑3, растворимая 4‑1BB, IL‑1α и гликопротеин EMMPRIN/CD147. В совокупности эти изменения указывают на более агрессивные, менее поддающиеся подавлению CAR‑T клетки, особенно пригодные для враждебной среды опухолей с низким уровнем антигена.
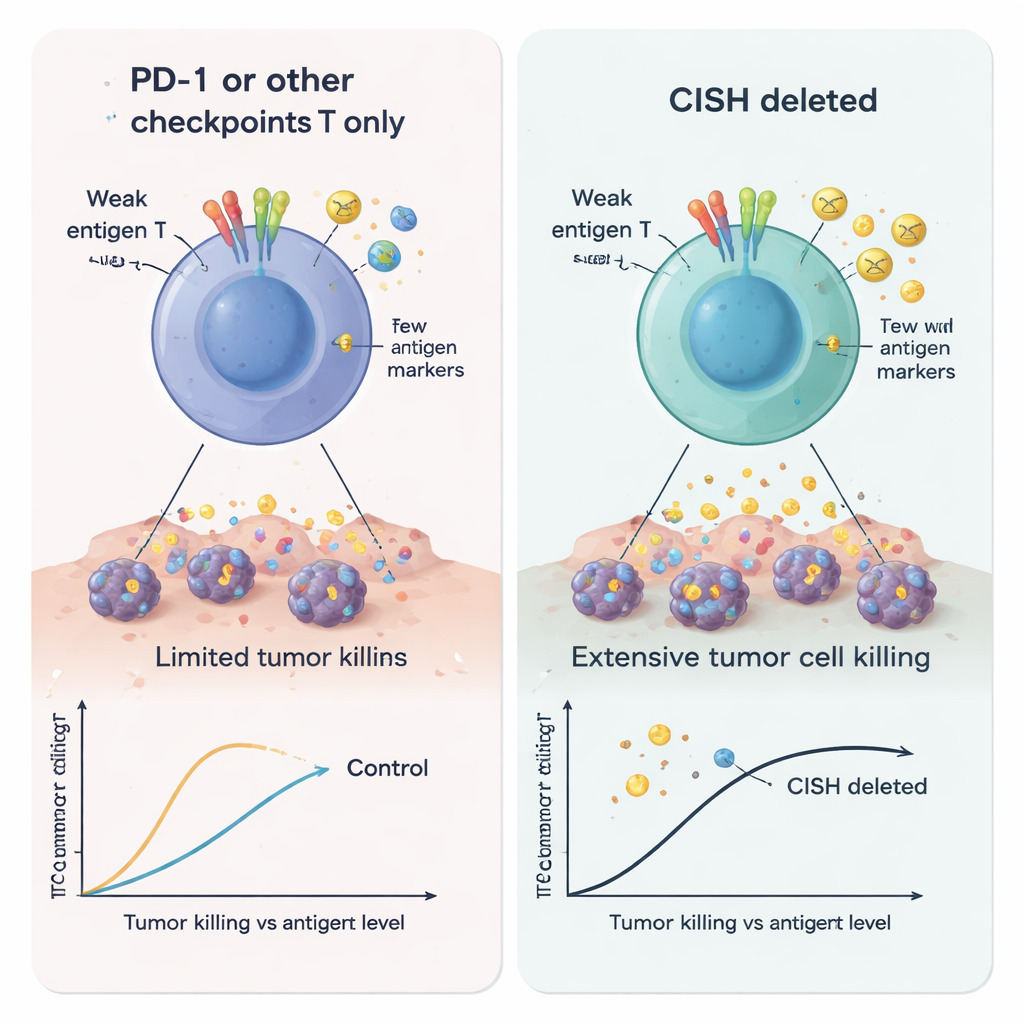
От лаборатории к пациентам
За пределами пробирок и культур идея нацеливания на CISH уже дошла до пациентов. Первое в мире клиническое исследование с использованием лимфоцитов, инфильтрирующих опухоль, отредактированных для удаления CISH у пациента с прогрессирующим колоректальным раком, привело к полному ответу, сохраняющемуся более двух лет, несмотря на устойчивость опухоли к множеству предыдущих лечений. Показав, что CISH является мощной, «наступательной» внутриклеточной контрольной точкой, повышающей чувствительность T‑клеток даже к слабым опухолевым сигналам, это исследование помогает объяснить этот впечатляющий клинический результат и поддерживает усилия по разработке будущих терапий — будь то генетически отредактированные клетки или пероральные препараты — которые безопасно ослабят этот внутренний «тормоз» и расширят возможности иммунотерапии рака.
Цитирование: Cano, F., Bravo-Blas, A., Colombe, M. et al. CISH, a key intracellular checkpoint, in comparison and combination to existing and emerging cancer immune checkpoints. Commun Biol 9, 319 (2026). https://doi.org/10.1038/s42003-026-09579-x
Ключевые слова: иммунотерапия рака, T-клетки, CAR‑T терапия, иммунные контрольные точки, редактирование генов CRISPR