Clear Sky Science · ru
Патогенная мутация в α‑SNAP нарушает связывание с липидами мембраны, скрывая критически важную гидрофобную петлю
Как крошечное изменение белка может нарушить развитие мозга
Клетки нашего мозга постоянно транспортируют грузы в крошечных пузырьках — везикулах, и вспомогательный белок alpha‑SNAP имеет ключевую роль в обеспечении этих доставок. Редкая мутация в alpha‑SNAP, известная по мышиной линии «hyh», вызывает серьёзные нарушения формирования мозга и баланса жидкости. В этом исследовании ставится на первый взгляд простая, но очень важная задача: мешает ли однобуквенная замена в alpha‑SNAP его прикреплению к клеточным мембранам, и может ли это быть ключевой причиной нарушений в развитии мозга?
Клеточный грузчик с множеством обязанностей
В норме alpha‑SNAP действует как своего рода грузчик на пристани для везикул, помогая им сливаться с клеточными мембранами, чтобы груз можно было высвободить или переработать. Он взаимодействует с набором белков SNARE и энергоёмким ферментом NSF, чтобы сблизить мембраны, а затем восстановить систему для следующего цикла. Помимо этой классической роли, alpha‑SNAP участвует в управлении такими процессами, как аутофагия (самоочищение клетки), программируемая гибель клеток, кальциевый вход и сенсоры энергии. Все эти функции в той или иной мере зависят от способности alpha‑SNAP касаться и частично внедряться в жирную поверхность мембран.
Скрытая петля и проблемная мутация
Ранее было показано, что alpha‑SNAP использует короткую «жирную» петлю рядом с одним концом белка, чтобы зацепляться за мембраны. В здоровом белке эта петля выступает наружу и может погружаться во внешний слой мембраны. У мышей hyh один строительный блок в позиции 105 заменён, что создаёт мутацию M105I. Авторы применили компьютерное моделирование, чтобы увидеть, как это изменение влияет на конформацию белка. Они обнаружили, что мутант становится слегка компактнее и скручивается так, что гидрофобная петля прячется внутрь, в сторону от воды и от мембран. В результате мутантный белок подходит к мембранам под более плоским углом и контактирует с ними менее липкой частью, что сокращает и время контакта, и глубину внедрения. Расчёты энергии связывания подтверждали это: дикого типа белок устанавливался в низкоэнергетическое, прочное связанное состояние, тогда как мутант предпочитал более слабые, поверхностные контакты.
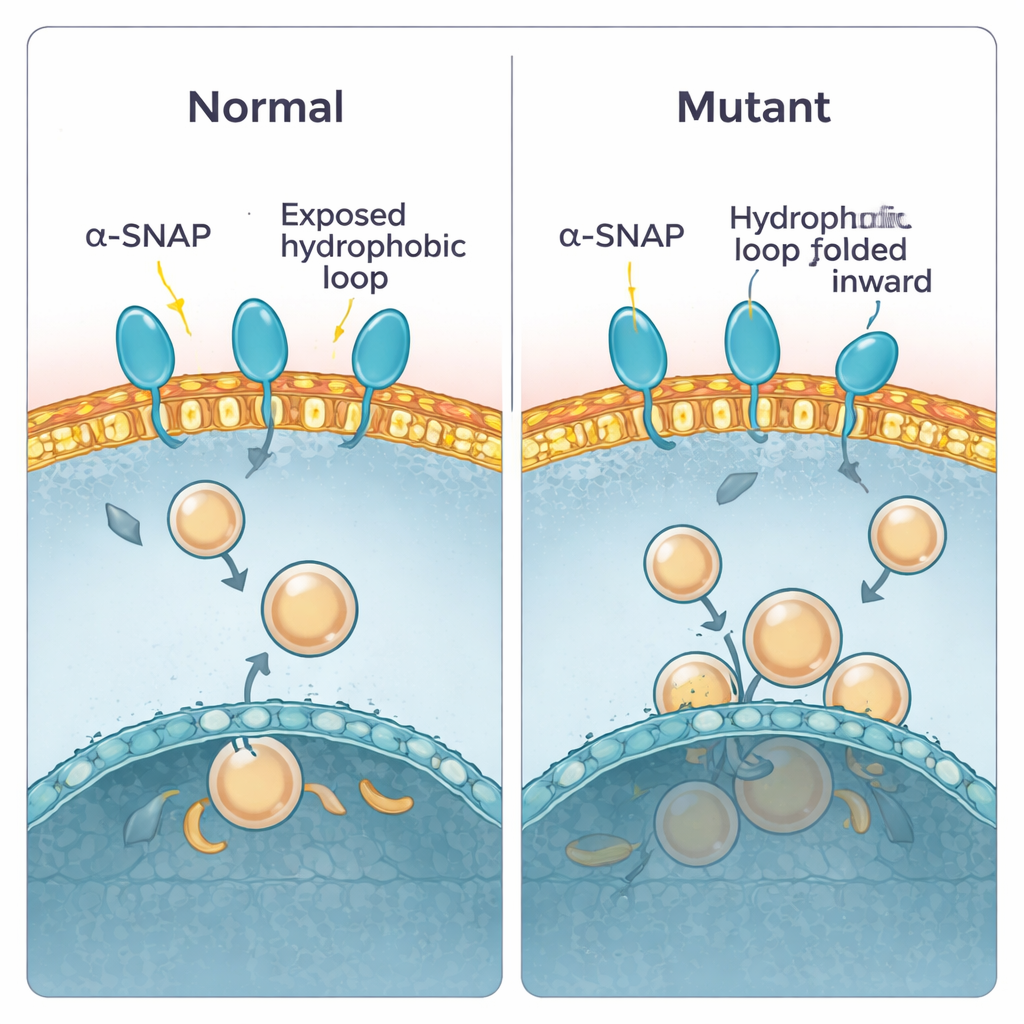
Проверка предсказания в лаборатории
Чтобы проверить эти предположения, команда очистила как нормальный, так и мутантный alpha‑SNAP и протестировала их поведение в разных экспериментальных системах. Сначала они использовали детергент, разделяющийся на водную и жировую фазы, имитируя выбор между водой и мембраной. Нормальный alpha‑SNAP равномерно распределялся, что соответствует сбалансированной, частично липидной поверхности. Мутантная версия была менее склонна переходить в жировую фазу, что указывает на то, что её жирные участки действительно более скрыты. Затем белки взаимодействовали с плоскими «листами» плазматической мембраны, полученными из клеток, и исследователи визуализировали количество мест связывания. И снова: нормальный alpha‑SNAP образовывал точки на мембране, тогда как мутант связывался значительно меньше. Наконец, они пропускали через сахарные градиенты искусственные мембранные пузырьки (липосомы), сделанные из липидов мозга. Дикий тип alpha‑SNAP поднимался вместе с везикулами, богатыми липидами плазматической мембраны, тогда как мутант отставал, слабо связываясь, если только пузыри не были составлены из иного, более внутреннего мембранного набора.
Последствия в развивающемся мозге
Дальше исследователи обратились к мозгам развивающихся эмбрионов мышей, сосредоточившись на стадии, когда рождаются новые нейроны. Разделяя содержимое клеток на растворимые и мембранно‑связанные фракции, они показали, что общий уровень alpha‑SNAP уже снижен в мозгах hyh, но важнее другое: доля белка, прикреплённого к мембранам, была непропорционально низкой по сравнению с нормой. При дальнейшем разделении разных типов мембран они обнаружили, что наибольшая потеря приходится на плазматическую мембрану — внешнюю поверхность клетки, тогда как внутренние мембраны затронуты гораздо меньше. Микроскопия подтвердила эти наблюдения: в нормальной ткани alpha‑SNAP очерчивал клетки в виде сотоподобной сетки, совпадающей с известным поверхностным маркером. В мозгах hyh эта чёткая краевая окраска растворялась в более рассеянном внутреннем свечении, что указывает на то, что мутантный белок не удерживается на краю клетки, где особенно активны слияние везикул и сигнальная передача.
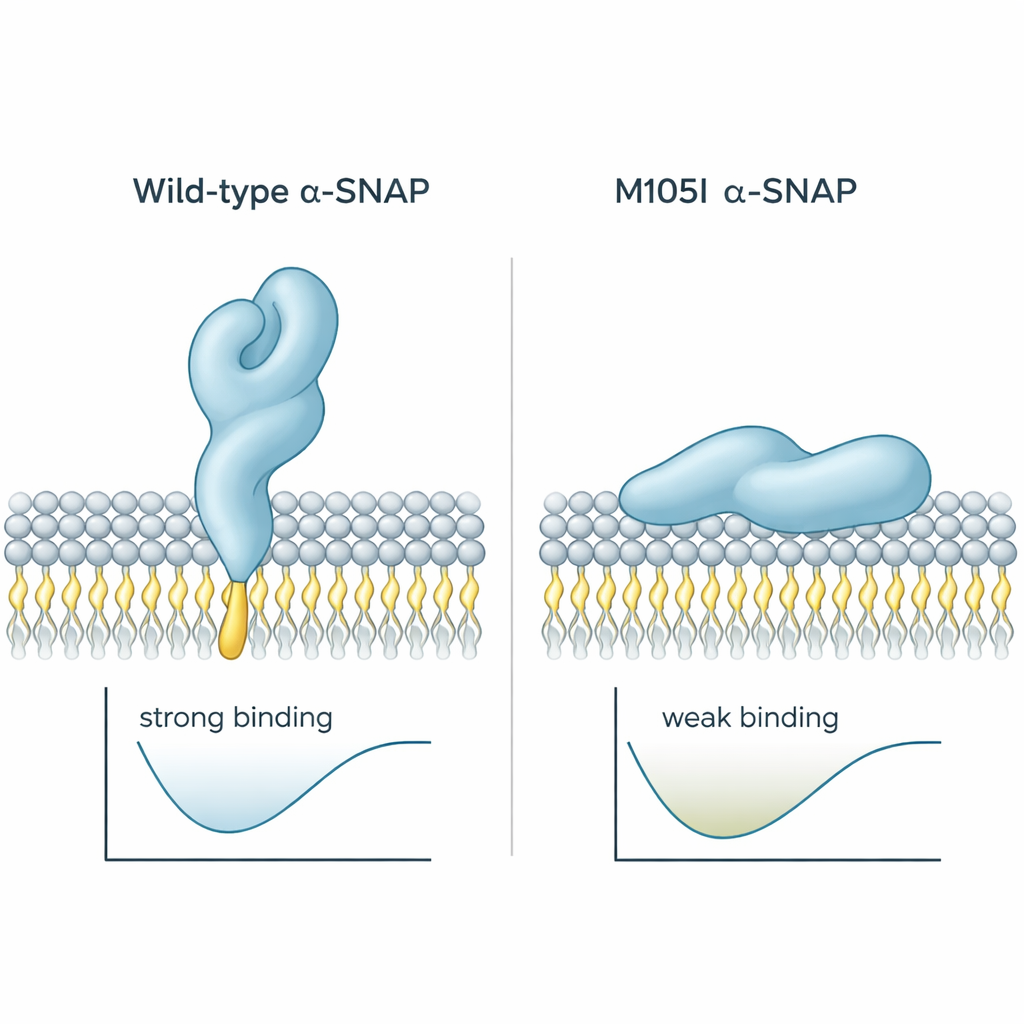
Почему это важно для болезни
В целом работа показывает, что мутация M105I делает не только уменьшение количества alpha‑SNAP; она изменяет свёртывание белка так, что его ключевая петля для захвата мембраны оказывается скрытой. Это затрудняет способность alpha‑SNAP зацепиться за плазматическую мембрану и принять правильную ориентацию для организации механизмов слияния. В развивающемся мозге, где точная доставка сигналов и строительных материалов к поверхности клетки имеет критическое значение, этот тонкий структурный дефект, вероятно, способствует развитию гидроцефалии, нарушений организации коры и другим дефектам, наблюдаемым у мышей hyh. Для неспециалистов посыл ясен: даже крошечное изменение формы одного белка способно изменить то, как клетки общаются, и, как следствие, то, как формируется мозг.
Цитирование: Méndez-Ruette, M., Bedoya, M., Hinrichsen, B. et al. A pathogenic mutation in α-SNAP impairs membrane lipid binding by concealing a critical hydrophobic loop. Commun Biol 9, 294 (2026). https://doi.org/10.1038/s42003-026-09578-y
Ключевые слова: alpha-SNAP, связывание с мембраной, мутация белка, развитие мозга, слияние везикул