Clear Sky Science · ru
Разработка лигандов prohibitin на основе капсаицина для модуляции взаимодействия Aurora kinase A/PHB2 и митофагии в раковых клетках
Почему химическое вещество из чили важно для рака
Жгучесть чили обусловлена капсаицином — небольшой молекулой, которая связывается с белками в наших клетках. В этом исследовании изучается неожиданный аспект знакомой приправы: учёные переработали капсаицин, создав новые близкие к лекарствам молекулы, которые нацеливаются на «энергетические станции» раковых клеток — митохондрии — и смягчают процесс, с помощью которого эти клетки поддерживают свои энергетические фабрики в рабочем состоянии. Поскольку раковые клетки сильно зависят от эффективных митохондрий для подпитки стремительного роста, способность выборочно нарушать эту систему поддержки может открыть новый путь для противораковой терапии.
Энергетические станции клетки и их внутренняя служба уборки
Митохондрии постоянно балансируют между созданием новых единиц и переработкой повреждённых. Сторона переработки, называемая митофагией, действует как система контроля качества: изношенные митохондрии помечаются и разрушаются, тогда как более здоровые остаются. Многие раковые клетки захватывают этот баланс, используя митофагию для удаления слабых митохондрий и обогащения «суперисполнителями», которые вырабатывают большое количество АТФ — энергетической валюты клетки. Белок Aurora kinase A (AURKA), часто чрезмерно экспрессируемый в опухолях, недавно был обнаружен внутри митохондрий, где он взаимодействует с другим белком, Prohibitin‑2 (PHB2), и адаптером аутофагии LC3. Вместе они формируют комплекс, который способствует митофагии и поддерживает высокий уровень энергетического выхода в раковых клетках.
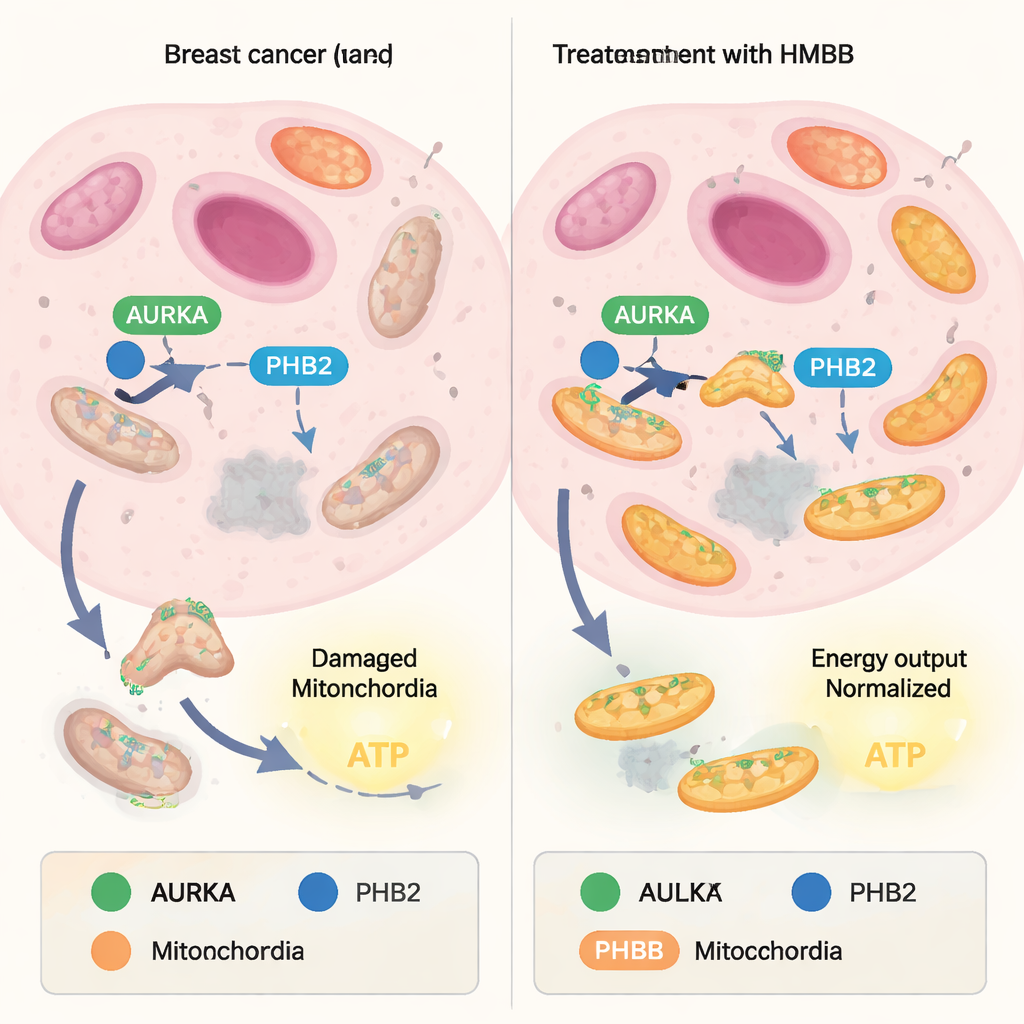
От жгучего капсаицина к специально настроенным молекулярным инструментам
Предыдущие работы показали, что природное соединение ксантохумол может связываться с PHB2 и разрывать комплекс AURKA–PHB2–LC3, блокируя митофагию и снижая производство митохондриального АТФ. Однако структура ксантохумола не идеальна для разработки лекарств. В этом исследовании авторы обратились к капсаицину, ещё одному природному лиганду PHB, и изучили, можно ли переработать его в более практичные инструменты. Сначала они подтвердили, что капсаицин немного ослабляет взаимодействие между AURKA и PHB2 в живых клетках молочной железы, используя метод визуализации (FRET/FLIM), который измеряет близость двух меченых белков. Затем они синтезировали 16 молекул, вдохновлённых капсаицином, модифицируя «хвост» и ароматическую «головку» исходной структуры, и систематически проверяли, как каждая версия влияет на партнёрство AURKA–PHB2 внутри митохондрий.
Открытие молекулярного «клея», который скрепляет белки
Модифицированные молекулы оказали поразительно разные эффекты. Некоторые, как сам капсаицин или производное, названное соединением 5, способствовали более лёгкому разъединению AURKA и PHB2. Другие почти не проявляли действия. Однако подмножество, особенно молекула, названная соединением 13, впоследствии получившая имя HMBB, действовало противоположно и значительно усиливало связь между AURKA и PHB2. Компьютерные докинг‑симуляции помогли объяснить такое поведение. Капсаицин и соединение 5, как правило, застревали в активном центре AURKA так, что создавали физические конфликты с PHB2, подталкивая два белка в разные стороны. Напротив, соединения 12 и 13 размещались в активном центре AURKA и одновременно контактировали с известным ингибирующим карманом на PHB2, не вызывая столкновения. Их формы позволяли им выступать в роли «молекулярного клея», связывающего AURKA и PHB2 и стабилизирующего комплекс.
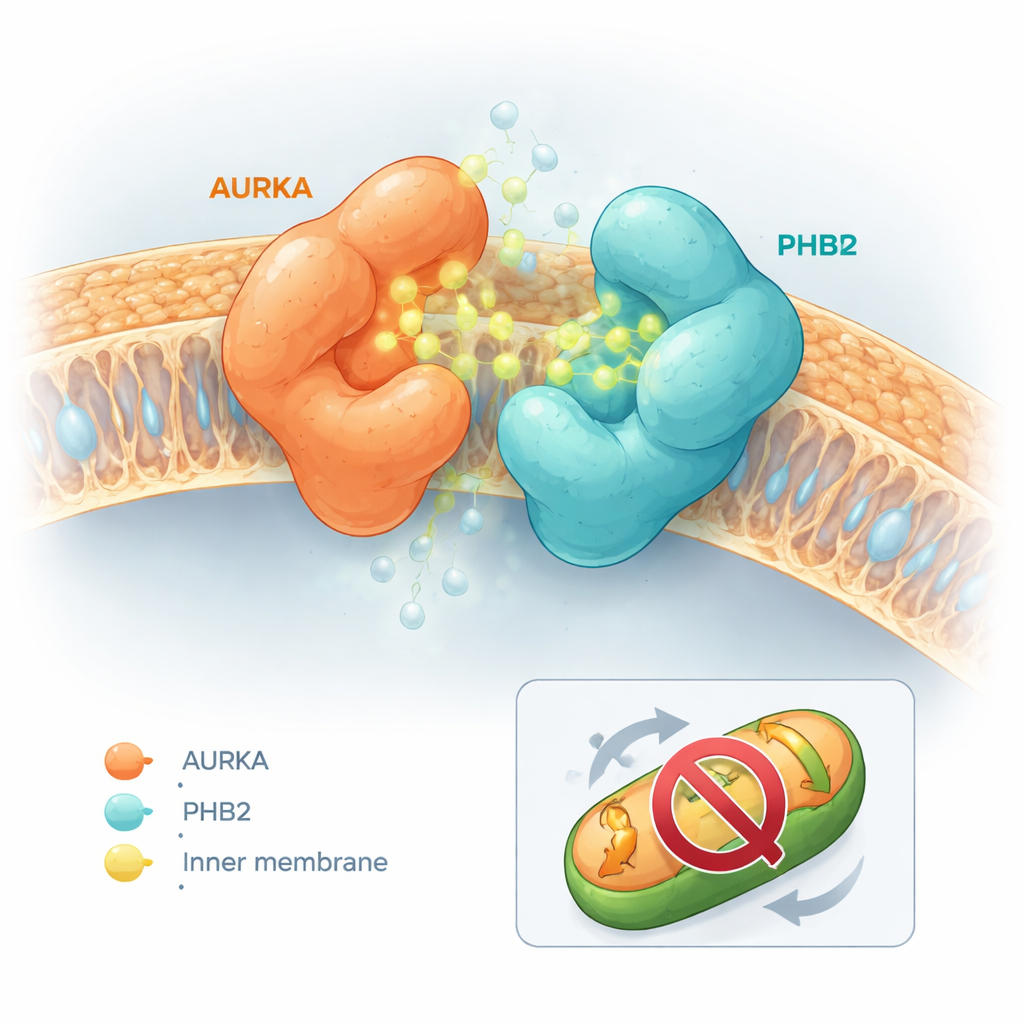
Блокирование митохондриальной уборки без отключения контрольного центра клетки
Критическим вопросом было то, отключает ли такое поведение «молекулярного клея» AURKA повсеместно в клетке, что могло бы привести к широким побочным эффектам, или действует более селективно. Используя отдельный флуоресцентный биосенсор, который сообщает об активации AURKA в центросомах — структурах, организующих аппаратуру деления клетки — команда наблюдала, что HMBB не снижал активность AURKA в этих участках. Тем не менее в митохондриальных тестах HMBB обращал вспять потерю митохондриальной массы, обычно вызванную сверхэкспрессией AURKA в клетках молочной железы. В клетках, которые естественно производят высокий уровень AURKA, HMBB увеличивал содержание митохондрий, указывая на то, что индуцированная AURKA митофагия была заблокирована. В клетках с низким уровнем AURKA HMBB оказывал минимальное влияние, подчёркивая его зависимость от пути AURKA–PHB2.
Что это может значить для будущих противораковых терапий
В совокупности результаты показывают, что тщательно разработанные производные капсаицина могут тонко настраивать взаимодействие AURKA и PHB2 в митохондриях. Выступая в роли молекулярного клея, HMBB и родственные соединения фиксируют AURKA и PHB2 в конфигурации, которая препятствует обычной программе митофагии, не блокируя при этом важные функции AURKA в других участках клетки. Для неспециалиста ключевая идея в том, что авторы создали прототипы молекул, которые селективно вмешиваются в то, как раковые клетки поддерживают свои «энергетические станции», потенциально ослабляя их энергетическое снабжение при одновременном сохранении нормальных функций клеток. Хотя эти соединения всё ещё находятся на ранней лабораторной стадии, они иллюстрируют перспективную стратегию: использование небольших, похожих на лекарства молекул для нацеливания на специфические белковые партнёрства внутри митохондрий и, таким образом, подрыва метаболических преимуществ, от которых зависят многие опухоли.
Цитирование: Djehal, A., Caron, C., Giordano, D. et al. Development of capsaicin-derived prohibitin ligands to modulate the Aurora kinase A/PHB2 interaction and mitophagy in cancer cells. Commun Biol 9, 320 (2026). https://doi.org/10.1038/s42003-026-09573-3
Ключевые слова: митохондрии, митофагия, Aurora kinase A, производные капсаицина, метаболизм рака