Clear Sky Science · ru
Функциональная перестройка iNKT-клеток реактивными к сульфатидам NKT-клетками типа II перепрограммирует альвеолярные макрофаги и ослабляет ишемическо‑реперфузионное повреждение легких
Почему важно защищать донорские легкие
Когда хирурги пересаживают легкое или восстанавливают кровоток после закупорки сосуда, внезапное возвращение кислорода может парадоксально повредить ткань. Эта проблема, называемая ишемически‑реперфузионным повреждением легких, является одной из основных причин ранней неудачи после трансплантации легкого и других критических вмешательств. В приведенном здесь исследовании рассматривается, как редкий тип иммунных клеток можно «перепрограммировать» для подавления воспаления, что может стать новым способом защиты уязвимых легких в моменты наибольшей потребности.
Иммунные клетки, которые могут лечить или вредить
Наши легкие патрулируют альвеолярные макрофаги — иммунные клетки, находящиеся в альвеолах и быстро реагирующие на угрозу. Эти клетки могут переключаться между двумя основными режимами. В «боевом» режиме (часто называемом M1) они выделяют провоспалительные вещества, которые помогают уничтожать микробы, но также могут повреждать ткань. В «восстановительном» режиме (часто называемом M2) они выделяют успокаивающие молекулы, ограничивающие воспаление и способствующие заживлению. При ишемии‑реперфузии легких баланс смещается в сторону повреждающего боевого режима. Исследователи предположили, что если мягко сдвинуть макрофаги в сторону режима восстановления в нужный момент, это может смягчить вред от такого повреждения.
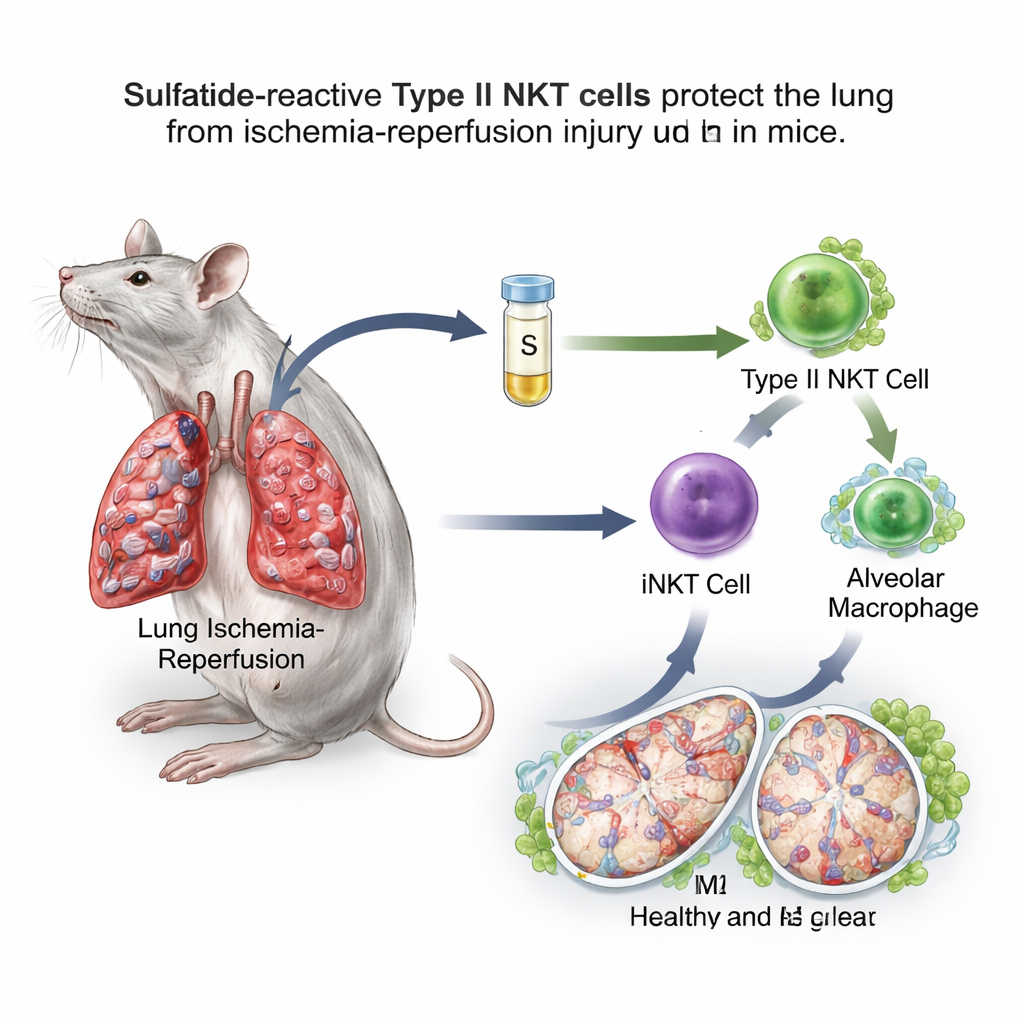
Сахаро‑жировая молекула переключает иммунный тумблер
Команда сосредоточилась на натуральных киллер‑T (NKT) клетках — необычных иммунных клетках, которые стоят на стыке быстрого врожденного ответа и более медленного направленного адаптивного ответа. NKT‑клетки делятся на два основных типа. Тип I, также называемый инвариантными NKT (iNKT) клетками, в экспериментах на мышах известен тем, что усугубляет ишемию‑реперфузию легких. Однако NKT‑клетки типа II способны сдерживать иммунные реакции в других органах. Жировая молекула сульфатид распознается именно клетками типа II. В модели на мышах, где кровоток к одному легкому перегораживали на час, а затем восстанавливали, исследователи вводили сульфатид за несколько часов до инсульта. Они обнаружили, что у мышей, получавших сульфатид, было меньше отека легких, меньше проницаемости сосудов, ниже оксидативный стресс, лучше насыщение кислородом и сниженное количество провоспалительных веществ в промывных жидкостях легкого по сравнению с неполучавшими препарат животными.
Перепрограммирование макрофагов через каскад сигналов
При более тщательном рассмотрении выяснилось, что сульфатид сдвигал альвеолярные макрофаги в сторону восстановительного M2‑состояния. Эти макрофаги проявляли больше поверхностных маркеров и экспрессии генов, связанных с исцелением, и лучше подавляли воспаление при пересадке в других мышей. Когда ученые выборочно удаляли альвеолярные макрофаги, повреждение легких усугублялось, а защитный эффект сульфатиду в значительной степени утратился, что показывает, что эти клетки являются ключевым узлом в пути. Важно, что польза сульфатида исчезала у мышей, лишенных либо NKT‑клеток типа II, либо iNKT‑клеток типа I, и восстановиться она могла при переносе обратно iNKT‑клеток, предварительно обработанных сульфатидом. В совокупности эти эксперименты выявили ретрансляцию: сульфатид активирует NKT‑клетки типа II, которые в свою очередь перестраивают поведение iNKT‑клеток, а те перепрограммируют альвеолярные макрофаги.
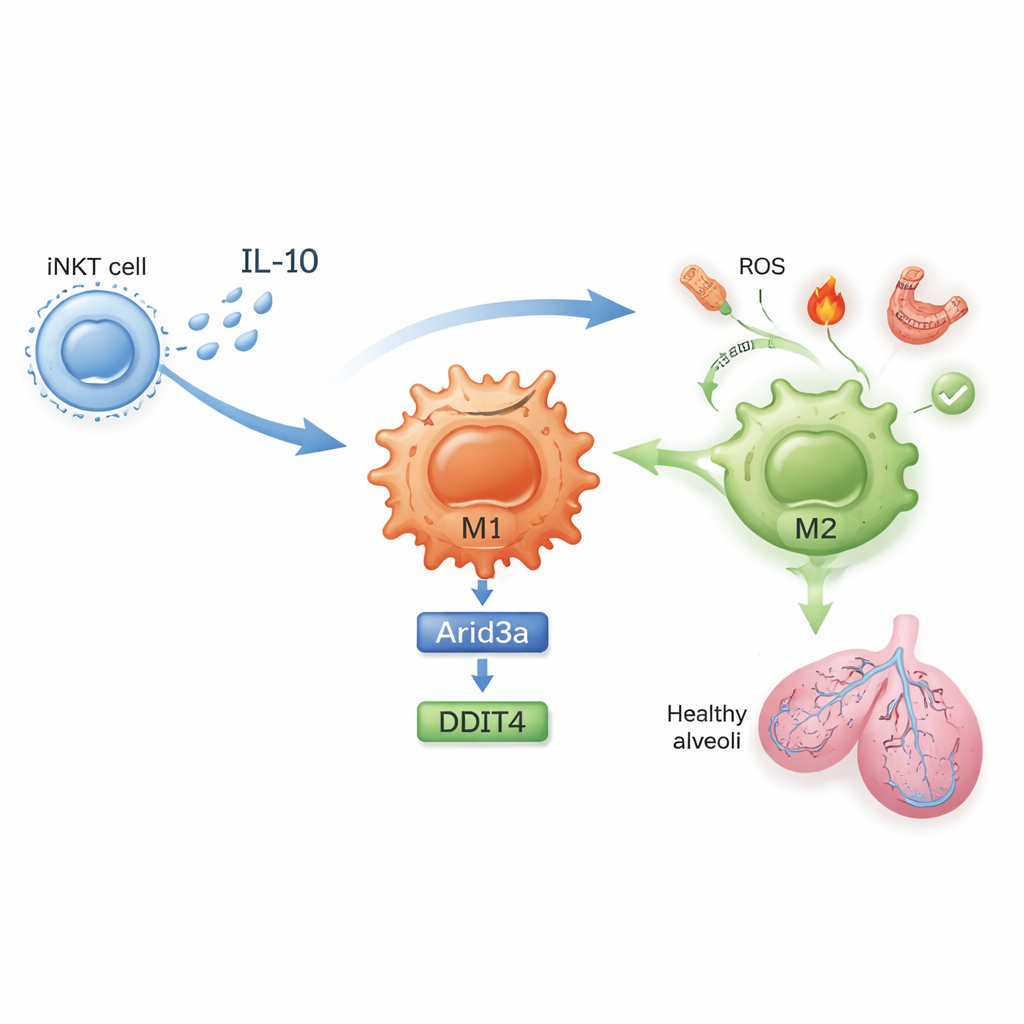
Молекулярная цепочка, успокаивающая воспаление
Что же именно меняется внутри этих клеток? У неполучавших лечение мышей iNKT‑клетки легких пролиферировали во время ишемии‑реперфузии и продуцировали высокие уровни интерферона‑гамма, мощного провоспалительного сигнала. После воздействия сульфатида iNKT‑клетки начали вырабатывать больше интерлейкина‑10 (IL‑10), сильного антивоспалительного медиатора, и меньше интерферона‑гамма. В исследовании показано, что IL‑10 от iNKT‑клеток действует непосредственно на макрофаги, заставляя их переходить к M2‑поляризации. С помощью профилирования экспрессии генов и тщательно спланированных экспериментов in vitro авторы выявили молекулярную цепочку в макрофагах: IL‑10 усиливает фактор транскрипции Arid3a, который, в свою очередь, повышает уровень стресс-индуцируемого гена DDIT4. Ось Arid3a–DDIT4 помогает подавить путь контроля роста, который в противном случае удерживает макрофаги в провоспалительном состоянии, подталкивая их к защитной программе M2.
От легких мышей к будущим терапиям
Чтобы проверить центральность этой молекулярной цепочки, исследователи использовали малые интерферирующие РНК для заглушения Arid3a или DDIT4 в макрофагах перед их переносом в мышей. При подавлении любого из этих генов сульфатид уже не смог полностью направить макрофаги в режим восстановления, и защита легких ослабевала. Дополнительный анализ указывает на то, что сигнальный белок YES1 помогает активированным сульфатидом NKT‑клеткам типа II перенастроить iNKT‑клетки в сторону продукции IL‑10. Хотя эти результаты получены на моделях на мышах и в модифицированных клеточных системах in vitro, они очерчивают понятную картину: кратковременная активация специфического подмножества NKT‑клеток сульфатидом может позволить превратить обычно повреждающие иммунные ответы в защитные, что могло бы помочь защищать пересаженные или травмированные легкие. В будущем препараты, имитирующие этот путь, могут помочь большему числу пациентов пережить и успешно восстановиться после жизненно важных операций на легких.
Цитирование: Li, Q., Yin, J., Lin, Q. et al. Functional remodeling of iNKT cells by sulfatide-reactive type II NKT cells reprograms alveolar macrophages to alleviate lung ischemia-reperfusion injury. Commun Biol 9, 289 (2026). https://doi.org/10.1038/s42003-026-09572-4
Ключевые слова: ишемия‑реперфузия легких, альвеолярные макрофаги, натуральные киллер‑T клетки, интерлейкин‑10, иммунная модуляция