Clear Sky Science · ru
Подпись радиопатома на основе глубокого обучения предсказывает риск рецидива гепатоцеллюлярной карциномы после гепатэктомии
Почему это важно для людей с раком печени
Рак печени входит в число самых смертельных онкологических заболеваний в мире, и даже после удаления видимой опухоли у многих пациентов болезнь возвращается уже через несколько лет. В этом исследовании представлен инструмент искусственного интеллекта, который объединяет медицинские сканы и микроскопические изображения опухолей, чтобы точнее предсказать, у кого с наибольшей вероятностью случится рецидив гепатоцеллюлярной карциномы, самой распространённой формы рака печени. Такие прогнозы могут помочь врачам персонализировать последующее наблюдение и дополнительные лечения, чтобы предотвратить рецидив и продлить жизнь пациентов.
Видеть опухоль целиком: снаружи и изнутри
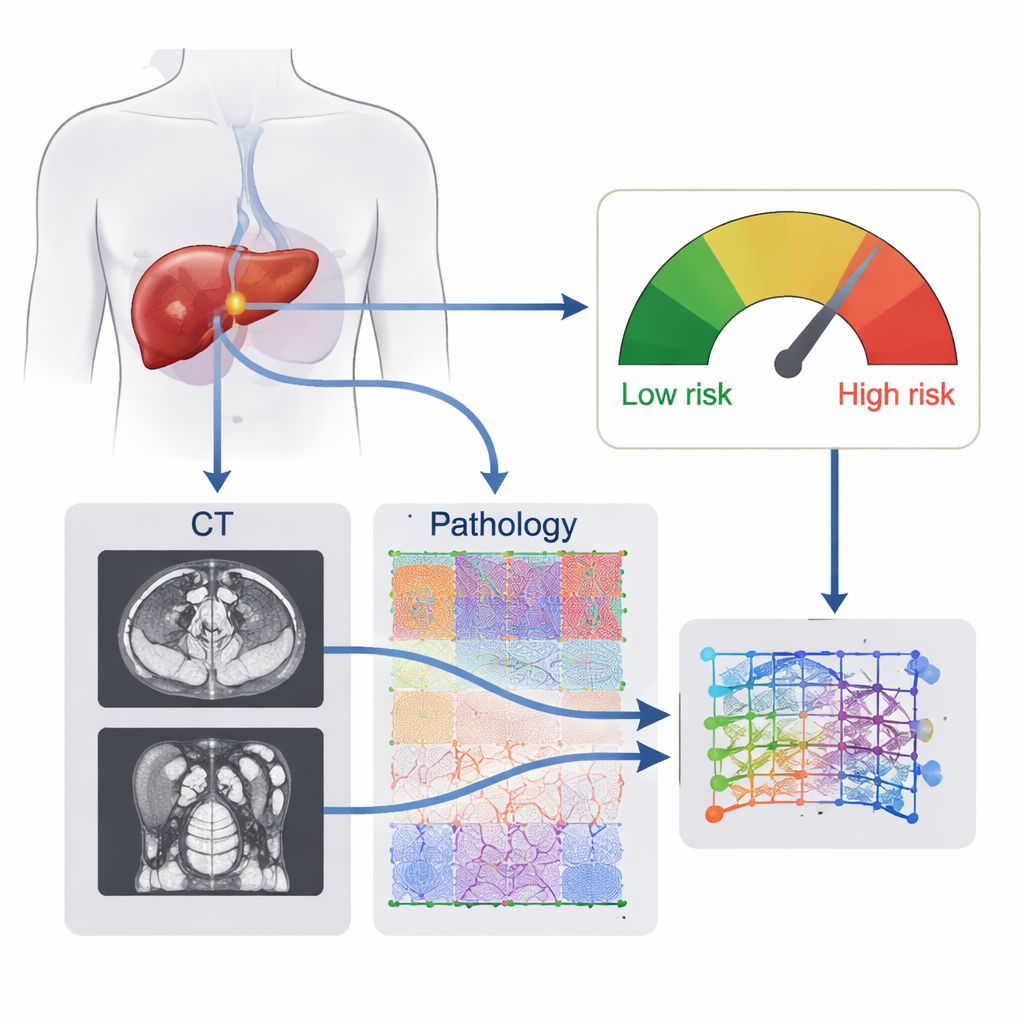
Врачи обычно опираются на КТ-сканы, анализы крови и базовые патологические отчёты, чтобы оценить риск рецидива после операции на печени. Каждый из этих инструментов показывает опухоль под своим углом, но ни один не отражает её сложность полностью. КТ изображение демонстрирует общую форму опухоли, кровоснабжение и соотношение с печенью, тогда как слайды под микроскопом выявляют степень агрессивности клеток и их взаимодействие с окружающей тканью. Исследователи предположили, что компьютерная система, которая «смотрит» на оба уровня — органные сканы и клеточные изображения — может распознать паттерны, недоступные человеку, и, следовательно, более точно предсказать вероятность возвращения рака.
Объединённый цифровой отпечаток опухоли
Команда разработала то, что они называют радиопатомическим признаком на основе глубокого обучения (DLRP) — по сути цифровой отпечаток опухоли каждого пациента, сформированный из двух источников данных. Во-первых, нейронная сеть автоматически выделяла опухоли на предоперационных КТ и изучала тонкие признаки изображения, связанные с рецидивом. Во-вторых, другая сеть анализировала целые слайды тканей, окрашенные гематоксилин-эозином, разбивая их на тысячи маленьких фрагментов и определяя, какие микроскопические паттерны имеют наибольшее значение. Модуль слияния затем объединял признаки КТ и патоморфологии в единый риск‑балл, отражающий поведение опухоли скорее в целом, чем любую отдельную видимую черту.
Тестирование шкалы на реальных пациентах
Исследователи применили эту систему к 599 пациентам, перенесшим операцию по поводу гепатоцеллюлярной карциномы в четырёх больницах, разделив их на тренировочные и независимые тестовые группы. Во всех тестовых наборах радиопатомическая подпись (DLRP) предсказывала безрецидивную выживаемость лучше, чем модели, использующие только КТ, только патологию, стандартные клинические показатели, такие как размер опухоли и маркёры в крови, или широко применяемая стадия по Barcelona Clinic Liver Cancer. Пациенты с высокими значениями DLRP имели значительно большую вероятность возвращения опухоли и более короткую общую выживаемость. Важно, что это наблюдалось во многих подгруппах, включая пациентов с малыми и крупными опухолями, с одиночными и множественными очагами, а также с циррозом и без него, что указывает на то, что шкала отражает ключевые аспекты агрессивности опухоли.
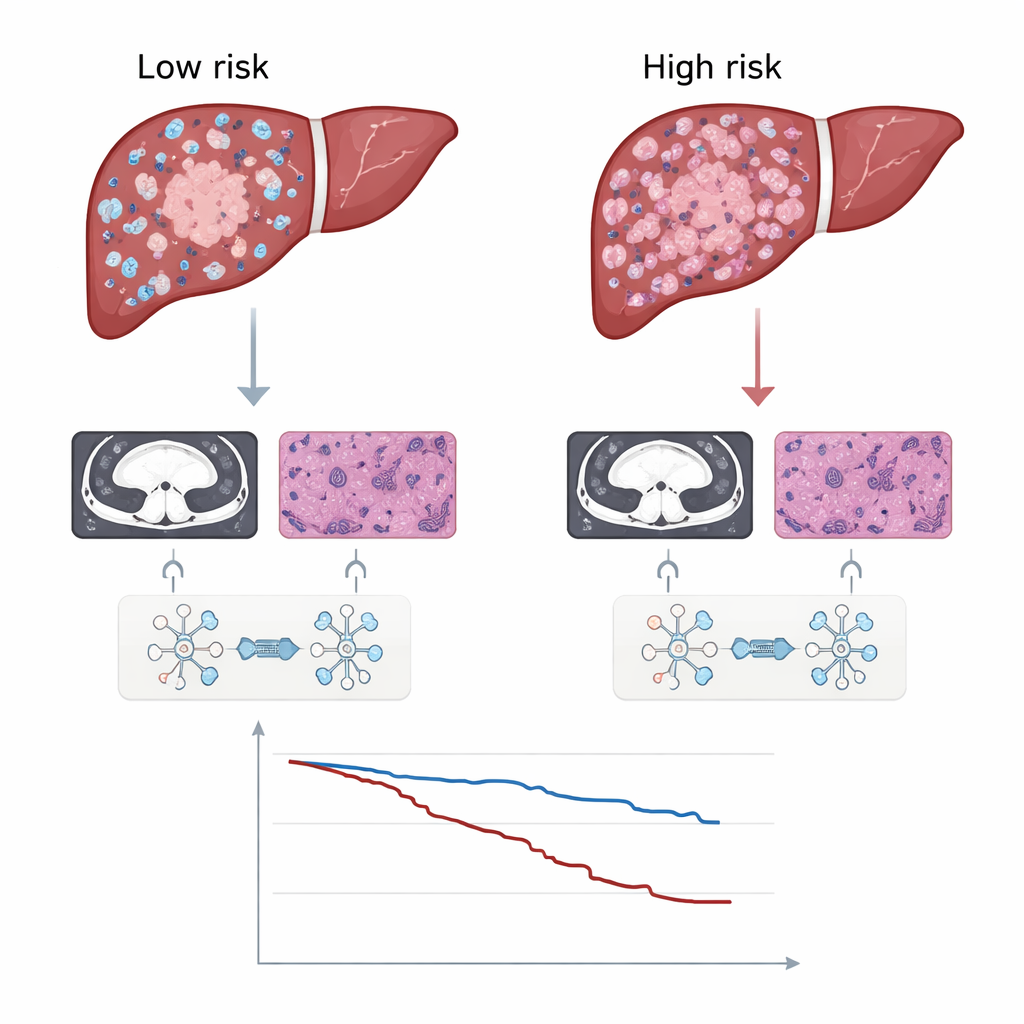
Руководство по дополнительному лечению и подсказки к биологии
Помимо предсказания, шкала помогла выделить пациентов, которые могли бы выиграть от дополнительной процедуры — послеоперационной адъювантной трансартериальной хемоэмболизации (PA‑TACE), при которой в печёночное кровоснабжение вводят химиопрепарат в масляном контрастном веществе. Среди всех пациентов в целом те, кто получал PA‑TACE, в среднем дольше оставались без рецидива. Но при разделении группы по подписи DLRP преимущества сосредоточились почти исключительно в группе высокого риска; у пациентов с низким риском явного преимущества не наблюдалось, что подразумевает возможность безопасного избегания дополнительной нагрузки терапии. Команда также попыталась объяснить, почему высокорисковые опухоли ведут себя хуже, связав DLRP‑оценки с генетическими данными из The Cancer Genome Atlas. Высокие баллы ассоциировались с активацией пути Wnt/β‑катенин, известного своей ролью в стимулировании роста опухоли и устойчивости к иммунотерапии, а также с меньшим проникновением противоопухолевых иммунных клеток, особенно CD8 T‑лимфоцитов, в опухоль.
Что это значит для будущего ухода при раке печени
Для непрофессионала вывод таков: компьютеры теперь могут объединять снимки, похожие на рентген, и микроскопические виды, чтобы выдать одно число, показывающее, с какой вероятностью рак печени вернётся после операции. Исследование демонстрирует, что такое число может превосходить традиционные системы стадирования и помогать решать, кому действительно нужны дополнительные вмешательства и более интенсивное наблюдение. Хотя инструмент ещё требует проспективной валидации в более широких популяциях пациентов, включая тех, у кого заболевание печени не связано с вирусом гепатита B, он указывает на будущее, в котором планы лечения формируются на основе богатых многоуровневых портретов каждой опухоли, а не лишь по размеру и стадии.
Цитирование: Wang, G., Chen, W., Liang, Z. et al. A deep learning radiopathomic signature predicts recurrence risk of hepatocellular carcinoma after hepatectomy. Commun Biol 9, 295 (2026). https://doi.org/10.1038/s42003-026-09571-5
Ключевые слова: гепатоцеллюлярная карцинома, рецидив рака печени, глубокое обучение, медицинская визуализация, микроокружение опухоли