Clear Sky Science · ru
Клеточные и изоформа-специфичные тесты киназ рецепторов, связанных с G-белком, для всесторонней оценки ингибиторов
Почему важно умение «убавлять громкость» в клетке
Многие наши лекарства действуют через повышение или снижение активности рецепторов на поверхности клетки, которые распознают гормоны, нейротрансмиттеры и лекарства. Эти рецепторы нужно аккуратно выключать, чтобы клетка не оставалась переактивированной — этот процесс частично контролируют ферменты, именуемые GRK. Когда GRK становятся чрезмерно активными, как это наблюдается при сердечной недостаточности и некоторых видах рака, сигнальные пути нарушаются. В этом исследовании разработаны практичные клеточные тесты, позволяющие измерять, насколько эффективно экспериментальные молекулы блокируют конкретные изоформы GRK, помогая учёным проектировать более точные лекарства, которые тонко настраивают эти важные «регуляторы громкости» клетки.
Стражи на поверхности клетки
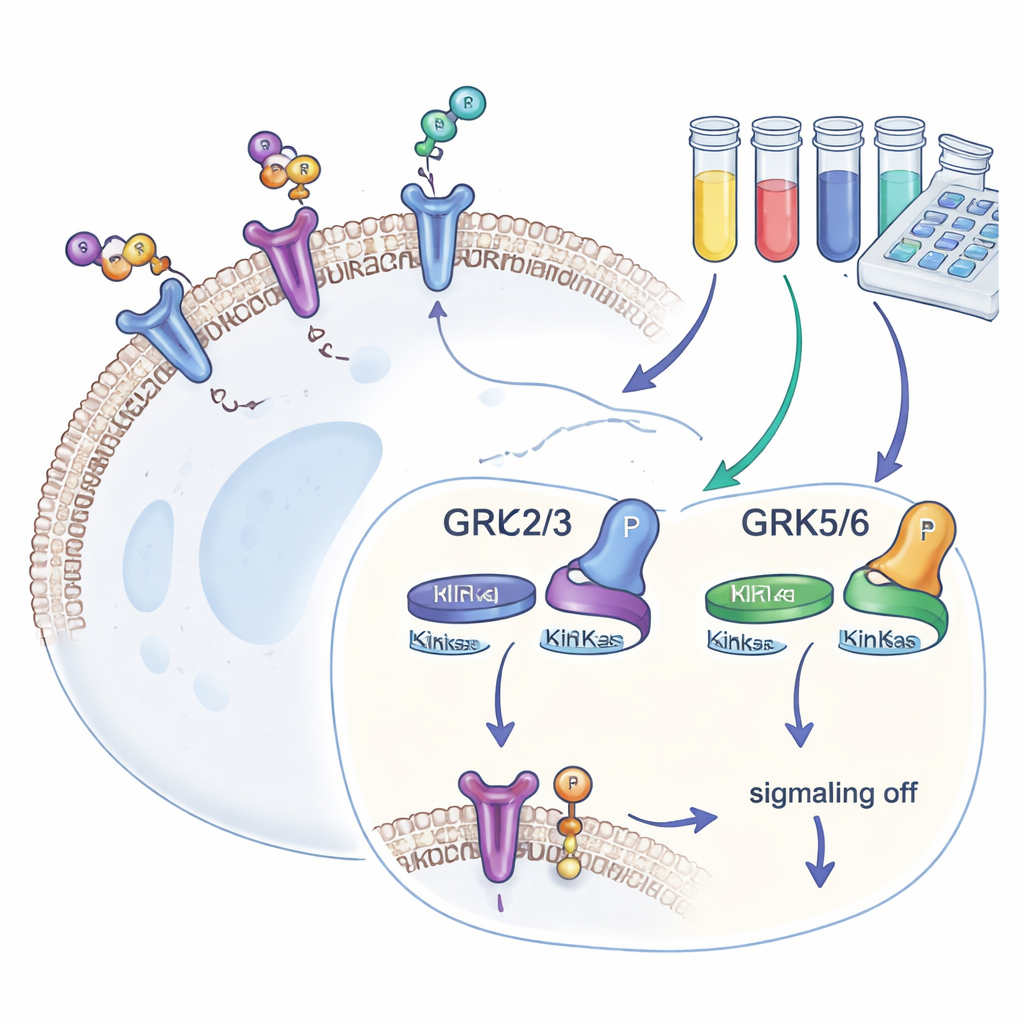
В наших клетках присутствуют сотни типов рецепторов, связанных с G-белком (GPCR), которые обнаруживают внешние сигналы и переводят их во внутренние ответы. После активации GPCR на его хвостовую часть GRK навешивают небольшие фосфатные «флажки». Эти метки привлекают белок бета-аррестин, который прекращает дальнейшую передачу сигнала и часто втягивает рецептор внутрь клетки. Четыре распространённые версии GRK — GRK2, GRK3, GRK5 и GRK6 — встречаются во многих тканях. Поскольку они определяют силу ответа GPCR и их уровни изменяются при таких заболеваниях, как сердечная недостаточность, рак и зависимость, разработчики лекарств заинтересованы в поиске блокаторов GRK, обладающих высокой активностью и селективностью.
Создание «чистой» испытательной площадки внутри клеток
Большинство предшествующих исследований GRK опирались на компьютерное моделирование или реакции в пробирке, которые показывают, насколько прочно ингибитор связывается, но не демонстрируют его работу в тесной среде живой клетки. Чтобы устранить этот разрыв, авторы создали клетки человеческой линии HEK293, лишённые всех четырёх распространённых GRK, и затем поочерёдно вводили только одну изоформу GRK. Каждая линия клеток также содержала хорошо изученный рецептор — бета-2 адренорецептор — с меткой, позволяющей считывать фосфорилирование в конкретной хвостовой позиции (обозначенной как T360/S364) с помощью чувствительного антительного анализа. Поскольку эту позицию модифицируют только GRK, количество фосфата служит прямой количественной мерой активности каждой изоформы GRK в живых клетках.
Отличение хороших, слабых и неспецифичных ингибиторов
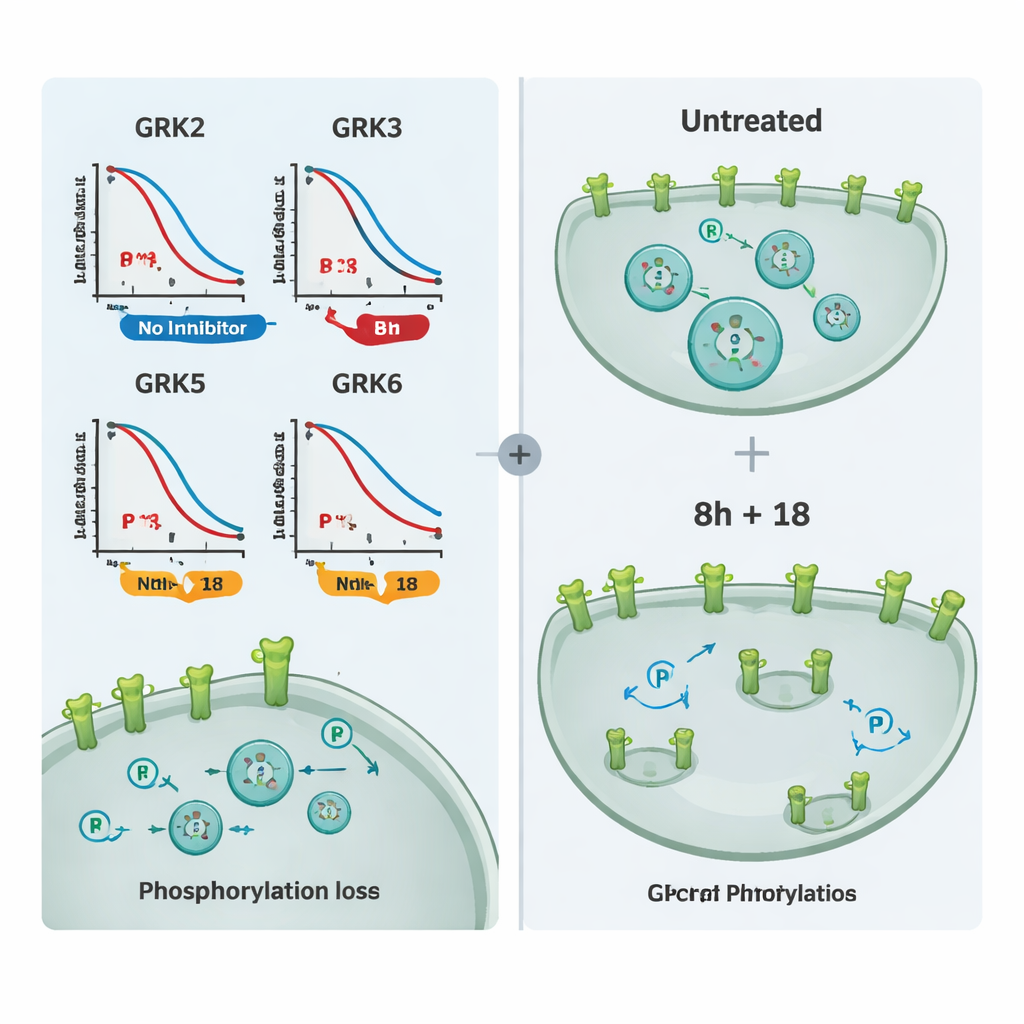
Используя этот набор методов, команда тестировала панель коммерчески доступных блокаторов GRK. Сначала они разделили соединения на группы: те, что преимущественно нацелены на GRK2 и GRK3, и другую группу, направленную на GRK5 и GRK6. Сравнивая, насколько каждое молекула снижала фосфорилирование рецептора в клетках, экспрессирующих только одну подтипную форму GRK, исследователи смогли составить карту реальной селективности. Одно соединение, названное 8h, проявило себя как самый мощный блокатор GRK2/3, тогда как соединение 18 выделялось селективным ингибированием GRK5/6. Некоторые широко используемые молекулы показали слабый эффект при тестируемых дозах, вероятно потому, что плохо проникали в клетки, а один очень мощный ковалентный ингибитор нарушал здоровье клеток, делая его непригодным для экспериментов с визуализацией.
От химических отпечатков к поведению рецептора
Чтобы показать, что эти ингибиторы влияют не только на один тестовый рецептор, но и на биологию GPCR в целом, авторы изучили несколько медицински значимых рецепторов, включая мю-опиоидный рецептор и вазопрессиновый V2-рецептор. Они измеряли как фосфорилирование, так и внутрение перемещение рецепторов с помощью микроскопии. По отдельности 8h или 18 частично снижали фосфорилирование и внутреннее перемещение рецепторов для многих целей, но сочетание 8h и 18 почти полностью предотвращало эти изменения и удерживало рецепторы на поверхности клетки. Дополнительные эксперименты по отслеживанию привлечения бета-аррестина подтвердили, что те же соединения способны модулировать сигнализацию у других рецепторов, регулируемых пересекающимися наборами GRK.
Что это значит для будущих лекарств
Для неспециалистов ключевая мысль такова: исследование предоставляет надёжный набор клеточных тестов — и два особенно полезных инструментальных соединения, 8h и 18 — которые позволяют исследователям видеть в живых клетках, как именно ослабляются разные изоформы GRK. Вместо догадок на основе упрощённых данных из пробирки учёные теперь могут сравнивать кандидатов бок о бок и решать, влияют ли они преимущественно на GRK2/3, на GRK5/6 или на все четыре сразу. Такая ясность должна ускорить разработку лекарств, способных более точно модулировать GPCR-сигнализацию, с потенциальной пользой для лечения сердечных заболеваний, рака, болевых расстройств и других состояний, где нарушен баланс сигнализации.
Цитирование: Blum, N.K., Kiefer, M.C., Decker, A. et al. Cell-based and isoform-selective G protein-coupled receptor kinase assays for comprehensive inhibitor evaluation. Commun Biol 9, 287 (2026). https://doi.org/10.1038/s42003-026-09568-0
Ключевые слова: GPCR-сигнализация, ингибиторы GRK, бета-адренорецептор, клеточный тест, поиск лекарств