Clear Sky Science · ru
Метаболит кишечника индол‑3‑уксусная кислота усугубляет нейропсихиатрическую форму волчанки через путь AHR/STAT3 в микроглии
Как кишечные микробы влияют на мозг
У людей с волчанкой, аутоиммунным заболеванием, иногда развиваются серьёзные нарушения мышления, настроения и памяти — состояние, называемое нейропсихиатрической волчанкой. Эти проявления со стороны мозга могут привести к инвалидизации, однако врачам по‑прежнему трудно точно объяснить их причину и найти эффективные методы лечения. В этом исследовании рассматривается неожиданный подозреваемый: определённые кишечные бактерии и вещества, которые они вырабатывают, — эти молекулы могут перемещаться из кишечника в мозг и разжигать там воспаление.
От микробов кишечника к проблемному поведению
Учёные начали с вопроса, отличаются ли микробы кишечника у пациентов с нейропсихиатрической волчанкой по своим эффектам от микробов пациентов с волчанкой, но без мозговых симптомов. Они пересадили бактерии из фекалий каждой группы пациентов здоровым мышам, предварительно очищенным от собственной микробиоты. Мыши, получившие микробиоту от пациентов с нейропсихиатрической волчанкой, проявляли больше поведенческих признаков тревоги, симптомы депрессии и нарушения обучения и памяти, чем мыши, которым пересаживали микробы от других пациентов с волчанкой. В их мозге наблюдали повышенную активацию микроглии — иммунных клеток мозга — и повышенные уровни провоспалительных молекул. Защитный барьер вокруг мозга, известный как гематоэнцефалический барьер, у этих животных также был более проницаемым, что говорит о том, что что‑то в пересаженной микробиоте повреждало этот критически важный барьер.
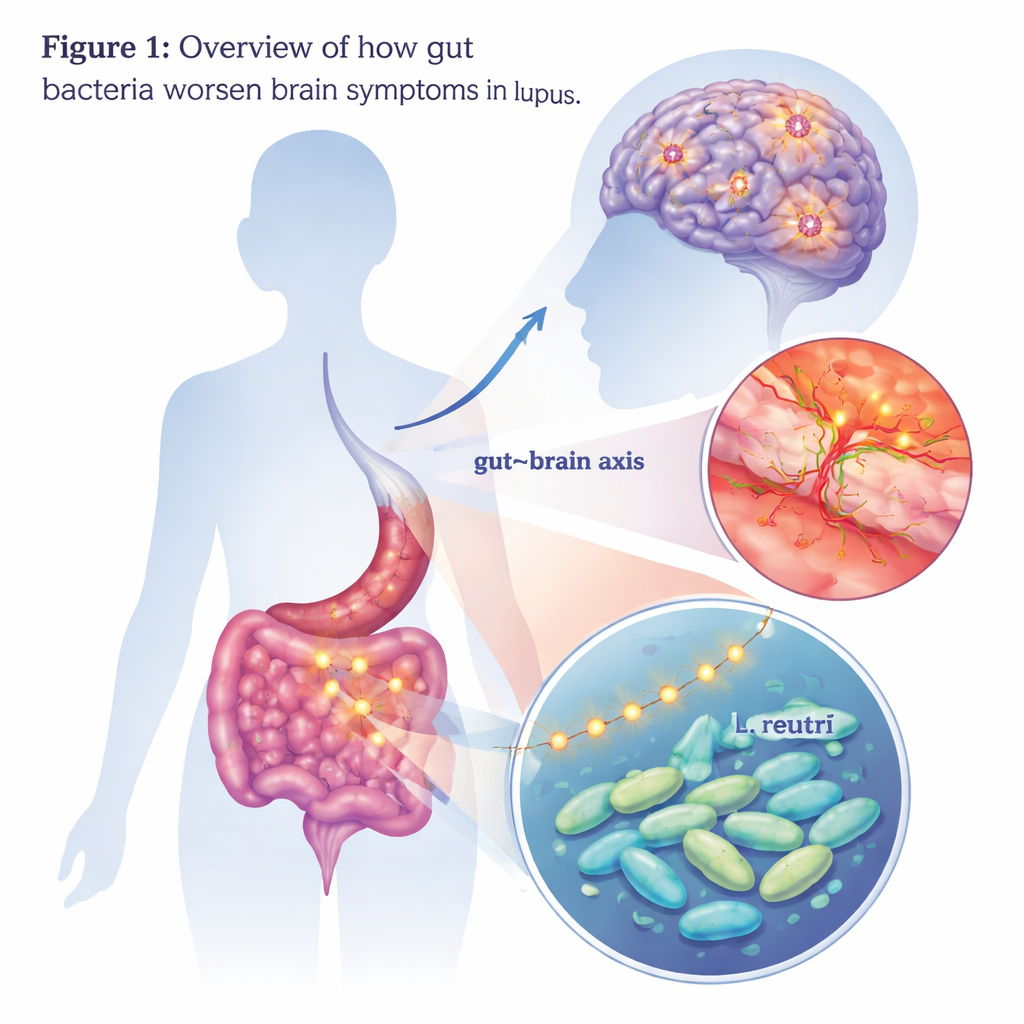
Внимание к одной бактерии
Чтобы выяснить, какие именно микробы могут быть ответственны, команда сравнила состав кишечной микробиоты пациентов и мышей. Выделилась одна группа: Lactobacillus, а в особенности вид Lactobacillus reuteri, был более представлен у пациентов с нейропсихиатрической волчанкой и у мышей с изменениями в мозге. Когда учёные скармливали L. reuteri в одиночку мышам, предрасположенным к волчанке, у животных усиливались тревожные и депрессивные поведенческие реакции, а также ухудшались показатели памяти. В их мозге наблюдали более активную микроглию, большую потерю нейронов и дальнейшее нарушение гематоэнцефалического барьера. Эти результаты указывают на то, что, по крайней мере в контексте волчанки, эта обычно считающаяся пробиотической бактерия может приобрести более вредную роль.
Маленькая молекула — большие последствия
L. reuteri известна тем, что синтезирует молекулу индол‑3‑уксусную кислоту (IAA) из пищевого триптофана. С помощью чувствительных химических анализов команда обнаружила более высокие уровни IAA в кале пациентов с нейропсихиатрической волчанкой по сравнению с другими пациентами с волчанкой и подтвердила, что культуры L. reuteri производят намного больше IAA, чем обычные кишечные бактерии, такие как Escherichia coli. У пациентов с нейропсихиатрической волчанкой уровни IAA в ликворе коррелировали с повышенными уровнями провоспалительных цитокинов, что даёт основание полагать, что эта молекула может достигать центральной нервной системы и вызывать воспаление. У мышей, предрасположенных к волчанке, кормление L. reuteri повышало уровни IAA в кишечнике, крови и мозге. Введение только IAA этим мышам воспроизводило многие из тех же изменений: аномальное поведение, активацию микроглии, повышенные провоспалительные сигналы и ослабление гематоэнцефалического и кишечного барьеров.
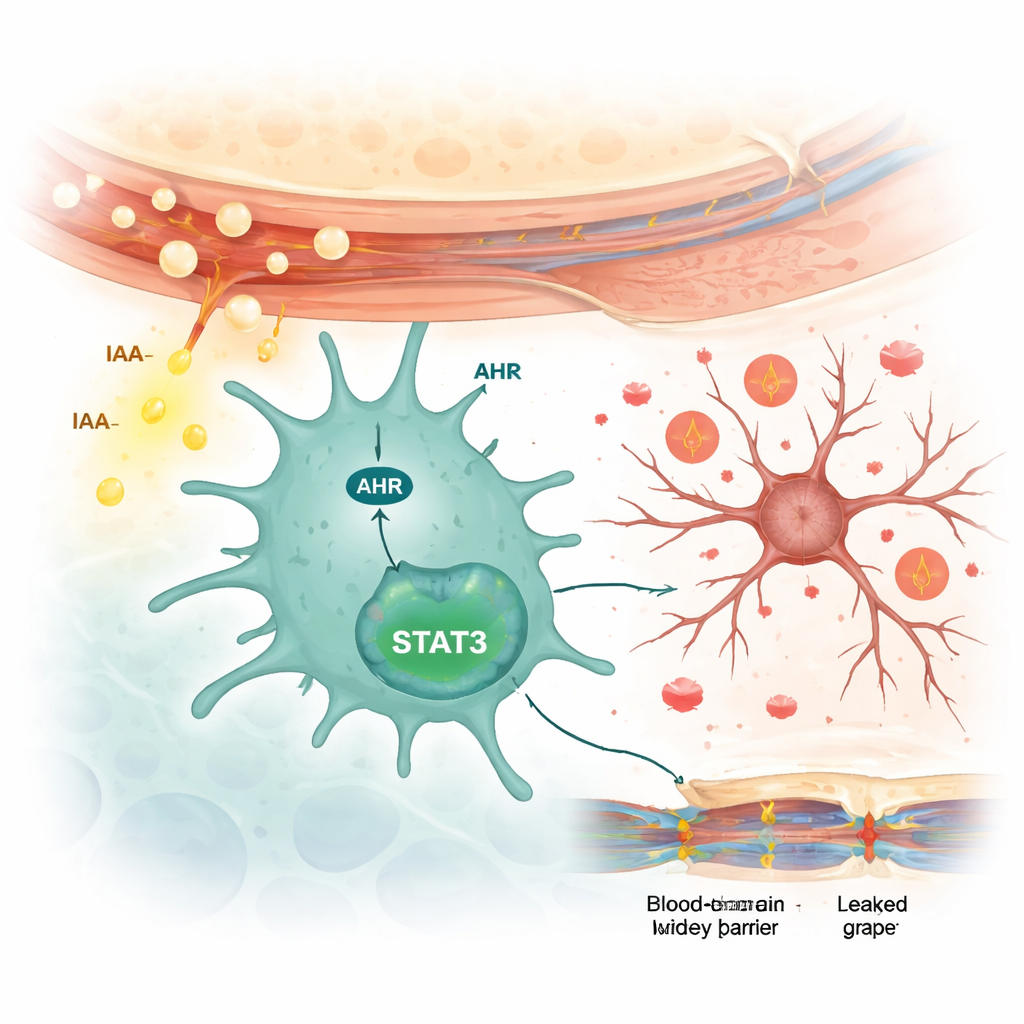
Как включаются иммунные клетки мозга
Затем учёные изучили, как IAA взаимодействует с клетками мозга. Они обнаружили, что IAA повышает активность сенсорного белка арильного гидрокарбонного рецептора (AHR) специфически в микроглии, но не в нейронах или астроцитах — звездчатых поддерживающих клетках. В культуре микроглиальных клеток IAA увеличивал уровни AHR и активировал связанный сигнальный белок STAT3, который, в свою очередь, стимулировал продукцию провоспалительных цитокинов. Блокирование AHR с помощью препарата предотвращало активацию STAT3 и снижало выделение этих воспалительных сигналов. Когда мышам, предрасположенным к волчанке, давали препарат‑ингибитор AHR, их тревожно‑депрессивные проявления уменьшались, активация микроглии снижалась, уровень воспалительных молекул падал, а гематоэнцефалический барьер становился менее проницаемым.
Что это значит для пациентов
В сумме исследование описывает цепочку событий, связывающую кишечник и мозг при нейропсихиатрической волчанке. Избыточное количество L. reuteri в кишечнике приводит к повышенному образованию IAA, что ослабляет кишечный барьер и позволяет молекуле попадать в кровоток. IAA затем достигает мозга, где активирует в микроглии сигнализацию через AHR и STAT3, запускающую воспаление, повреждающее нейроны и нарушающее гематоэнцефалический барьер. Для пациентов эти данные означают, что в перспективе изменение состава кишечной микробиоты, снижение уровней вредных метаболитов, таких как IAA, или блокирование пути AHR/STAT3 в микроглии могут помочь защитить мозг от разрушительных эффектов нейропсихиатрической волчанки.
Цитирование: Feng, Y., Zheng, L., Tang, W. et al. Gut metabolite indole-3-acetic acid aggravates neuropsychiatric lupus via the AHR/STAT3 pathway in microglia. Commun Biol 9, 281 (2026). https://doi.org/10.1038/s42003-026-09561-7
Ключевые слова: нейропсихиатрическая волчанка, микробиота кишечника, Lactobacillus reuteri, воспаление микроглии, гематоэнцефалический барьер