Clear Sky Science · ru
Радионуклид-индуцированная динамическая терапия вызывает дополнительные иммуноактивные пути гибели раковых клеток: некроптоз и апоптоз
Обратить трюки рака против него самого
Рак известен своей способностью уклоняться от лучших методов лечения, особенно агрессивные опухоли груди, дающие метастазы по всему организму. В этом исследовании рассматривается изобретательный подход, называемый радионуклид-стимулированной динамической терапией (RaST), который использует диагностические радионуклидные трассеры и светочувствительные наноматериалы для уничтожения раковых клеток способами, одновременно активирующими иммунную систему. Это важно, потому что работа показывает, как существующие инструменты визуализации и «умные» материалы можно перенастроить для более длительного иммунного контроля заболевания, а не только для временного уменьшения опухоли.
Новый способ подсветить опухоль изнутри
Традиционные световые методы лечения рака эффективны лишь там, куда может дойти внешний луч, например на коже или поверхностных опухолях. RaST обходит это ограничение, используя радиоактивный сахар, похожий на трассер, применяемый в ПЭТ, который накапливается в быстрорастущих раковых клетках. По мере прохождения через опухоль этот трассер испускает слабое голубое свечение, известное как черенковское излучение. Исследователи разработали крошечные наночастицы диоксида титана, покрытые белком, нацеленным на опухоль, чтобы они тоже накапливались в новообразовании. Когда трассер и наночастицы встречаются, внутренний свет активирует частицы, которые в свою очередь генерируют всплески реактивных форм кислорода — высокореактивных молекул, повреждающих раковые клетки изнутри.
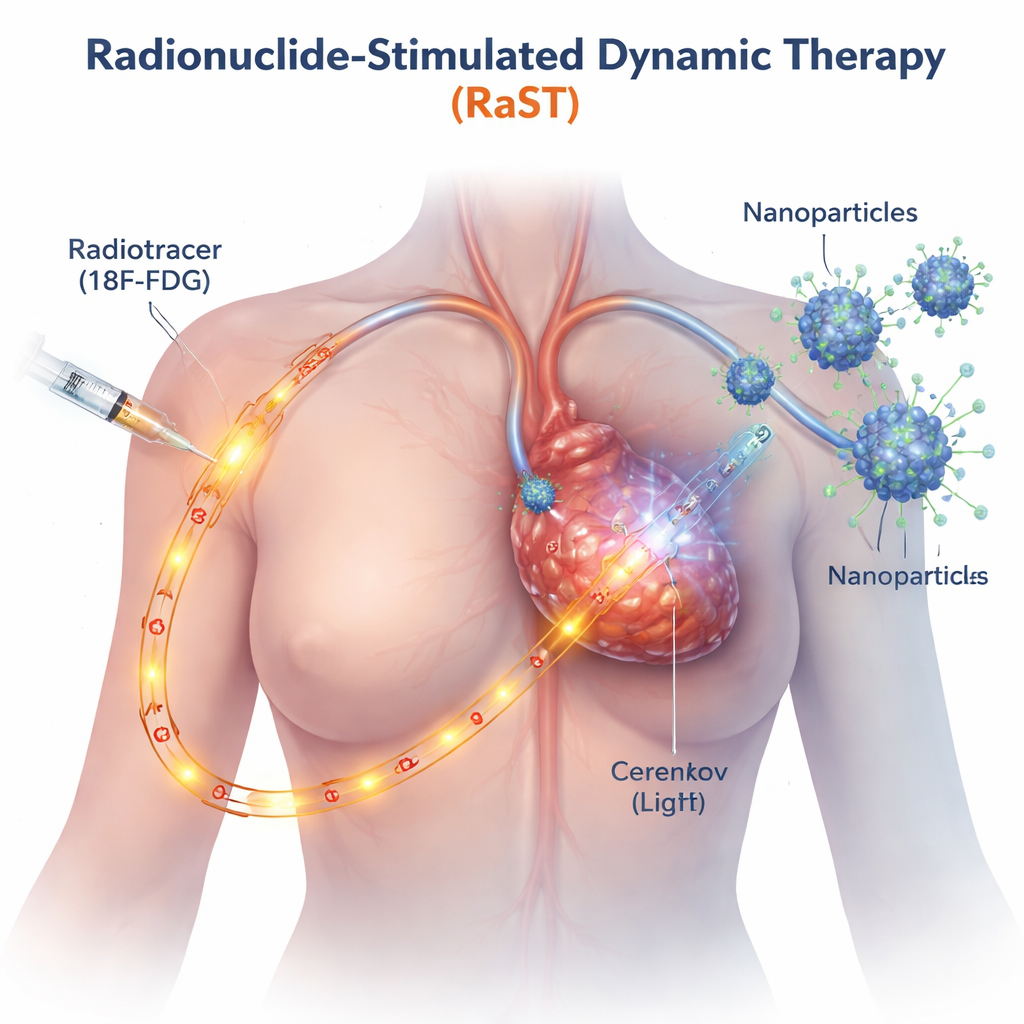
Запуск двух различных путей гибели клеток
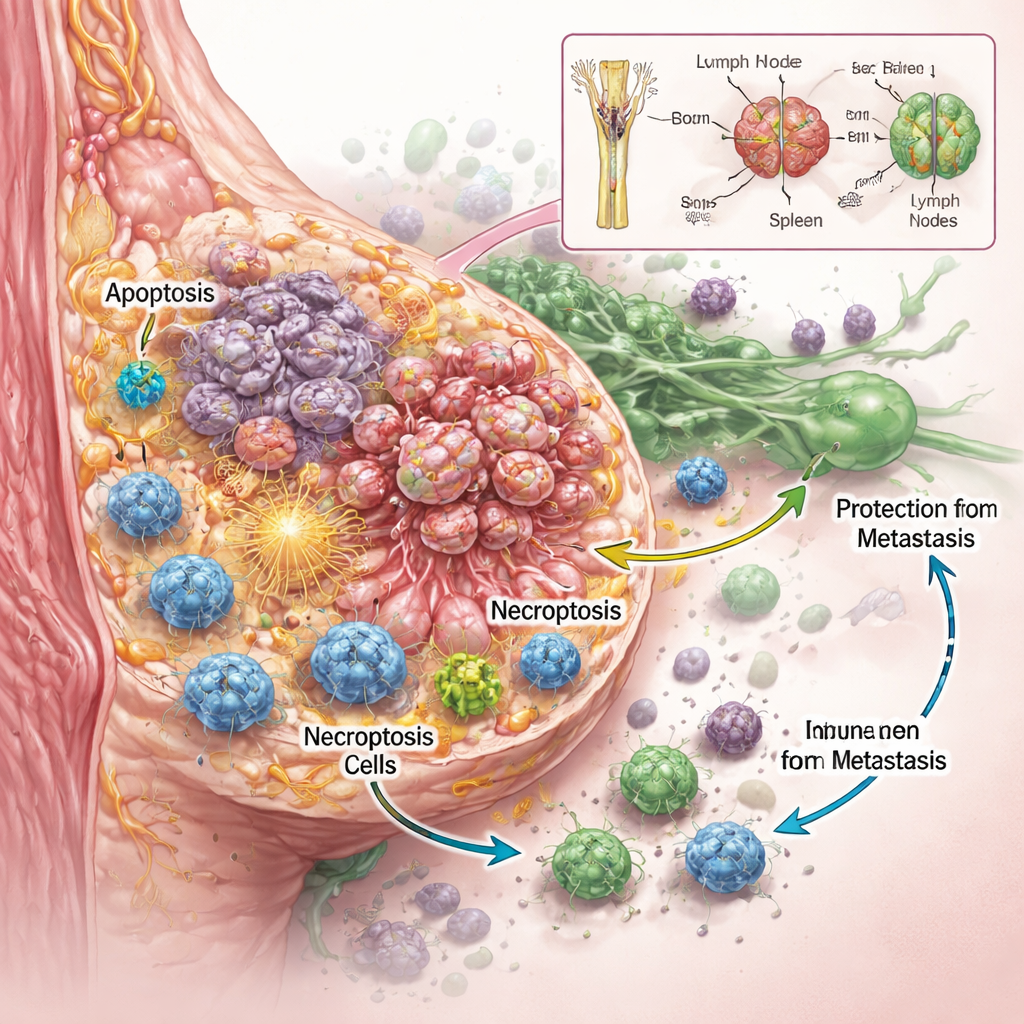
Команда хотела понять не только то, убивает ли RaST раковые клетки, но и как именно. На нескольких агрессивных линиях раковых клеток молочной железы в лаборатории они обнаружили, что тщательно подобранные дозы радиоактивного трассера и наночастиц действуют совместно, повреждая опухолевые клетки эффективнее, чем каждый компонент по отдельности, даже в типах, устойчивых к стандартной химиотерапии. Детальное изображение и измерения белков показали, что RaST одновременно активирует две регулируемые программы гибели клеток. Одна — апоптоз, часто описываемый как клеточное «самоубийство», при котором клетка упорядоченно распадается. Другая — некроптоз, более взрывоподобная форма гибели, при которой клетки набухают, разрываются и выбрасывают молекулярные сигналы бедствия в окружающую среду. Эти сигналы, известные как молекулы, ассоциированные с повреждением, и воспалительные цитокины, могут служить маяками, привлекающими и активирующими иммунные клетки.
Привлечение иммунной системы для длительного контроля
Чтобы проверить, важен ли такой воспалительный способ уничтожения опухоли в живом организме, исследователи испытали RaST на мышиных моделях рака молочной железы. У мышей с ослабленным иммунитетом RaST мало что менял в росте опухоли или в метастазировании в легкие, несмотря на обильную локальную гибель клеток. Но у животных с неповрежденной иммунной системой то же лечение вызывало частичные и полные ответы опухолей и предотвращало метастазирование в легкие. В опухолях после RaST накапливались иммунные клетки — особенно миелоидные клетки, такие как макрофаги и дендритные клетки, — которые эффективно поглощают мертвый материал и представляют фрагменты опухоли Т-клеткам. Анализы крови показывали волны иммунно-стимулирующих и иммунно-регулирующих сигналов с течением времени, что указывает на то, что RaST сначала разжигает атаку на опухоль, а затем смещает ответ к более сбалансированному состоянию по мере уменьшения или стабилизации опухолей.
Поиск скрытых остатков и защита от рецидива
Даже у мышей, у которых опухоли казались полностью излеченными после RaST, высокочувствительный контрастный краситель позже выявил крошечные очаги оставшихся раковых клеток в лимфатических узлах. Удивительно, но эти животные в течение многих месяцев не развивали новых опухолей и отдаленных метастаз. Химические анализы показали, что наночастицы диоксида титана, первоначально в больших количествах в костях и печени, постепенно перераспределялись в селезенку и лимфатические узлы — как раз в те центры, где патрулируют иммунные клетки. Это медленное перемещение, вероятно, поддерживает локальный источник реактивного кислорода для иммунных клеток, помогая им распознавать и контролировать скрытые остатки опухоли до того, как те смогут возобновить рост или распространение.
Что это может значить для будущего лечения рака
Проще говоря, работа демонстрирует, что RaST — это не просто еще один способ отравить опухолевые клетки. Сочетая радиоактивные трассеры, светочувствительные наночастицы и собственные защитные силы организма, метод переводит раковые клетки в две формы программируемой гибели, которые громко сигналят иммунной системе. У животных с полноценным иммунитетом это приводит к длительному контролю агрессивных опухолей молочной железы и блокирует метастазирование, даже если несколько клеток остаются в лимфоузлах. Хотя до широких клинических испытаний еще многое предстоит сделать, исследование указывает путь к будущим лечением, цель которых не просто уменьшить опухоль, а перестроить отношения между раком, клеточной смертью и иммунитетом, чтобы организм сам помогал держать болезнь под контролем в долгосрочной перспективе.
Цитирование: Egbulefu, C., Black, K., Su, X. et al. Radionuclide-stimulated dynamic therapy induces complementary immunogenic necroptosis and apoptosis cancer cell death pathways. Commun Biol 9, 275 (2026). https://doi.org/10.1038/s42003-026-09555-5
Ключевые слова: рак молочной железы, наночастицы, иммунотерапия, радионуклидная терапия, некроптоз