Clear Sky Science · ru
Гликофагия — древний билияриальный путь, поддерживающий метаболическую адаптацию через структурную эволюцию STBD1
Как устрицы раскрывают скрытые энергитические трюки
Живые существа переживают трудные периоды, используя запасы топлива, но не все полагаются на один и тот же «аккумулятор». Это исследование посвящено тихоокеанским устрицам и показывает, что в отличие от многих других животных, которые опираются на жир, устрицы в значительной степени зависят от запасов сахара в виде гликогена. Работа выявляет малоизвестный путь клеточного рециркулирования — называемый гликофагией — который помогает устрицам быстро расходовать и пополнять сахарные запасы, и прослеживает, как эта система развивалась в животном царстве.
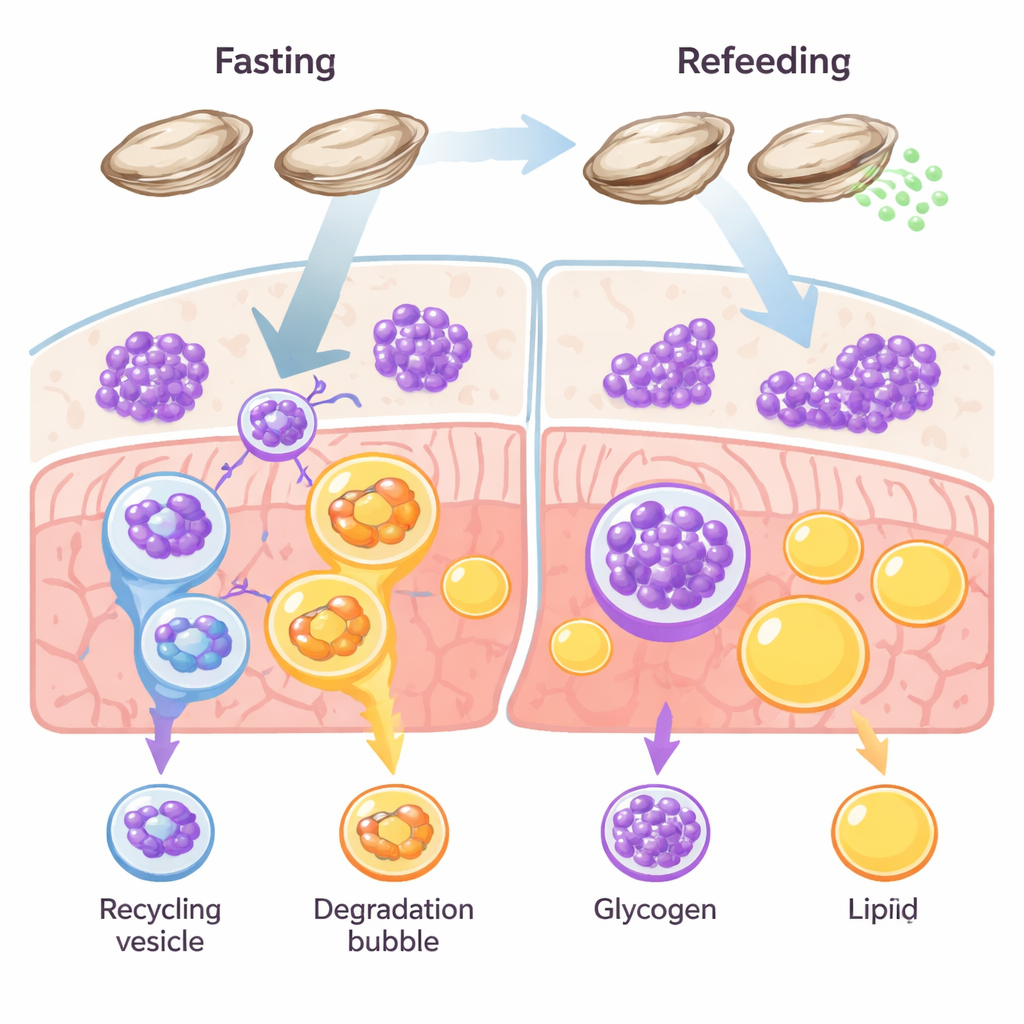
Стратегия выживания, основанная на сахаре
Большинство животных используют несколько энергетических резервов, главным образом жиры и гликоген. У позвоночных, таких как рыбы и млекопитающие, в качестве долгосрочного хранилища чаще доминирует жир. Устрицы ломают это правило. Их ткани насыщены гликогеном, и ранее полученные данные указывали на то, что эти моллюски расходуют сахар, а не жир, когда пища становится дефицитной или при производстве икры и сперматозоидов. Авторы поставили задачу проверить, выступает ли гликофагия — целенаправленное разрушение гликогена внутри клеток — основным путем выживания устриц в условиях голодания и восстановления.
Наблюдение за переключением клеток от накопления к расходованию
Исследователи голодали тихоокеанских устриц в течение двух недель, а затем вновь кормили их, отслеживая реакцию тканей во времени. Во время голодания микроскопические окрашивания показали всплеск маркеров аутопагии — сигналов клеточной «уборки» — именно там, где хранился гликоген, в то время как сам гликоген уменьшался. Запасы жира, напротив, практически не изменялись. После повторного кормления гликоген быстро восстанавливался, а сигналы аутопагии падали. Одновременно уровни ключевого рецепторного белка STBD1, который специфически связывает гликоген с аппаратурой аутопагии, повышались и понижались в такт использованию гликогена. Другой рецептор, связанный с утилизацией жира — p62 — оставался относительно стабильным. Вместе эти закономерности указывают на специализированный, ориентированный на сахар путь рециркуляции: гликофагия, а не липофагия (разрушение жира), берёт на себя основную роль в энергетическом балансе устриц.
Молекулярный «крючок», который захватывает гликоген
Гликофагия зависит от того, что STBD1 действует как молекулярный крючок: он связывает гликоген и передаёт его мелким адаптерным белкам, которые формируют везикулы для рециркуляции. У устриц STBD1 оказался устроен иначе, чем у позвоночных. Устриный белок несёт свой гликоген-связывающий участок, известный как домен CBM20, на переднем конце (N-конце), тогда как у позвоночных CBM20 расположен на заднем конце (C-конце) и включает дополнительный гидрофобный хвост, якорящий его к клеточным мембранам. Компьютерные модели и моделирование предложили, что N-конфигурация у устриц даёт CBM20 более прочное и универсальное сцепление с разветвлёнными сахарными цепями. Лабораторные эксперименты подтвердили это: очищенный устриный STBD1 связывал гликоген сильнее, чем STBD1 рыбы или мыши, и когда все версии экспрессировали в человеческих клетках, устриный белок вызывал более резкое падение гликогена при индуцированной аутопагии.
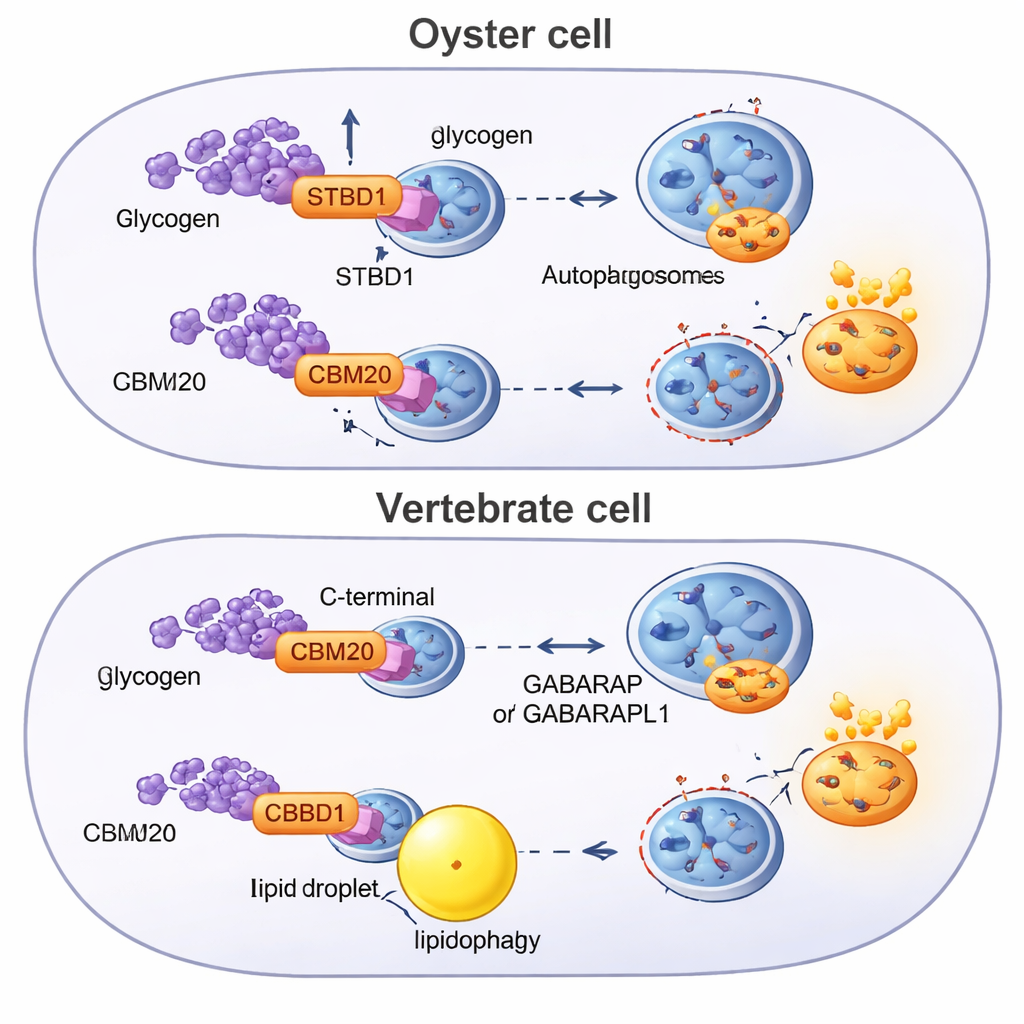
Переконфигурация древнего пути у разных животных
Чтобы понять происхождение этой системы, исследователи просканировали геномы десятков животных в поисках белков с доменом CBM20 и построили эволюционные деревья. Они обнаружили, что STBD1 — это изобретение билиатерий — появившееся у общего предка животных с двусторонней симметрией тела — но его структура была переработана в разных линиях. Устрицы и другие лофотрохофоаны, как правило, сохраняют исходную N-концевую схему с CBM20, иногда даже дублируя модуль связывания сахара. Хордовые, группа, включающая позвоночных, демонстрируют отличную версию, в которой CBM20 перемещён в хвостовую часть белка. Эта перестановка коррелирует с более слабым связыванием гликогена и с метаболической стратегией, более ориентированной на расщепление жиров через липофагию, поддерживаемую другими рецепторами аутопагии и адаптерными белками, которых у устриц нет.
Что это значит для энергетического выбора жизни
Для неспециалистов главный вывод таков: животные эволюционировали не одним способом справляться с энергетическим дефицитом. Устрицы демонстрируют древнюю, ориентированную на сахар стратегию: высокоаффинная версия STBD1 быстро захватывает гликоген и направляет его в клеточные рециркуляционные структуры, делая гликофагию главным источником энергии при стрессе. Позвоночные, напротив, похоже, в какой-то мере пожертвовали этой сильной «сахарной хваткой» в пользу более сбалансированного или жирово-ориентированного подхода, поддерживаемого другими белковыми партнёрами и схемами доменов. Связывая детальную структуру белков с выбором топлива целым организмом, это исследование иллюстрирует, как небольшие молекулярные «перенастройки» могут помочь разным ветвям животного древа адаптироваться к своим средам и образу жизни.
Цитирование: Ren, L., Bai, Y., Shi, C. et al. Glycophagy is an ancient bilaterian pathway supporting metabolic adaptation through STBD1 structural evolution. Commun Biol 9, 268 (2026). https://doi.org/10.1038/s42003-026-09546-6
Ключевые слова: гликофагия, метаболизм гликогена, биология устриц, аутопагия, эволюция метаболизма