Clear Sky Science · ru
Эпигенетическая и метаболическая перенастройка при метастатических феохромоцитомах и параганглиомах, вызванная мутациями SDHB
Почему эти редкие опухоли имеют значение
Феохромоцитомы и параганглиомы — редкие опухоли, развивающиеся из гормонопродуцирующих нервных клеток, часто рядом с надпочечниками. Большинство растут медленно и поддаются хирургическому иссечению, но приблизительно у одного из пяти пациентов опухоль в конце концов распространяется в другие органы и становится опасной для жизни. В этом исследовании поставлен простой, но ключевой вопрос: что заставляет некоторые из этих опухолей становиться опасными? Глубокий анализ того, как эти раки включают и выключают гены, и как они получают энергию, выявляет скрытую уязвимость, которую в будущем можно будет использовать для новых методов лечения.
От тихого роста к смертоносному метастазированию
Исследователи сосредоточились на опухолях с изменениями в гене SDHB. SDHB помогает митохондриям — энергетическим станциям клетки — функционировать в части цикла Кребса, ключевого пути производства энергии. При повреждении SDHB накапливается соединение сукцинат, и клетки начинают вести себя так, будто испытывают дефицит кислорода, даже когда его достаточно. Авторы изучили ткани 34 пациентов, сравнив локализованные опухоли с уже метастазирующими. С помощью подробной карты метилирования ДНК — которая показывает, какие химические метки усиливают или подавляют гены — они обнаружили, что у метастатических опухолей наблюдается более выраженный профиль подавления генов по сравнению с доброкачественными, особенно при наличии мутаций SDHB.
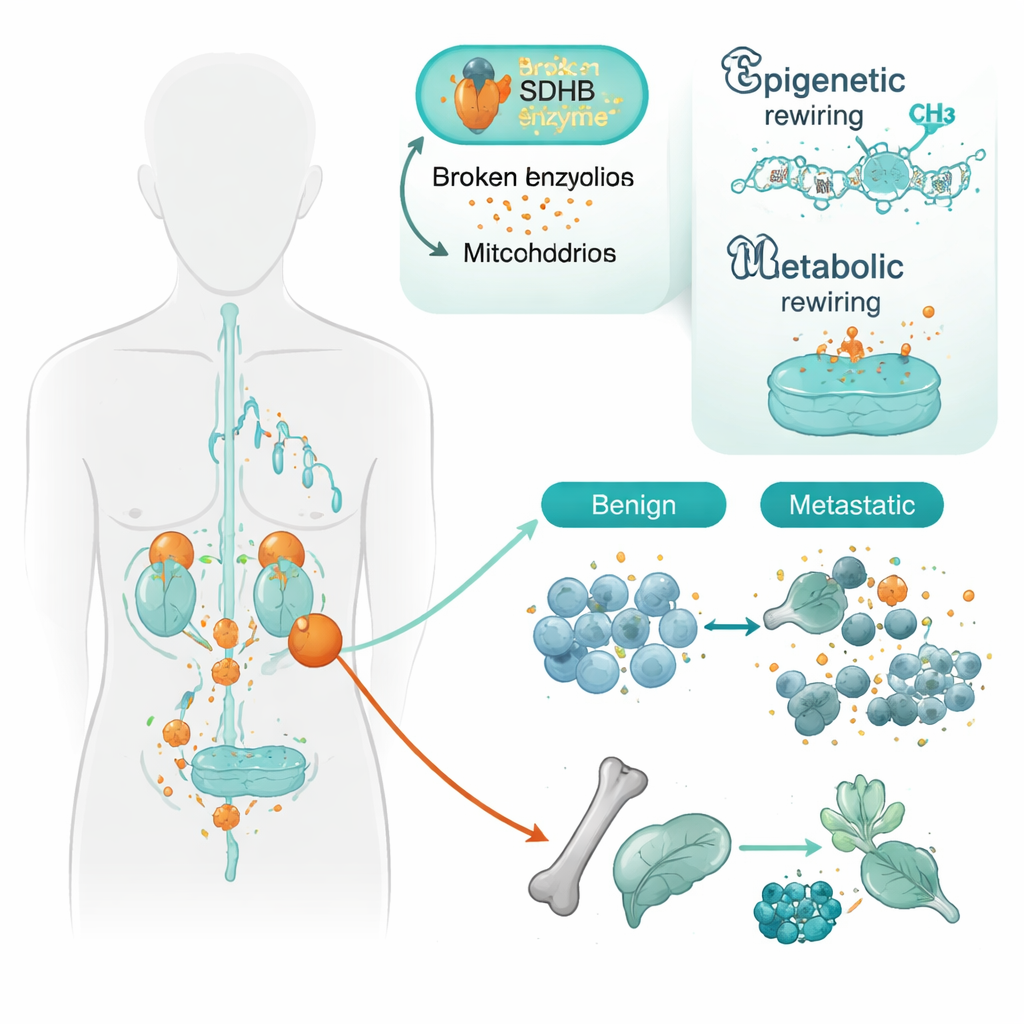
Перепрограммирование клеточной идентичности
Многие из генов, заглушённых в агрессивных опухолях, отвечают за созревание нервоподобных клеток и поддержание их специализированной идентичности. Сюда входят семейства генов, которые управляют клеточной адгезией, организацией ДНК и решением о типе дифференцировки клетки. Ярким примером стал ген клеточной адгезии PCDHGC3. Даже в не метастазирующих опухолях с мутацией SDHB участки регуляции этого гена были уже частично выключены; в метастазах подавление было ещё сильнее. Другой ген, SATB2, участвующий в организации больших участков ДНК, оказался выключенным только в метастатических опухолях независимо от статуса SDHB. В совокупности эти паттерны указывают на то, что утрата SDHB «подготавливает» клетки к менее зрелому, более подвижному состоянию, а дополнительные эпигенетические изменения затем помогают им отделяться и распространяться.
Перенастройка потребления сахаров опухолями
Удивительно, но не все изменения приводили к подавлению генов. Небольшая группа генов стала менее метилированной и более активной, и они были тесно связаны с транспортом сахаров в клетки. Среди них выделялся ген транспортёра фруктозы SLC2A5. Его продукт, известный как GLUT5, переносит фруктозу — сахар, распространённый в плодах и многих переработанных продуктах — в клетки. В лабораторных моделях клеток, имитирующих опухолевые и находящихся в условиях низкого кислорода, SLC2A5 постепенно включался, тогда как другие транспортеры сахаров реагировали менее последовательно. Авторы затем получили культуры клеток, полученные от пациентов с PPGL, и показали, что при дефиците глюкозы добавление фруктозы помогало этим клеткам продолжать делиться, особенно в условиях низкого кислорода, которые имитируют микроокружение опухоли.
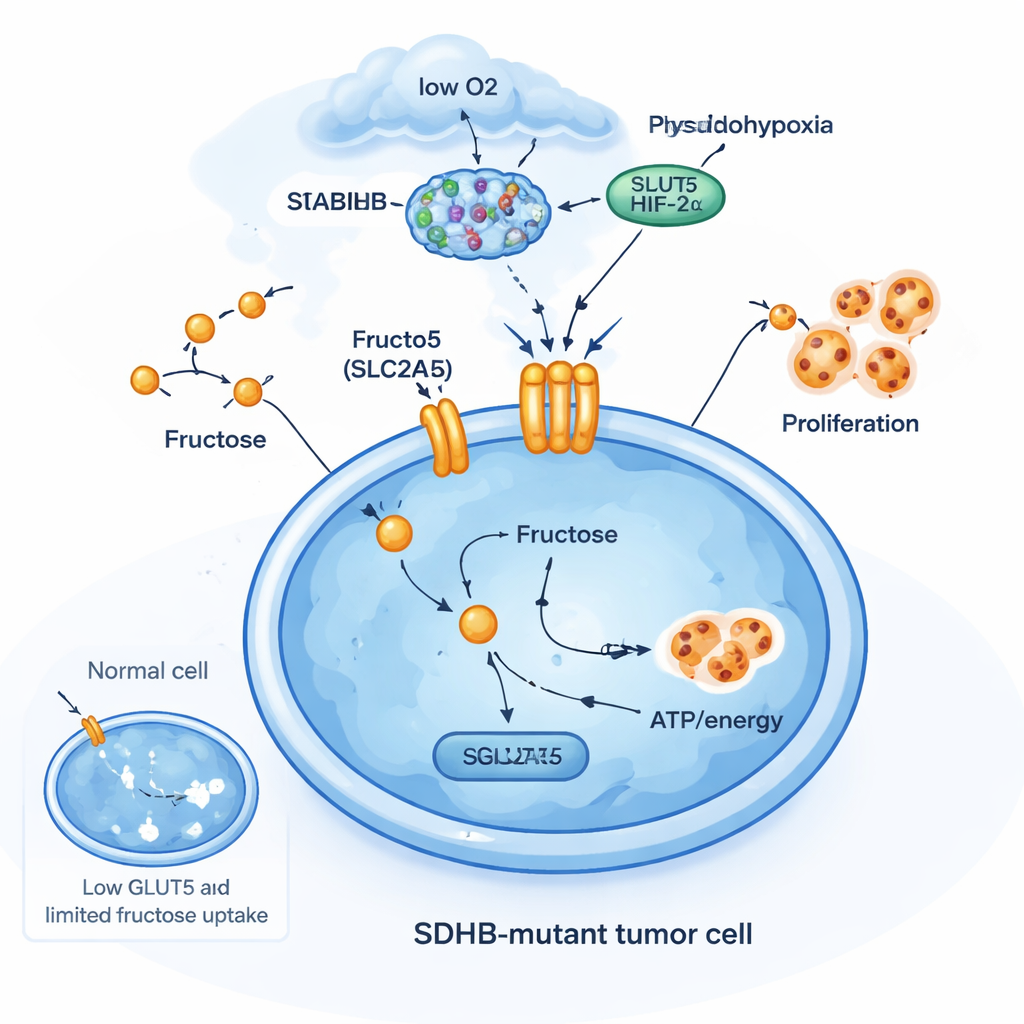
Приём выживания на фруктозе
Чтобы понять, почему здесь важны мутации SDHB, команда отредактировала несколько типов клеток, удалив SDHB. В хромаффиноподобных клетках надпочечника и в клеточной линии рака почки с постоянной активацией фактора HIF2α потеря SDHB усиливала уровни SLC2A5. Но в более распространённых клеточных линиях рака, лишённых этих нейроэндокринных или HIF2α‑характеристик, та же депривация SDHB не активировала SLC2A5. Это показывает, что транспортёр фруктозы не является частью универсального стресс‑ответа; это высокоспецифическая адаптация в определённых типах клеток, уже находящихся в «псевдогипоксическом» состоянии. В этих клетках утрата SDHB, накопление сукцината и активность HIF2α действуют совместно, открывая новый метаболический путь: поглощение фруктозы для подпитки роста при ограничении кислорода и глюкозы.
Что это значит для пациентов
Проще говоря, исследование выявляет двойную перестройку в метастатических PPGL с мутациями SDHB. Во‑первых, их система контроля ДНК перенастраивается так, что клетки становятся менее специализированными и более пластичными, склонными к инвазии. Во‑вторых, их энергетическая система перенастраивается, чтобы использовать фруктозу как альтернативное топливо в суровых нишах с низким содержанием кислорода и глюкозы. Идентификация фруктозного транспортёра SLC2A5/GLUT5 как ключевого участника этого процесса указывает на возможную ахиллесову пяту: блокирование поглощения или метаболизма фруктозы могло бы избирательно лишать эти опухоли энергии, не затрагивая большинство нормальных тканей. Хотя такие терапии пока недоступны, картирование этой эпигенетической и метаболической ландшафтной картины — важный шаг к более точным, ориентированным на метаболизм методам лечения пациентов с высокорисковыми SDHB‑мутациями PPGL.
Цитирование: Cubiella, T., Alba-Linares, J.J., San-Juan-Guardado, J. et al. Epigenetic and metabolic rewiring in metastatic pheochromocytomas and paragangliomas driven by SDHB mutations. Commun Biol 9, 266 (2026). https://doi.org/10.1038/s42003-026-09543-9
Ключевые слова: феохромоцитома, параганглиома, мутация SDHB, эпигенетика, обмен фруктозы